Dòng điện trong chất điện phân - Phương pháp giải bài tập trong chất điện phân
I - BẢN CHẤT DÒNG ĐIỆN TRONG CHẤT ĐIỆN PHÂN
Dòng điện trong chất điện phân là dòng chuyển dời có hướng của các ion dương theo chiều điện trường và các ion âm ngược chiều điện trường
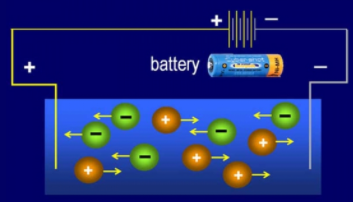
- Chất điện phân: là dung dịch muối, axít, bazơ có khả năng phân li thành ion âm, ion dương.
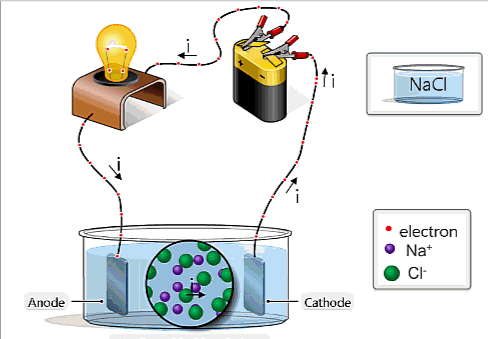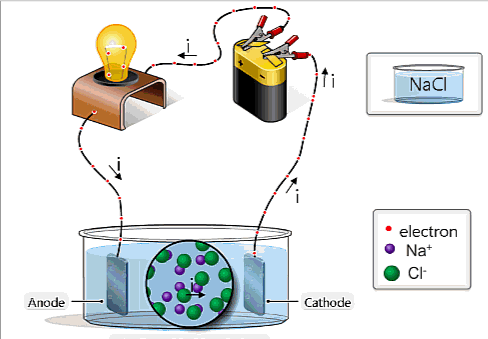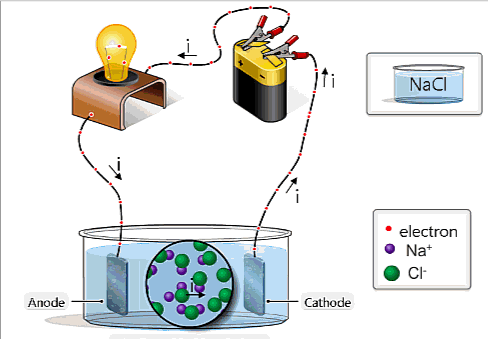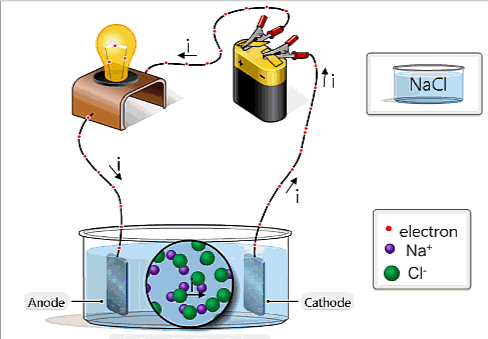
- Chất điện phân không dẫn điện tốt bằng kim loại.
- Dòng điện trong chất điện phân không chỉ tải điện lượng mà còn tải cả vật chất đi theo. Tới điện cực chỉ có các electron có thể đi tiếp, còn lượng vật chất đọng lại ở điện cực, gây ra hiện tượng điện phân.
II - CÁC HIỆN TƯỢNG DIỄN RA Ở ĐIỆN CỰC. HIỆN TƯỢNG DƯƠNG CỰC TAN
- Hiện tượng dương cực tan xảy ra khi điện phân một dung dịch muối kim loại mà anốt làm bằng chính kim loại ấy
+ Các ion chuyển động về các điện cực có thể tác dụng với chất làm điện cực hoặc với dung môi tạo nên các phản ứng hoá học gọi là phản ứng phụ trong hiện tượng điện phân.
+ Hiện tượng dương cực tan xảy ra khi các anion đi tới anôt kéo các ion kim loại của diện cực vào trong dung dịch.
+ Khi có hiện tượng dương cực tan, dòng điện trong mạch tuân theo định luật Ôm, giống như đối với đoạn mạch chỉ có điện trở thuần.
- Hiện tượng giải phóng khí H2 và O2 ở hai điện cực
+ Điều kiện: Dung dịch chất điện phân là H2SO4 , các điện cực được làm bằng Cacbon hoặc inox.
+ Dung dịch chất điện phân: \({H_2}S{O_4} \to {H^ + } + {(S{O_4})^{2 - }}\)
Cực dương dẫn điện nhưng không thể tan vào trong dung dịch điện phân nên các hiện tượng vật lí và hóa học diễn ra ở điện cực phức tạp hơn. Kết quả cuối cùng nước trong dung dịch điện phân bị tách thành H2 và O2 dịch chuyển về hai đầu điện cực.
Ứng dụng của phương pháp trên dùng để điện phân nước biển tạo ra H2 và O2 dùng trong các tàu ngầm hoạt động lâu dưới đáy biển.
III - CÁC ĐỊNH LUẬT FA-RA-ĐÂY
* Định luật Fa-ra-đây thứ nhất
Khối lượng vật chất được giải phóng ở điện cực của bình điện phân tỉ lệ thuận với điện lượng chạy qua bình đó.
\(m = kq\)
k gọi là đương lượng điện hóa, phụ thuộc vào bản chất của chất được giải phóng ra ở cực.
- Trong hệ SI, đơn vị của k là: kg/C
* Định luật Fa-ra-đây thứ hai:
Đương lượng điện hoá k của một nguyên tố tỉ lệ với đương lượng gam \(\frac{A}{n}\) của nguyên tố đó. Hệ số tỉ lệ \(\frac{1}{F}\), trong đó F gọi là số Fa-ra-đây.
\(k = \frac{1}{F}.\frac{A}{n}\)
Kết quả thí nghiệm cho thấy: F ≈ 96500 C/mol.
* Công thức Fa-ra-đây :
\(m = \frac{1}{F}\frac{A}{n}q = \frac{1}{F}.\frac{A}{n}It\)
Trong đó:
+ m là chất được giải phóng ở điện cực (g)
+ I - cường độ dòng điện không đổi đi qua bình điện phân (A)
+ t: thời gian dòng điện chạy qua bình (s)
IV - ỨNG DỤNG CỦA HIỆN TƯỢNG ĐIỆN PHÂN
- Điều chế hóa chất: Clo, hiđrô, xút (NaOH) bằng cách điện phân dung dịch muối ăn
- Luyện kim: Dựa vào hiện tượng dương cực tan để tinh chế kim loại
- Mạ điện: Dùng phương pháp điện phân
+ Vật cần được mạ dùng làm cực âm
+ Kim loại dùng để mạ làm cực dương
+ Chất điện phân là dung dịch muối của kim loại dùng để mạ
