Lời giải của giáo viên
 HocOn247.com
HocOn247.com
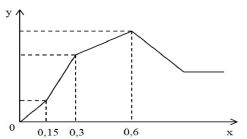
*Đoạn 1:
OH- + H+ → H2O
Ba2+ + SO4 2- → BaSO4
Ta có: nH+ = nOH‑ = 2nBa(OH)2 = 2.0,15 = 0,3 mol
*Đoạn 2:
Ba2+ + SO4 2- → BaSO4
A13+ + 3OH- → Al(OH)3
Ta có: n SO4(2-) = nBa2+ = nBa(OH)2 = 0,3 mol
*Đoạn 3: Al3+ + 3OH- + Al(OH)3
Ta có nOH- = nH+ + 3nAl(OH)3 → nAl(OH)3 max = 0,3 mol
Vậy nHCl = nH+ = 0,3 mol ; nAl2(SO4)3 = 1/3.nSO4(2-) = 0,1 mol
Bảo toàn Al suy ra nAlCl3 = 0,1 mol
Vậy tổng a=0,3 + 0,1 + 0,1 = 0,5 mol
Đáp án A
CÂU HỎI CÙNG CHỦ ĐỀ
Nung nóng 100 gam hỗn hợp gồm \(N{a_2}C{O_3},NaHC{O_3}\) cho đến khối lượng không đổi còn lại 69 gam chất rắn. Thành phần % khối lượng mỗi chất trong hỗn hợp ban đầu là
Ankan Y phản ứng với clo tạo ra 2 dẫn xuất monoclo có tỉ khối hơi so với bằng 39,25.
Tên của Y là
Đốt cháy hoàn toàn 68,2 gam hỗn hợp X gồm glyxin, alanin, axit glutamic và axit oleic, thu được N2, 55,8 gam H2O và a mol CO2. Mặt khác 68,2 gam X tác dụng được tối đa với 0,6 mol NaOH trong dung dịch. Giá trị của a là:
Nhúng một thanh Al nặng 20 gam vào 400 ml dung dịch CuCl2 0,5M. Khi nồng độ dung dịch CuCl2 giảm 25% thì lấy thanh Al ra khỏi dung dịch, giả sử tất cả Cu thoát ra bám vào thanh Al. Khối lượng thanh Al sau phản ứng là
Thực hiện các thí nghiệm sau:
(a) Cho kim loại Cu vào dung dịch Fe2(SO4)3 dư,
(b) Hấp thụ hết 0,15 mol CO2 vào dung dịch chứa 0,2 mol NaOH.
(c) Cho Fe3O4 vào dung dịch H2SO4 đặc, nóng, dư.
(d) Cho dung dịch KOH dư vào dung dịch AlCl3.
(e) Cho NaHCO3 dư vào dung dịch Ba(OH)2.
Sau khi các phản ứng xảy ra hoàn toàn. Số thí nghiệm thu được dung dịch chứa hai muối là
Trung hoà hoàn toàn 8,88 gam một amin (bậc một, mạch cacbon không phân nhánh) bằng axit HCl, tạo ra 17,64 gam muối. Amin có công thức là
Nung m gam bột sắt trong oxi, thu được 4,5 gam hỗn hợp chất rắn X. Hòa tan hết hỗn hợp X trong dung dịch H2SO4 đặc nóng (dư) thoát ra 1,26 lít (đktc) SO2 (là sản phẩm khử duy nhất). Giá trị của m là
Trong các phản ứng của Si với \(C{l_2},{\text{ }}{F_2},{\text{ }}{O_2},{\text{ }}HN{O_3}\) đặc nóng, dung dịch NaOH, Mg. Số phản ứng mà trong đó Si thể hiện tính oxi hóa là
Trong các phản ứng sau, phản ứng nào NH3 không thể hiện tính khử?
Trong khi làm các thí nghiệm ở lớp hoặc trong các giờ thực hành hóa học có một số khí thải: \(C{l_2},{\text{ }}{H_2}S,{\text{ }}S{O_2},{\text{ }}N{O_2},{\text{ }}HCl\). Biện pháp đúng dùng để khử các khí trên là
Cho 2 phản ứng sau:
(1) \(Cu{\text{ }} + {\text{ }}2FeC{l_3}\xrightarrow[{}]{{}}CuC{l_2}{\text{ }} + {\text{ }}2FeC{l_2}\)
(2) \(Fe{\text{ }} + {\text{ }}CuC{l_2}\xrightarrow[{}]{{}}FeC{l_2}{\text{ }} + {\text{ }}Cu\)
Kết luận nào dưới đây là đúng?
Nung nóng m gam bột sắt ngoài không khí, sau phản ứng thu được 36 gam hỗn hợp X gồm \(Fe,{\text{ }}FeO,{\text{ }}F{e_2}{O_3}\) và \(F{e_3}{O_4}\) . Hòa tan hết X trong dung dịch HNO3 loãng thu được 5,6 lít hỗn hợp khí Y gồm NO và H2 có tỉ khối so với là 19. Giá trị m là
Dẫn luồng khí CO qua hỗn hợp \(A{l_2}{O_3},{\text{ }}CuO,{\text{ }}MgO,{\text{ }}F{e_2}{O_3}\) (nóng) sau khi phản ứng xảy ra hoàn toàn thu được chất rắn gồm
Cho các polime sau: Tơ tằm, tơ visco, tơ axetat, tơ nitron, cao su buna-S, poli vinylclorua, poli vinylaxetat, nhựa novolac. Số polime có chứa nguyên tố oxi trong phân tử là
Oxi hoá hết 2,2 gam hỗn hợp hai ancol đơn chức thành anđehit cần vừa đủ 4,8 gam CuO . Cho toàn bộ lượng anđehit trên tác dụng với lượng dư dung dịch AgNO3 trong NH3, thu được 23,76 gam Ag. Hai ancol lần lượt là