Đề thi thử THPT QG môn Hóa học năm 2018 - Trường THPT Chuyên Sơn La
Đề thi thử THPT QG môn Hóa học năm 2018 - Trường THPT Chuyên Sơn La
-
Hocon247
-
40 câu hỏi
-
90 phút
-
31 lượt thi
-
Trung bình
Tham gia [ Hs Hocon247.com ] - Cộng Đồng Luyện Thi Trực Tuyến để được học tập những kiến thức bổ ích từ HocOn247.com
Chất nào sau đây thuộc loại ancol đa chức?
Đáp án A
Ancol đa chức là ancol có 2 nhóm OH trở lên
Criolit dùng trong khi điện phân nóng chảy Al2O3 có công thức là
Criolit dùng trong khi điện phân nóng chảy Al2O3 có công thức là NaAlO2
Đáp án A
Cho Fe dư tác dụng với dung dịch HNO3, sau phản ứng thu được dung dịch có chất tan là
Đáp án A
Fe dư + HNO3 => Chỉ tạo ra được muối sắt(II)
Fe + 4HNO3 → Fe(NO3)3 + NO↑ + 2H2O
Fe + 2Fe(NO3)3 → 3Fe(NO3)2
Muốn điều chế Cu từ dung dịch CuSO4 theo phương pháp thủy luyện người ta dùng kim loại nào sau đây làm chất khử?
Đáp án C
Dùng Fe để điều chế Cu từ CuSO4 theo phương pháp thủy luyện
Fe + CuSO4 → FeSO4 + Cu↓
Để thu được khí CO khô không bị lẫn hơi nước, người ta dẫn khí CO lần lượt qua
Đáp án A
Dùng Ca(OH)2 đặc để hút nước
Trong phân tử cumen có bao nhiêu nguyên tử cacbon?
Đáp án D
CTCT của cumen là C6H5- CH(CH3)- CH3 => Có tất cả 9 nguyên tử C
Công thức của este no đơn chức mạch hở là
Công thức của este no đơn chức mạch hở là CnH2nO2.
Đáp án B
Oxit nào sau đay có tính lưỡng tính?
Đáp án D
CrO3 là oxit axit
MgO, CaO là oxit bazo
Cr2O3 là oxit lưỡng tính
Tơ nào sau đây thuộc loại tơ tổng hợp?
Đáp án D
Tơ visco, tơ xenlulozo axetat: tơ bán tổng hợp
Sợi bông: tơ thiên nhiên
Tơ nilon – 6,6 : tơ tổng hợp.
Khí thải công nghiệp và của các động cơ ô tô, xe máy… là nguyên nhân chủ yếu gây ra mưa axit. Những thành phần hóa học chủ yếu trong các khí thải trực tiếp gây ra mưa axit là
Đáp án B
Đó là các khí NO, NO2, SO2
Natri hiđrocacbonat được dùng làm bột nở trong công nghiệp thực phẩm, dùng chế thuốc chữa đau dạ dày,…Công thức của natri hiđrocacbonat là
Đáp án D
CTHH của Natri hiđrocacbonat : NaHCO3
Chất nào sau đây là chất điện li yếu?
Đáp án D
Ghi nhớ: Chất điện li yếu là các axit yếu, bazo yếu
Cho 0,1 mol O2 tác dụng hết với 14,4 gam kim loại M ( hóa trị không đổi), thu được phần rắn X. Hòa tan toàn bộ X bằng dung dịch HCl, thu được 13,44 lít H2(đktc). M là
4M + xO2 → 2M2Ox
0,4/x 0,1
2M + 2xHCl → 2MClx + xH2
1,2/x 0,6
→ 0,4/x + 1,2/x = 14,4/M → M = 9x (M là Al)
Xà phòng hóa hoàn toàn 16,4 gam hai este đơn chức X, Y ( MX < MY) cần 250 ml dung dịch NaOH 1M. Cô cạn dung dịch sau phản ứng, thu được một muối và hai ancol đồng đẳng liên tiếp. Phần trăm khối lượng của X trong hỗn hợp ban đầu là
X, Y + NaOH → 1 muối + 2 ancol ancol đồng đẳng liên tiếp
→ 2 este ban đầu được tạo từ cùng 1 gốc axit và 2 ancol đồng đẳng liên tiếp
Gọi CT của 2 este là RCOOR’
neste = nNaOH = 0,25 (mol)
→ 2 este phải là HCOOCH3 và HCOOC2H5
Gọi HCOOCH3 : x (mol) ; HCOOC2H5 : y (mol)
Ta có:
x + y = 0,25 và 60x + 74y = 16,4
→ %HCOOCH3 = [(0,15.60) : 16,4].100% = 54,88%
Trong hai chất nào sau đây nguyên tố nitơ đều có cả tính oxi hóa và khử?
Trong NO và NO2 thì nitơ đều có cả tính oxi hóa và khử.
Đáp án C
Cho 6,05 gam hỗn hợp X gồm Fe và Zn phản ứng hoàn toàn với dung dịch HCl loãng 9 (dư), thu được 0,1 mol khí H2 (đktc). Khối lượng Fe trong X là
56nFe + 65nZn = 6,05
nFe + nZn = nH2 = 0,1 mol
→ nFe = nZn = 0,05 mol
→ mFe = 2,8g
Cho dãy các chất: Etilen, stiren, etanol và axit acrylic. Số chất trong dãy có khả năng làm mất màu nước brom là
Đáp án C
Các chất làm mất màu dung dịch nước brom là: etilen( CH2= CH2), stiren( C6H5CH=CH2) , axit acrylic ( CH2=CH-COOH) => có 3 chất
Khi thủy phân tristearin trong môi trường axit, thu được sản phẩm là
Đáp án C
Tristearin có CTCT là: (C17H35COO)3C3H5
(C17H35COO)3C3H5 + 3NaOH → 3C17H35COONa + C3H5(OH)3 (glixerol)
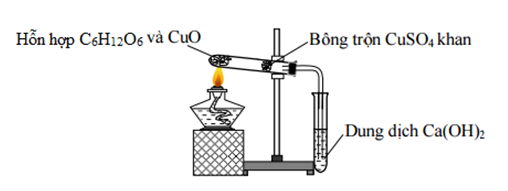
Cho thí nghiệm như hình vẽ:
Thí nghiệm trên dùng để định tính nguyên tố nào có trong hợp chất hữu cơ?
Đáp án B
Từ hình vẽ: Bông trộn CuSO4 khan để nhận biết ra sự có mặt của nước (CuSO4 khan màu trắng sẽ chuyển sang màu xanh) => nhận biết sự có mặt của Hiđro
Dung dịch Ca(OH)2 ( hiện tượng dd Ca(OH)2 trong suốt sẽ vẩn đục ) dùng để nhận biết ra CO2 => nhận biết sự có mặt của Cacbon
Cho 21 gam hỗn hợp gồm glyxin và axit axetic tác dụng vừa đủ với dung dịch KOH, thu được dung dịch X chứa 32,4 gam muối. Cho X tác dụng với dung dịch HCl dư thu được dung dịch chứa m gam muối. Giá trị của m là:
CH2NH2COOH + KOH → CH2NH2COOK + H2O
CH3COOH + KOH → CH3COOK + H2O
Cứ 1 mol hh pư với KOH thì khối lượng muối tăng 39-1 = 38 gam
Vậy số mol hh = (32,4-21)/38 = 0,3 mol
Số mol KOH = 0,3 mol.
Khi HCl pứ với ddX thì xem như HCl pứ KOH và glixin tạo muối.
Đặt x,y là số mol của glixin và ax axetic ta có:
75x + 60y = 21 và x + y = 0,3 được x = 0,2 và y = 0,1
Muối thu được: NH3ClCH2COOH: 0,2 mol và KCl 0,3 mol
Vậy m = 111,5.0,2 + 74,5.0,3 = 44,65 gam
Trong thực tế người ta thường nấu rượu ( ancol etylic) từ gạo ( chứa 81% tinh bột). Tinh bột chuyển hóa thành ancol etylic qua 2 giai đoạn: Tinh bột → glucozơ → ancol. Biết hiệu suất mỗi giai đoạn là 80%, khối lượng riêng của C2H5OH là 0,8 g/ml. Thể tích ancol etylic 460 thu được từ 10 kg gạo là
Để thuận tiện cho tính toán ta bỏ qua hệ số n
mtb = 10.0,81 = 8,1 (kg)
→ ntb = 8,1 : 162 = 0,05 (Kmol)
→ nancol = 2ntb = 0,1 (Kmol)
Vì quá trình sản xuất có hiệu suất
→ nancol thực tế thu được = nancol lí thuyết. %H = 0,1. (0,8. 0,8) = 0,064 (Kmol) = 64 (mol)
→ mancol thực tế = 64. 46 = 2900 (g)
→ V ancol = m : d = 2944 : 0,8 = 3680 ml = 3,68 lít
Độ rượu = (V rượu : V dung dịch rượu).100 = (3,68.100) : 46 = 8 lít
Cho sơ đồ chuyển hóa: C8H15O4N + NaOH dư → X + CH4O + C2H6O.
X + HCl dư → Y + 2NaCl
Nhận định nào sau đây đúng?
Ta có:
H2N – C3H5 (COOCH3) – COOC2H5 + NaOH → H2N – C3H5 (COONa)2 (X) + CH3OH + C2H5OH
H2N – C3H5 (COONa)2 + 3HCl → ClH3N – C3H5 (COOH)2 (Y) + 2NaCl
A đúng vì X làm quỳ đổi màu xanh và Y làm quỳ đỏ
B sai
C sai vì X là muối của aminoaxit
D sai vì X tác dụng với HCl theo tỉ lệ mol là 1 : 1
Đáp án cần chọn là: B
Cho 1,792 lít O2 tác dụng hết với hỗn hợp X gồm Na, K và Ba thu được hỗn hợp rắn Y chỉ gồm các oxit và các kim loại dư. Hòa tan hết toàn bộ Y vào H2O dư, thu được dung dịch Z và 3,136 lít H2. Cho Z tác dụng với lượng dư dung dịch NaHCO3, thu được 39,4 gam kết tủa. Mặt khác, hấp thụ hoàn toàn 10,08 lít CO2 vào dung dịch Z, thu được m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Giá trị của m là
Đáp án B
Bảo toàn electron:
ne kim loại nhường = 4nO2 + 2nH2 = 4. 0,08 + 2.0,14 = 0,6 (mol)
=> dd Z chứa nOH- = 0,6 (mol)
Dd Z tác dụng với NaHCO3 dư => nBa2+ = nBaCO3 = 0,2 (mol)
Dd Z tác dụng với 0,45 mol CO2 => thu được nCO32- = 0,15 ; nHCO3- = 0,3 (mol)
=> mBaCO3 ↓ = 0,15.197 = 29,55 (g) ( Tính theo số mol của CO32-)
Hòa tan Fe3O4 vào dung dịch HCl dư, thu được dung dịch X. Cho dãy các chất: KMnO4; Cl2; KOH; Na2CO3; CuSO4, HNO3; Fe; NaNO3. Số chất trong dãy tác dụng được với dung dịch X là
Đáp án A
Fe3O4 + HCl dư → dd X gồm: FeCl2; FeCl3; HCl dư.
Vậy dd X tác dụng được với các chất là: KMnO4; Cl2; KOH; Na2CO3; HNO3; Fe; NaNO3
5FeCl2 + KMnO4 + 8HCl → 5FeCl3 + KCl + MnO2↓ + Cl2↑ + 4H2O
2FeCl2 + Cl2 → 2FeCl3
FeCl2 + KOH → Fe(OH)2↓ + 2KCl
FeCl3 + KOH → Fe(OH)3↓ + 3KCl
HCl + KOH → KCl + H2O
2FeCl3 + 3Na2CO3 + 3H2O → 2Fe(OH)3↓ + 3CO2↑ + 6NaCl
2HCl + Na2CO3 → 2NaCl + H2O + CO2↑
FeCl2 + 4HNO3 → Fe(NO3)3 + 2HCl + NO2 ↑ + H2O
2FeCl3 + Fe → 3FeCl2
2HCl + Fe → FeCl2 + H2↑
3Fe2+ + NO3- + 4H+ → 3Fe3+ + NO + 2H2O
→ vậy có tất cả 7 chất phản ứng với dd X
Cho các so sánh sau về nhôm và crom ( kí hiệu M chung cho 2 kim loại):
(1) Đều tác dụng với dung dịch HCl và bị oxi hóa lên số oxi hóa +3.
(2) Đều tác dụng được với dung dịch NaOH được NaMO2
(3) Đều bị thụ động trong H2SO4 loãng nguội.
(4) Phèn K2SO4. M2(SO4)3.24H2O đều được dùng làm trong nước đục.
(6) Đều tạo được lớp màng oxit mỏng M2O3 bền vững bảo vệ.
(7) Oxit M2O3 đều tan được trong dung dịch H2SO4 loãng hoặc NaOH loãng.
Đáp án A
1) sai vì Al lên +3 còn Cr lên số oxi hóa +2
2) Sai vì Cr không tác dụng được với dd NaOH
3) Sai vì Al và Cr bị thu động trong H2SO4 đặc nguội.
4) Sai chỉ có phèn nhôm mới được dùng để làm trong nước đục.
6) đúng
7) Sai vì Cr2O3 tan được trong dd axit và kiềm đặc
=> chỉ có 1 phát biểu đúng
Crackinh pentan một thời gian thu được 1,792 lít hỗn hợp X chỉ gồm các hiđrocacbon. Thêm 4,48 lít H2 vào X rồi nung với Ni đến phản ứng hoàn toàn thu được 5,824 lít hỗn hợp khí đều đo ở đktc. Đốt cháy hoàn toàn Y rồ cho sản phẩm cháy hấp thụ vào dung dịch nước vôi trong dư, khối lượng kết tủa tạo thành là
nX = 0,08 mol
nH2 = 2 mol và nY = 0,26 mol
→ nH2 phản ứng = 0,08 + 0,2 – 0,26 = 0,02
→ H2 còn dư và các anken đã phản ứng hết.
→ nAnken trong X = nH2 phản ứng = 0,02
→ nAnkan trong X = 0,08 – 0,02 = 0,06
→ nC5H12 ban đầu = 0,06
Bảo toàn C → nCaCO3 = nC = 0,06.5 = 0,3
→ mCaCO3 = 30 gam
Cho các chất sau: ClH3N- CH2-COOH; H2N- CH( CH3)- CO-NH-CH2-COOH;CH3-NH3NO3; (HOOC- CH2- NH3)2SO4; ClH3N- CH2-CONH-CH2-COOH; CH3-COO-C6H5. Số chất trong dãy khi tác dụng với dung dịch NaOH dư, đun nóng, thu được dung dịch chứa 2 muối là
Đáp án B
ClH3N- CH2-COOH; H2N- CH( CH3)- CO-NH-CH2-COOH; (HOOC- CH2- NH3)2SO4; ClH3N- CH2-CONH-CH2-COOH; CH3-COO-C6H5.
=> có tất cả 5 chất
ClH3N- CH2-COOH + NaOH → NH2- CH2-COONa + NaCl + H2O
H2N- CH( CH3)- CO-NH-CH2-COOH + 2NaOH → H2N- CH(CH3)- COONa + NH2 –CH2-COONa + H2O
(HOOC- CH2- NH3)2SO4 + 4NaOH → 2NH2-CH2-COONa + Na2SO4 + 2H2O
ClH3N- CH2-CONH-CH2-COOH + NaOH → 2NH2-CH2-COONa + NaCl + H2O
CH3-COO-C6H5 + NaOH → CH3-COONa + C6H5ONa + H2O
Kết quả thí nghiệm của các dung dịch X, Y, Z, T với thuốc thử được ghi lại trong bảng sau:
Đáp án C
X là hồ tinh bột
Y là anilin
Z là axit axetic
T là metyl fomat
Đốt cháy hoàn toàn x mol một peptit X mạch hở được tạo thành từ amino axit no A chỉ chứa 1 nhóm –NH2 và một nhóm –COOH thì thu được b mol CO2 và c mol nước. Biết b – c = 3,5x. Số liên kết peptit trong X là
Đáp án A
Gọi X có dạng CnH2n+ 2 - kNkOk-1 : x (mol) - với k là số amino axit ban đầu tạo thành
BTNT C => nCO2 = nC = nx (mol)
BTNT H => nH2O = nH = (n + 1 – 0,5k)x (mol)
Ta có: nCO2 – nH2O = 3,5 x
<=> nx - (n + 1 – 0,5k)x= 3,5x
<=> 0,5k = 4,5
=> k = 9
=> Có 8 liên kết peptit trong X
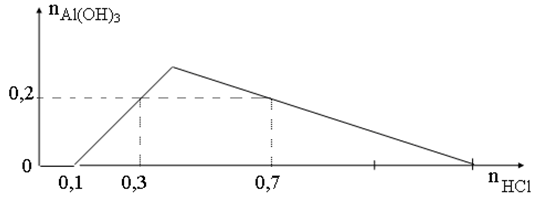
Khi nhỏ từ từ đến dư dung dịch HCl vào dung dịch hỗn hợp gồm a mol Ba(OH)2 và b mol Ba(AlO2)2, kết quả thí nghiệm được biểu diễn trên đồ thị bên.
Tỉ lệ a: b là
Đáp án A
Từ đồ thị ta thấy số mol HCl bắt đầu 0,1 mol mới xuất hiện kết tủa
=> 0,1 mol HCl dùng để trung hòa Ba(OH)2
=> nOH- = nH+ = 0,1 (mol) => nBa(OH)2 = 1/2nOH- = 0,05 (mol) = a
Ta thấy tại giá trị nHCl = 0,3 và 0, 7 mol đều thu được lượng kết tủa như nhau Al(OH)3: 0,2 (mol)
=> Tại nHCl = 0,7 mol thì lượng kết tủa Al(OH) đã đạt cực đại, sau đó bị hòa tan đến khi còn 0, 2 mol
Áp dung công thức nhanh ta có:
nH+ = 4nAlO2 – 3nAl(OH)3 + nOH-
=>0, 7 = 4. 2b – 3. 0,2 + 0,1
=> b = 0,15 (mol)
Vậy a: b = 0,05: 0,15 = 1: 3
Cho các phát biểu sau:
(a) Các oxit của kim loại kiềm thổ đều phản ứng với CO để tạo kim loại.
(b) Các kim loại Ca, Fe, Al và Na chỉ điều chế được bằng phương pháp điện phân nóng chảy.
(c) Các kim loại Mg, K và Fe đều khử được ion Ag+ trong dung dịch thành Ag.
(d) Khi cho Mg vào dung dịch FeCl3 dư không thu được kim loại sắt.
(e) Nhôm là kim loại nhẹ, dẫn điện và dẫn nhiệt tốt, khó kéo dài và dát mỏng.
(g) Hợp kim Na – K dùng làm chất trao đổi nhiệt trong phản ứng hạt nhân.
Số phát biểu sai là
Đáp án D
(a) S. CO chỉ khử được các oxit của kim loại đứng sau Al trong dãy điện hóa.
(b) S. Fe được điều chế bằng phương pháp thủy luyện.
(c) S. Do K phản ứng với H2O nên không khử được Ag+ thành Ag.
(d) Đ
(e) S. Nhôm dễ kéo sợi và dát mỏng.
(g) Đ
Số phát biểu sai là 4
Tiến hành các thí nghiệm sau:
(a) Cho Mg vào dung dịch Fe2(SO4)3 dư
(b) Sục khí Cl2 vào dung dịch FeCl2
(c) Dẫn khí H2 qua bột CuO nung nóng
(d) Cho Na vào dung dịch CuSO4 dư
(e) Đốt FeS2 trong không khí
(g) Điện phân dung dịch NaCl điện cực trơ
Sau khi kết thúc các phản ứng, số thí nghiệm thu được kim loại là
(a) Mg + Fe2(SO4)3 dư → MgSO4 + 2 FeSO4
(b) 2FeCl2 + Cl2 → 2FeCl3
(c) CuO + H2 → Cu + H2O
(d) 2Na + 2H2O → 2NaOH + H2
2NaOH + CuSO4 → Cu(OH)2↓ + Na2SO4
(e) 4FeS2 + 11O2 → 2Fe2O3 + 8SO2
(g) 2NaCl + 2H2O → 2NaOH + H2 + Cl2
Sau khi kết thúc các phản ứng các thí nghiệm thu được kim loại là (c)
Điện phân dung dịch gồm 28,08 gam NaCl và m gam Cu(NO3)2 (điện cực trơ, màng ngăn xốp) đến khi khối lượng dung dịch giảm 51,60 gam thì ngừng điện phân thu được dung dịch X. Cho thanh sắt vào X, sau khi các phản ứng kết thúc thấy khối lượng thanh sắt giảm 6,24 gam và thu được khí NO (sản phẩm khử). Giá trị của m gần nhất với giá trị nào sau đây?
Đáp án B
nNaCl = 0,48 mol
Do khi cho Fe vào dung dịch X thì thấy thoát ra khí NO là sản phẩm khử duy nhất nên H2O đã bị điện phân ở anot.
Catot:
Cu2+ +2e → Cu
x…….2x……x
Anot:
Cl- -1e → 0,5Cl2
0,48…0,48…0,24
2H2O - 4e → O2 + 4H+
4y…..y…..4y
n e trao đổi = 2x = 0,48 + 4y (1)
m dung dịch giảm = mCu + mCl2 + mO2 => 64x + 71.0,24 + 32y = 51,6 (2)
Giải (1) và (2) => x = 0,48; y = 0,12
=> nH+ = 0,48 mol
3Fe + 8H+ + 2NO3- → 3Fe2+ + 2NO + 4H2O
0,18 ← 0,48
Fe + Cu2+ → Fe2+ + Cu
z z z
Khối lượng thanh sắt giảm: (z+0,18).56 – 64z = 6,24 => z = 0,48 mol
=> nCu(NO3)2 ban đầu = x + z = 0,48 + 0,48 = 0,96 mol
=> m = 0,96.188 = 180,48 gam
Cho X, Y là hai axit cacboxylic đều hai chức, mạch hở, kế tiếp nhau trong dãy đồng đẳng; Z, T là hai este hơn kém nhau 14u, Y và Z là đồng phân của nhau (MX < MY < MZ). Đốt cháy 11,52 gam hỗn hợp E gồm X, Y, Z, T (số mol X gấp 2 lần số mol Y) cần dùng 0,32 mol O2. Mặt khác, để tác dụng hết với 11,52 gam hỗn hợp E cần vừa đủ 200 ml dung dịch NaOH 1M thu được mgam hỗn hợp 3 ancol với số mol bằng nhau. (Các phản ứng xảy ra hoàn toàn). Giá trị của m gần nhất với giá trị nào sau đây?
Đáp án C
Y, Z là đồng phân nên X, Y, Z, T đều là các chất 2 chức
nNaOH = 0,2 mol => nE = 0,1 mol => nO = 4nE = 0,4 mol
Đặt mol CO2 và H2O lần lượt là a, b
BTKL: 44a+18b = 11,52 + 0,32.32
BTNT O: 2a + b = 0,32.2 + 0,4
=> a = 0,38; b = 0,28
Ta thấy nE = nCO2 – nH2O => X, Y, Z, T đều là các hợp chất no
Số C trung bình: 0,38 / 0,1 = 3,8
Do MX < MY = MZ < MT, este có ít nhất 4C nên các chất có CTPT là:
X: C3H4O4
Y và Z: C4H6O4
T là: C5H8O4
Do E + NaOH → 3 ancol nên Z cho 1 ancol và T cho 2 ancol
Vậy các este là:
T: CH3OOC-COOC2H5 (y mol)
Z: (HCOO)2C2H4 (y mol)
Các ancol gồm CH3OH (y mol); C2H5OH (y mol); C2H4(OH)2: y mol
Giả sử: E gồm
C3H4O4: 2x
C4H6O4 (axit): x
C4H6O4 (este): y
C5H8O4: y
nE = 2x+x+y+y = 0,1
nC = 3.2x+4x+4y+5y = 0,38
=> x = 0,02; y = 0,02
Vậy m = (32+46+62).0,02 = 2,8 gam
Hòa tan hết 4,667 gam hỗn hợp Na, K, Ba và ZnO (trong đó oxi chiếm 5,14% về khối lượng) vào nước, thu được dung dịch X và 0,032 mol khí H2. Cho 88 ml dung dịch HCl 1M vào X đến khi các phản ứng kết thúc, thu được m gam kết tủa. Giá trị của m là
Đáp án D
mO = 4,667.5,14/100 = 0,24 gam => nO = nZnO = 0,015 mol
Luôn có: nOH- = 2nH2 = 0,064 mol
ZnO + 2OH- → ZnO22- + H2O
0,015→0,03→ 0,015
Vậy dung dịch X gồm: 0,034 mol OH- dư; 0,015 mol ZnO2 2-
Khi cho 0,088 mol HCl vào X:
H+ + OH- → H2O
0,034 ← 0,034
ZnO22- + 2H+ → Zn(OH)2
0,015→ 0,03 → 0,015
2H+ + Zn(OH)2 → Zn2+ + 2H2O
0,088-0,034-0,03→ 0,012
m↓ = (0,015-0,012).99 = 0,297 gam
Đun nóng hỗn hợp E chứa 3 peptit mạch hở (được tạo bởi X, Y là 2 amino axit no, chứa 1 nhóm –NH2 và 1 nhóm –COOH; MX < MY) với dung dịch NaOH vừa đủ thu được dung dịch chỉ chứa 0,24 mol muối của X và 0,32 mol muối của Y. Mặt khác đốt cháy 38,2 gam E cần dùng 1,74 mol O2. Tổng phân tử khối của X và Y là:
Đáp án A
*Xét 0,1 mol hỗn hợp E:
Quy đổi hỗn hợp thành:
CONH: 0,24+0,32 = 0,56 mol
CH2: x
H2O: 0,1
Đốt cháy:
CONH + 0,75O2 → CO2 + 0,5H2O
0,56 →0,42 0,56
CH2 + 1,5O2 → CO2 + H2O
x 1,5x x
Vậy đốt cháy (43.0,56 + 14x + 1,8) gam E cần (1,5x + 0,42) mol O2
38,2 gam 1,74 mol
=> x = 0,88 mol
=> nCO2 (khi đốt 0,1 mol E) = 0,56 + x = 1,44
Giả sử số C trong X và Y là n và m
BTNT C: 0,24n + 0,32m = 1,44 => 6n + 8m = 36
Mà m, n ≥ 2 => 2 ≤ m ≤ 4
+ m = 2 => n = 10/3 (loại)
+ m = 3 => n = 2
+ m = 4 => n = 2/3 (loại)
Vậy X là glyxin và Y là Alanin có tổng phân tử khối là 75 + 89 = 164
Hòa tan hoàn toàn m gam hỗn hợp X gồm Mg, MgO, Fe, FeCO3, Cu(NO3)2 vào dung dịch chứa 4,545 gam KNO3 và a mol H2SO4, thu được dung dịch Y chỉ chứa 63,325 gam muối trung hòa (không có ion Fe3+) và 3,808 lít (đktc) hỗn hợp khí Z (trong đó có 0,02 mol H2). Tỉ khối của Z so với metan bằng 38/17.Thêm dung dịch KOH 1M vào Y đến khi thu được kết tủa lớn nhất là 31,72 gam thì vừa hết 865 ml. Giá trị của m là
mZ = MZ. nZ = 608/17. 0,17 = 6,08 (g)
dd Y + 0,865 mol KOH → sẽ thu được duy nhất muối K2SO4
Bảo toàn nguyên tố K → nK2SO4 = ½( nKNO3 + nKOH ) = 0,91 (mol)
→ nSO42- = nK2SO4 = 0,455 (mol) = a
Ta có hệ 3 phương trình:
Bảo toàn nguyên tố H → nH2O = nH2SO4 – nH2 – 4n(NH4)2SO4 = 0,455 – 0,02 – 4.0,0125 = 0,385 (mol)
Bảo toàn khối lượng : mX + mKNO3 + mH2SO4 = mY + mZ + mH2O
→ mX = mY + mZ + mH2O - mKNO3 - mH2SO4 = 63,325 + 6,08 + 0,385.18 – 4,545 – 0,455.98 = 27,2 (g)
Hỗn hợp X gồm glyxin, alanin, valin, metylamin và etylamin. Đốt cháy hoàn toàn 0,16 mol hỗn hợp X cần dùng vừa đủ 0,57 mol O2. Sản phẩm cháy gồm CO2, H2O và N2 (trong đó số mol CO2 là 0,37 mol). Cho lượng X trên vào dung dịch KOH dư thấy có a mol KOH tham gia phản ứng. Giá trị của a là
Đáp án B
Giả sử X gồm:
CnH2n+1O2N (amino axit): x mol
CmH2m+3N (amin): y mol
Đốt cháy:
CnH2n+1O2N + (1,5n-0,75)O2 → nCO2 + (n+0,5)H2O + 0,5N2
x 1,5nx-0,75x nx
CmH2m+3N + (1,5m+0,75)O2 → mCO2 + (m+1,5) H2O + 0,5N2
y 1,5my+0,75m my
+ nO2 = 1,5nx – 0,75x + 1,5my + 0,75y = 0,57 (1)
+ nX = x + y = 0,16 (2)
+ nCO2 = nx + my = 0,37 (3)
Giải (1)(2)(3) => x = 0,07; y = 0,09
nKOH = n amino axit = 0,07 mol
Hỗn hợp X gồm Cu2O, FeO, M (kim loại M có hóa trị không đổi), trong X số mol của O gấp 2 lần số mol M. Hòa tan 38,55 gam X trong dung dịch HNO3 loãng dư thấy có 1,5 mol HNO3 phản ứng, sau phản ứng thu được 118,35 gam hỗn hợp muối và 2,24 lít NO (đktc). Phần trăm khối lượng của M trong X là
Đáp án D
BTKL: mH2O = mX + mHNO3 – m muối – mNO = 38,55 + 1,5.63 – 118,35 – 0,1.30 = 11,7 gam
=> nH2O = 0,65 mol
BTNT H: nHNO3 = 4nNH4+ + 2nH2O => nNH4+= (1,5-2.0,65)/4 = 0,05 mol
BTNT N: nNO3- muối = nHNO3 – nNH4+ - nNO = 1,5-0,05-0,1 = 1,35 mol
mKL = m muối – mNH4+ - mNO3- = 118,35 – 0,05.18 – 1,35.62 = 33,75 gam
=> mO = 38,55-33,75 = 4,8 gam (0,3 mol)
=> nM = 0,15 mol
Giả sử X gồm: 2x mol Cu; y mol Fe; 0,3 mol O; 0,15 mol M
mKL=64.2x+56y+0,15M=33,75 (1)
BT e: 2.2x+3y+0,15n = 0,3.2+0,1.3+0,05.8 (2)
(1) và (2) => M = 72n - 79
Với n = 2 thì M = 65 (Zn)
%mZn = 0,15.65/38,55 = 25,29%
Thủy phân hoàn toàn hỗn hợp X gồm 2 este mạch hở trong dung dịch NaOH đun nóng, sau phản ứng thu được m gam muối natri axetat và 10,8 gam hỗn hợp Y gồm 2 ancol no, mạch hở có cùng số nguyên tử cacbon. Đốt cháy hoàn toàn 10,8 gam hỗn hợp Y thu được 8,96 lít khí CO2 (đktc) và 10,8 gam H2O. Giá trị của m là
Đáp án A
Do thủy phân X thu được muối natri axetat nên 2 este là este của axit axetic.
nCO2 = 0,4 mol; nH2O = 0,6 mol
=> n ancol = nH2O – nCO2 = 0,2 mol
Số C trong mỗi ancol: 0,4/0,2 = 2
Vậy 2 ancol là: CH3CH2OH (x mol) và C2H4(OH)2 (y mol)
x + y = 0,2
46x + 62y = 10,8
=> x = y = 0,1
Este là: CH3COOC2H5 (0,1 mol) và (CH3COO)2C2H4 (0,1 mol)
=> nCH3COONa = 0,3 mol
m = 0,3.82 = 24,6 gam