Đề thi thử THPT QG môn Hóa học năm 2020 - Trường THPT Chuyên Bắc Ninh
Đề thi thử THPT QG môn Hóa học năm 2020 - Trường THPT Chuyên Bắc Ninh
-
Hocon247
-
40 câu hỏi
-
90 phút
-
63 lượt thi
-
Dễ
Tham gia [ Hs Hocon247.com ] - Cộng Đồng Luyện Thi Trực Tuyến để được học tập những kiến thức bổ ích từ HocOn247.com
Chất hữu cơ nào sau đây trong thành phần có chứa nguyên tố nitơ?
Protein là chất hữu cơ trong thành phần có chứa nguyên tố nitơ.
Chất nào sau đây là chất điện li mạnh?
Chất điện li mạnh là KClO3.
Đáp án A
Axit nào sau đây là axit béo?
Axit linoleic là axit béo.
Đáp án A
Cho 10 gam hỗn hợp gồm KHCO3 và CaCO3 vào dung dịch HCl (dư), thể tích khí (đktc) thu được là
KHCO3 và CaCO3 đều có M = 100g
→ nCO2 = nKHCO3 + nCaCO3 = 0,1mol
→ VCO2 = 2,24 lit
Đáp án C
Để hòa tan hoàn toàn 5,4 gam Al cần dùng vừa đủ Vml dung dịch NaOH 0,5M. Giá trị của V là:
Al + NaOH + H2O → NaAlO2 + 3/2 H2
0,2 0,2
VNaOH = 0,2 : 0,5 = 0,4 lít = 400 mol
Đáp án A
Hợp chất nào sau đây thuộc loại polisaccarit?
Aminozơ thuộc loại polisaccarit
Đáp án B
Trung hòa hoàn toàn 1,8 gam một axit hữu cơ đơn chức X bằng dung dịch NaOH vừa đủ rồi cô cạn dung dịch sau phản ứng được 2,46 gam muối khan. Axit X là:
RCOOH + NaOH → RCOONa + H2O.
1 mol RCOOH → 1 mol RCOONa, m tăng 22 (g).
0,03 mol RCOOH ← m tăng 0,66 (g) (là 2,46 - 1,8).
MRCOOH = R + 45 = 1,8 : 0,03 = 60 → R = 15 → R là CH3-
Axit là CH3COOH.
Chất có thể dùng làm khô NH3 là:
Chất có thể dùng làm khô NH3 là CaO
Trong phòng thí nghiệm axetilen được điều chế từ đất đèn, thành phần chính của đất đèn là:
Thành phần chính của đất đèn là CaC2
Chất nào sau đây không tác dụng với dung dịch NaOH.
Ancol etylic không tác dụng với dung dịch NaOH.
Đáp án D
Quặng nào sau đây chứa oxit sắt:
Quặng Hematit chứa oxit sắt.
Dãy gồm các kim loại bị hòa tan trong dung dịch NaOH là:
Dãy gồm các kim loại bị hòa tan trong dung dịch NaOH là Al, Zn
Lên men một lượng glucozơ, thu được a mol ancol etylic và 0,1 mol CO2. Giá trị của a là
C6H12O6 → 2CO2 + 2C2H5OH
nCO2 = 0,1 mol → nCO2 = nC2H5OH = 0,1 mol
Thủy phân hoàn toàn 8,8 gam este C4H8O2 thu được 6 gam ancol. Tên của este là
Thủy phân hoàn toàn 8,8 gam este C4H8O2 thu được 6 gam ancol. Tên của este là Isopropyl fomat.
Đáp án D
Cho các thí nghiệm sau:
(1). Đun nóng nước cứng vĩnh cửu.
(2). Cho phèn chua vào dung dịch NaOH dư.
(3). Cho dung dịch NaOH dư vào dung dịch CrCl3.
(4). Cho khí CO2 dư vào dung dịch NaAlO2.
(5). Cho khí NH3 dư và dung dịch AlCl3.
(6). Cho CrO3 vào dung dịch Ba(OH)2 dư.
Số thí nghiệm thu được kết tủa là:
Các thí nghiệm tạo kết tủa là (4), (5) và (6)
Đốt cháy hoàn toàn 0,5 mol hỗn hợp anken A và ankin B thu được 44 gam CO2. Tên gọi của A và B lần lượt là:
nCO2 = 1mol ⇒ Số trung bình = 2 anken và ankin đều có 2 nguyên tử C trong phân tử ⇒ C2H4 và C2H2
Cho các phát biểu sau:
1. Sự kết tủa của protein bằng nhiệt được gọi là sự đông tụ.
2. Sợi bông và tơ tằm có thể phân biệt bằng cách đốt chúng.
3. Dùng dung dịch HCl có thể tách riêng benzen ra khỏi hỗn hợp gồm benzen và anilin.
4. Glucozơ có vị ngọt hơn fructozơ.
5. Để nhận biết glucozơ và fructozơ có thể dùng dung dịch AgNO3 trong NH3 đun nóng.
6. Gạo nếp dẻo hơn gạo tẻ do trong gạo nếp chứa nhiều amilopectin hơn.
Số nhận xét đúng là:
Các nhận xét đúng là (1), (2), (3) và (6)
Cho m gam Na vào 200 ml dung dịch hỗn hợp NaOH 1M và Ba(OH)2 0,5M, đến phản ứng hoàn toàn thu được dung dịch X. Cho dung dịch X vào 200 ml dung dịch hỗn hợp Al2(SO4)3 0,5M và HCl 1M, đến phản ứng hoàn toàn thu được 31,1 gam kết tủa. Giá trị lớn nhất của m là:
Ta có: \(31,1\left\{ \begin{array}{l}
BaS{O_4}:0,1\\
Al{(OH)_3}:0,1
\end{array} \right.\) → Na lớn nhất khi kết tủa bị tan một phần.
Dung dịch cuối cùng chứa: \(\left\{ \begin{array}{l}
SO_4^{2 - }:0,2\\
C{l^ - }:0,2\\
AlO_2^ - :0,1\\
N{a^ + }:0,7
\end{array} \right. \to m = 0,5.23 = 11,5(gam)\)
Peptit X có công thức phân tử C6H12O3N2. Số đồng phân peptit của X là:
+ Với peptit ta → Có 1 đồng phân Ala – Ala
+ Với H2N-CH2-COOH và CH3CH2CH(NH2)COOH → Có 2 đồng phân
+ Với H2N-CH2-COOH và CH3(CH3)C(NH2)COOH → Có 2 đồng phân
Khi cho H2SO4 loãng vào dung dịch K2CrO4 sẽ có hiện tượng:
Khi cho H2SO4 loãng vào dung dịch K2CrO4 thì dung dịch từ màu vàng chuyển sang màu da cam.
Thực hiện các thí nghiệm sau:
1. Nhúng thanh Fe nguyên chất vào dung dịch CuSO4.
2. Nhúng thanh Fe nguyên chất vào dung dịch FeCl3.
3. Nhúng thanh Fe nguyên chất vào dung dịch H2SO4 loãng, có nhỏ vài giọt CuSO4.
4. Cho dung dịch Fe(NO3)2 vào dung dịch AgNO3.
5. Để thanh thép ngoài không khí ẩm.
Số trường hợp kim loại bị ăn mòn chủ yếu theo ăn mòn điện hóa là:
Đáp án (1), (3) và (5)
Trong các phản ứng sau phản ứng nào được xem là phương pháp nhiệt luyện dùng để điều chế kim loại.
- Phương pháp nhiệt luyện được ứng dụng rộng rãi trong công nghiệp để điều chế những kim loại có độ hoạt động hóa học trung bình như Zn, Cr, Fe, Sn, Pb…Cơ sở của phương pháp này là khử những ion kim loại trong các hợp chất ở nhiệt độ cao bằng các kim loại mạnh như C, CO, H2 hoặc Al, kim loại kiềm,
kiềm thổ.
Vậy có phản ứng D thỏa mãn
Cho hình vẽ mô tả thí nghiệm điều chế chất lỏng Y từ dung dịch X:
.png)
Trong thí nghiệm trên, xảy ra phản ứng hóa học nào sau đây
Dung dịch X và C6H5NH3Cl là muối nên không thể là chất lỏng Y được → loại B.
Dung dịch X; C2H4 là khí → không phải phản ứng này → loại C.
C2H4 là khí, muốn hóa lỏng phải là nhiệt độ âm → không thể là chất lỏng Y được → loại D.
Loại trừ hoặc biết được A là đúng.!
Cho V lít dung dịch chứa đồng thời Ba(OH)21M và NaOH 0,5M vào 200ml dung dịch H2SO4 1M và HCl 1M. Sau khi các phản ứng xảy ra kết thúc, thu được dung dịch có pH=7. Giá trị V là:
Ta có: \(\left\{ \begin{array}{l}
{n_{O{H^ - }}} = V(2 + 0,5)\\
{n_{{H^ + }}} = 0,2(2 + 1)
\end{array} \right. \to 2,5V = 0,6 \to V = 0,24(lit)\)
Cho hỗn hợp gồm 0,1 mol Zn và 0,2 mol Mg vào 400ml dung dịch chứa đồng thời Cu(NO3)2 1M và AgNO31M. Sau khi phản ứng xảy ra hoàn toàn, thu được chất rắn X. Hòa tan hoàn toàn X trong lượng dư dung dịch HNO3 thu được V lít NO(sản phẩm khử duy nhất của N+5 ,đktc). Giá trị của V là:
\(\begin{array}{l}
{n_{NO_3^ - }} = 1,2(mol)\\
BTDT:\left\{ \begin{array}{l}
M{g^{2 + }}:0,2\\
Z{n^{2 + }}:0,1\\
C{u^{2 + }}:0,3
\end{array} \right. \to X\left\{ \begin{array}{l}
Cu:0,1\\
Ag:0,4
\end{array} \right.
\end{array}\)
\(BTE:{n_{NO}} = \frac{{0,1.2 + 0,4}}{3} = 0,2 \to V = 4,48(lit)\)
Bảng dưới đây ghi lại hiện tượng khi làm thí nghiệm với các chất X, Y, Z, T ở dạng dung dịch với dung môi nước:
X, Y, Z lần lượt là Anilin, glucozơ, glixerol, frutozơ.
Tiến hành các thí nghiệm sau:
(a) Cho Mg vào dung dịch Fe2(SO4)3 dư.
(b) Sục khí H2S vào dung dịch FeCl3.
(c) Cho tính thể NaNO2 vào dung dịch NH4Cl bão hoà rồi đun nóng.
(d) Cho FeS tác dụng với dung dịch HCl.
(e) Đun nóng hỗn hợp gồm NaCl tinh thể và H2SO4 đặc.
Số thí nghiệm không sinh ra đơn chất là
Các thí nghiệm không sinh ra đơn chất là (a), (d) và (e).
Cho dung dịch metylamin dư lần lượt vào từng dung dịch HCl, Na2CO3, NaCl, KOH, dd hỗn hợp chứa HCOOH và KNO2. Số phản ứng xảy ra là:
Metylamin dư lần lượt phản ứng với các dung dịch HCl, dung dịch hỗn hợp chứa HCOOH và KNO2
Nhỏ rất từ từ đến hết 200 ml dung dịch X chứa đồng thời H2SO4 aM và HCl 0,15M vào 100 ml dung dịch chứa đồng thời NaOH 0,5M và Na2CO3 0,4M. Sau khi các phản ứng xảy ra hoàn toàn, thu được 0,448 lít khí (đktc). Giá trị của a là
\(\begin{array}{l}
\left\{ \begin{array}{l}
{n_{{H^ + }}} = 0,2(2a + 0,15)\\
{n_{CO_3^{2 - }}} = 0,04\\
{n_{NaOH}} = 0,05\\
{n_{C{O_2}}} = 0,02
\end{array} \right.\\
BTNT.H:\,\,\,\,\,0,2(2a + 0,15) = 0,05 + 0,04 + 0,02 \to a = 0,2
\end{array}\)
Cho các chất sau :
1) CH3CH(NH2)COOH
2) HOOC–CH2–CH2–NH2
3) HO–CH2–COOH
4) HCHO và C6H5OH
5) HO–CH2–CH2–OH và p-C6H4(COOH)2
6) H2N[CH2]6NH2 và HOOC(CH2)4COOH
Các trường hợp có thể tham gia phản ứng trùng ngưng là :
Các chất có thể tham gia phản ứng trùng ngưng là phân tử phải có ít nhất 2 nhóm chức có khả năng phản ứng
→ các trường hợp là
(1) CH3CH(NH2)COOH
(3) HO–CH2–COOH
(4) HCHO và C6H5OH
(5) HO–CH2–CH2–OH và p-C6H4(COOH)2
(6) H2N[CH2]6NH2 và HOOC(CH2)4COOH
Đáp án cần chọn là A
Cho x mol Mg và 0,1 mol Fe vào 500 ml dung dịch hỗn hợp AgNO3 1M và Cu(NO3)2 1M, đến phản ứng hoàn toàn thu được dung dịch A chứa 4 cation kim loại và chất rắn B. Giá trị x nào sau đây không thỏa mãn?
Dung dịch A chứa 4 ion kim loại → Có hai trường hợp xảy ra
Trường hợp 1: A chứa Mg2+, Fe3+, Cu2+, Ag+ \( \to 2x + 0,1.3 < 0,5 \to x < 0,1\)
Trường hợp 2: A chứa Mg2+, Fe2+, Cu2+, Fe3+ \(BTDT:\,\,\,0,1 < x < 0,15\)
Hiđrat hóa hỗn hợp etilen và propilen có tỉ lệ mol 1:3 khi có mặt axit H2SO4 loãng thu được hỗn hợp ancol X. Lấy m gam hỗn hợp ancol X cho tác dụng hết với Na thấy bay ra 448 ml khí (đktc). Oxi hóa m gam hỗn hợp ancol X bằng O2 không khí ở nhiệt độ cao và có Cu xúc tác được hỗn hợp sản phẩm Y. Cho Y tác dụng với AgNO3 trong NH3 dư thu được 2,808 gam bạc kim loại. Phần trăm số mol ancol propan-1-ol trong hỗn hợp là:
Ta có: \({n_{{H_2}}} = 0,02 \to {n_{ancol}} = 0,04 \to \left\{ \begin{array}{l}
{C_2}{H_5}OH:0,01\\
{C_3}{H_7}OH:0,03
\end{array} \right.\)
Và \({n_{Ag}} = 0,026 \to {n_{CHO}} = 0,013 \to {n_{{C_2}{H_5}CHO}} = 0,003 \to \% {C_2}{H_5}CHO = 7,5\% \)
Hỗn hợp X chứa 3,6 gam Mg và 5,6 gam Fe cho vào 1 lít dung dịch chứa AgNO3 a M và Cu(NO3)2 a M thu được dung dịch A và m gam hỗn hợp chất rắn B. Cho A tác dụng với NaOH dư thu được kết tủa D. Nung D ngoài không khí đến khối lượng không đổi thu được chất rắn E có khối lượng 18 gam. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị m là
Ta có: \(18\left\{ \begin{array}{l}
MgO:0,15\\
F{e_2}{O_3}:0,05\\
CuO:0,05
\end{array} \right. \to A\left\{ \begin{array}{l}
M{g^{2 + }}:0,15\\
F{e^{2 + }}:0,1\\
C{u^{2 + }}:0,05
\end{array} \right. \to NO_3^ - :0,6 \to a = 0,2\)
\( \to m\left\{ \begin{array}{l}
Ag:0,2\\
Cu:0,15
\end{array} \right. \to m = 31,2\)
Tiến hành các thí nghiệm sau:
(a) Cho dung dịch AgNO3 vào dung dịch HCl.
(b) Cho Al2O3 vào dung dịch NaOH loãng dư.
(c) Cho Cu vào dung dịch HCl đặc, nóng dư.
(d) Cho Ba(OH)2 vào dung dịch KHCO3.
(e) Đổ 100 ml dung dịch Ca(OH)2 và 100 ml dung dịch H3PO4 1M.
(f) Sục khí CO2 vào dung dịch thủy tinh lỏng.
(g) Cho catechol vào dung dịch nước Br2.
Sau khi kết thúc các phản ứng, số thí nghiệm thu được chất rắn là
Các thí nghiệm thu được chất rắn là (a), (c), (e), (f) và (g)
Cho từ từ đến dư dung dịch Ba(OH)2 vào dung dịch chứa m gam hỗn hợp Al2(SO4)3 và AlCl3. Sự phụ thuộc của khối lượng kết tủa (y gam) vào số mol Ba(OH)2 (x mol) được biểu diễn bằng đồ thị bên.
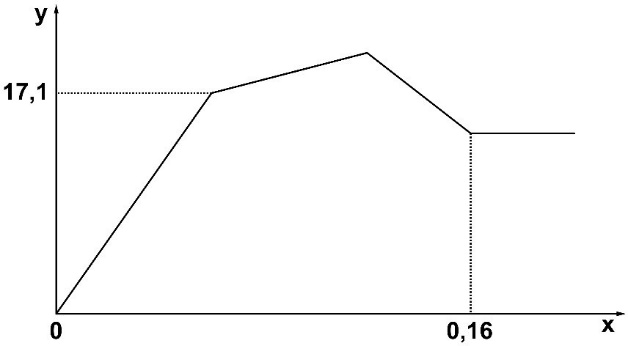
Giá trị của m là
Từ đồ thị có ngay Al2(SO4)3: 0,02
Điền số: \( \to \left\{ \begin{array}{l}
B{a^{2 + }}:0,16\\
SO_4^{2 - }:0,06\\
AlO_2^ - :0,04 + a\\
C{l^ - }:3a
\end{array} \right. \to a = 0,04 \to m = 12,18\)
X,Y là hai hữu cơ axit mạch hở ( MX < MY ). Z là ancol no, T là este hai chức mạch hở không nhánh tạo bởi X, T, Z. Đun 38,86 gam hỗn hợp E chứa X, Y, Z, T với 400ml dung dịch NaOH 1M vừa đủ thu được ancol Z và hỗn hợp F chứa hai muối có số mol bằng nhau. Cho Z vào bình chứa Na dư thấy bình tăng 19,24 gam và thu được 5,824 lít H2 ở đktc. Đốt hoàn toàn hỗn hợp F cần 15,68 lít O2 (đktc) thu được khí CO2, Na2CO3 và 7,2 gam H2O. Phần trăm số mol của T trong E gần nhất với:
Ta có :
F \(\left\{ \begin{array}{l}
{n_{NaOH}} = 0,4 \to \left\{ \begin{array}{l}
n_{COO}^{trong\,E} = 0,4\\
{n_{N{a_2}C{O_3}}} = 0,2
\end{array} \right.\\
{n_{{H_2}}} = 0,26 \to {m_{ancol}} = 19,76 \to {C_3}{H_8}{O_2}
\end{array} \right.\,\,\,\,\)
Đốt cháy \(BTNT.O:\,\,\,0,4.2 + 0,7.2 = 2{n_{C{O_2}}} + 0,2.3 + 0,4 \to {n_{C{O_2}}} = 0,6\)
\(\begin{array}{l}
\to \overline {{C_F}} = 2 \to F\left\{ \begin{array}{l}
HCOONa:0,2\\
C{H_2} = CH - COONa:0,2
\end{array} \right.\\
BTKL:\,{m_F} = 32,4
\end{array}\)
Cho E vào NaOH
\(BTKL:\,\,{n_{{H_2}O}} = {n_{X + Y}} = 0,15 \to {n_X} = {n_Y} = 0,075\)
\( \to {n_T} = 0,125 \to \% {n_T} = \frac{{0,125}}{{0,15 + 0,26}} = 30,49\% \)
Cho các hợp chất sau: FeCl2, FeCl3, FeO, Fe3O4, Fe(NO3)3, Fe(NO3)2, C2H5OH, CH2=CH-COOCH3. Tổng số chất vừa có tính oxi hóa vừa có tính khử là?
Tất cả các chất trên.
Đáp án D
Hòa tan hoàn toàn 12,64 gam hỗn hợp X chứa S, CuS, Cu2S, FeS và FeS2 bằng dung dịch HNO3 (đặc, nóng, vừa đủ). Sau phản ứng thu được dung dịch Y và 25,984 lít hỗn hợp khí Z (đktc) gồm SO2 và NO2 với tổng khối lượng 54,44 gam. Cô cạn Y thu được 25,16 gam hỗn hợp muối. Nếu cho Ba(OH)2 dư vào Y thì khối lượng kết tủa thu được là:
Ta có: \(12,64\left\{ \begin{array}{l}
S:a\\
Cu:b\\
Fe:c
\end{array} \right. \to {n_Z} = 1,16\left\{ \begin{array}{l}
S{O_2}:0,06 \to {n_{SO_4^{2 - }}} = a - 0,06\\
N{O_2}:1,1
\end{array} \right.\)
\( \to \left\{ \begin{array}{l}
32a + 64b + 56c = 12,64\\
0,06.4 + 6(a - 0,06) + 2b + 3c = 1,1
\end{array} \right.\)
\( \to 25,16\left\{ \begin{array}{l}
F{e^{3 + }}:c\\
C{u^{2 + }}:b\\
SO_4^{2 - }:a - 0,06\\
NO_3^ - :3c + 2b - 2a + 0,12
\end{array} \right.\)
\( \to - 28a + 188b + 242c = 23,48 \to \left\{ \begin{array}{l}
a = 0,15\\
b = 0,07\\
c = 0,06
\end{array} \right.\)
\( \to {m_ \downarrow } = 34,25\left\{ \begin{array}{l}
Fe{(OH)_3}:0,06\\
Cu{(OH)_2}:0,07\\
BaS{O_4}:0,09
\end{array} \right.\)
Hỗn hợp E chứa 0,02 mol etylamin; 0,02 mol axit acrylic và 0,03 mol hexapeptit (được tạo bởi Gly, Ala, Val). Đốt cháy toàn bộ E cần dùng vừa đủ a mol O2, cho tất cả sản phẩm cháy hấp thụ vào 700 ml dung dịch NaOH 1M thu được dung dịch Y. Cho rất từ từ 0,4a mol HCl vào Y thấy có 4,8384 lít khí CO2 (đktc) thoát ra. Mặt khác, cho toàn bộ E vào dung dịch NaOH dư thu được m gam muối. Giá trị của m là?
Cộng dồn amin vào axit \( \to 3{n_{C{O_2}}} - 3(0,01 + 0,09) = 2a \to {n_{C{O_2}}} = \frac{2}{3}a + 0,1\)
Điền số
\( \to \left\{ \begin{array}{l}
C{l^ - }:0,4a\\
N{a^ + }:0,7\\
HCO_3^ - :0,7 - 0,4a
\end{array} \right. \to 0,7 - 0,4a + 0,216 = \frac{2}{3}a + 0,1 \to a = 0,765\)
\( \to {n_C} = 0,61 \to m = 0,57.14 + 0,2.69 - 17.0,02 = 21,44\)
Hỗn hợp X gồm Mg, Fe, Fe3O4 và CuO, trong đó oxi chiếm 20% khối lượng. Cho m gam X tan hoàn toàn vào V ml dung dịch Y gồm H2SO4 1,65M và NaNO3 1M, thu được dung dịch Z chỉ chứa 3,66m gam muối trung hòa và 1,792 lít khí NO (đktc). Dung dịch Z phản ứng tối đa với 1,22 mol KOH. Giá trị của V là
Gọi thể tích của Y là V (lít) \( \to \left\{ \begin{array}{l}
{n_{{H_2}S{O_4}}} = 1,65V\\
{n_{NaN{O_3}}} = V
\end{array} \right.\)
Dung dịch sau cùng chứa \(\left\{ \begin{array}{l}
N{a^ + }:V\\
{K^ + }:1,22\\
SO_4^{2 - }:1,65V\\
\to NO_3^ - :1,22 - 2,3V
\end{array} \right. \to {n_{NH_4^ + }} = 3,3V - 1,3\)
Phân chia nhiệm vụ H+ \( \to 3,3V = 0,08.4 + 10(3,3V - 1,3) + \frac{{0,2m}}{{16}}.2\)
Trong Z chứa \(3,66m\left\{ \begin{array}{l}
Mg,Fe,Cu:0,8m\\
SO_4^{2 - }:1,65V\\
N{a^ + }:V\\
NH_4^ + :3,3V - 1,3\\
NO_3^ - :1,22 - 2,3V
\end{array} \right.\)
\(BTKL:3,36m = 0,8m + 96.1,65V + 23V + 18(3,3V - 1,3) + 62(1,22 - 2,3V)\)
\( \to \left\{ \begin{array}{l}
2,86m = 98,2V + 52,24\\
- 29,7V = - 12,68 + 0,025m
\end{array} \right. \to \left\{ \begin{array}{l}
2,86m - 98,2V = 52,24\\
0,025m + 29,7V = 12,68
\end{array} \right. \to \left\{ \begin{array}{l}
m = 32\\
V = 0,4
\end{array} \right.\)

