Đề thi thử tốt nghiệp THPT QG môn Hóa năm 2020 - Sở GD&ĐT Bắc Ninh
Đề thi thử tốt nghiệp THPT QG môn Hóa năm 2020 - Sở GD&ĐT Bắc Ninh
-
Hocon247
-
40 câu hỏi
-
90 phút
-
17 lượt thi
-
Trung bình
Tham gia [ Hs Hocon247.com ] - Cộng Đồng Luyện Thi Trực Tuyến để được học tập những kiến thức bổ ích từ HocOn247.com
Trong công nghiệp, kim loại nào sau đây được điều chế bằng phương pháp điện phân nóng chảy?
Ca được điều chế bằng phương pháp điện phân nóng chảy
Một cốc chứa nước có thành phần ion gồm: Ca2+, Mg2+ , HCO3- , Cl-, SO4-2-. Nước trong cốc thuộc loại nào?
Nước có thành phần ion gồm: Ca2+, Mg2+ , HCO3- , Cl-, SO4-2- là nước cứng có tính cứng toàn phần
Dùng Al dư khử hoàn toàn 4,8 gam Fe2O3 thành Fe bằng phản ứng nhiệt nhôm. Khối lượng Fe thu được là
2Al + Fe2O3 → 2Fe + Al2O3
0,03....... 0,06
mFe = 0,06.56 = 3,36 gam
Chất X ở điều kiện thường là chất khí, không màu, mùi khai, tan tốt trong nước. X là
NH3 ở điều kiện thường là chất khí, không màu, mùi khai, tan tốt trong nước.
Công thức hóa học của sắt (III) nitrat là
sắt (III) nitrat là Fe(NO3)3
Kim loại Fe không phản ứng với chất nào sau đây trong dung dịch?
Kim loại Fe không phản ứng với dung dịch KCl
Chất nào sau đây tác dụng được với dung dịch HCl?
Al(OH)3 là hidroxit lưỡng tính nên tác dụng được với dung dịch NaOH và dung dịch HCl
Các loại dầu ăn như dầu lạc, dầu cọ, dầu vừng, dầu ô-liu,... có thành phần chính là
Các loại dầu ăn như dầu lạc, dầu cọ, dầu vừng, dầu ô-liu,... có thành phần chính là chất béo
Quặng nào sau đây có thành phần chính là Al2O3?
Boxit - Al2O3.nH2O
Cho 500 ml dung dịch glucozơ phản ứng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3, thu được 10,8 gam Ag. Nồng độ của dung dịch glucozơ đã dùng là
Sơ đồ phản ứng: 1 glucozo → 2 Ag
0,05 ......0,1
CM glucozơ = 0,05/0,5 = 0,1 M
Trong tự nhiên, canxi sunfat tồn tại dưới dạng muối ngậm nước (CaSO4.2H2O) được gọi là
thạch cao sống - CaSO4.2H2O
Ở điều kiện thường, chất tồn tại ở trạng thái khí là
etylamin ở điều kiện thường tồn tại ở trạng thái khí
Trong cơ thể người, polisaccarit X bị thủy phân thành monosaccarit Y nhờ các enzim trong nước bọt và ruột non. Phần lớn Y được hấp thụ trực tiếp qua thành ruột vào máu đi nuôi cơ thể, phần còn dư được chuyển về gan. X và Y lần lượt là
X là tinh bột, Y là glucozo
Cho dung dịch anbumin (lòng trắng trứng) tác dụng với Cu(OH)2 trong môi trường kiềm thu được dung dịch có màu
Cho dung dịch anbumin (lòng trắng trứng) tác dụng với Cu(OH)2 trong môi trường kiềm thu được dung dịch có màu tím
Trong các kim loại sau đây, kim loại có tính khử yếu nhất là
kim loại có tính khử yếu nhất là Ag
Chất nào sau đây là chất điện li mạnh?
NaCl là chất điện li mạnh
Kim loại nào sau đây phản ứng được với dung dịch NaOH?
kim loại Al tác dụng được với dung dịch NaOH
Etyl propionat là este có mùi thơm của dứa. Công thức của etyl propionat là
etyl propionat - C2H5COOC2H5
Axit glutamic không phản ứng với dung dịch chất nào
Axit glutamic không phản ứng với dung dịch KCl
Cho vài mẩu canxi cacbua vào ống nghiện đã đựng 1 ml H2O và đậy nhanh ống nghiệm bằng nút có ống dẫn khí, phản ứng sinh ra hiđrocacbon X làm nhạt màu dung dịch brôm. Chất X là
CaC2 + 2H2O → Ca(OH)2 + C2H2
Cho các kim loại sau: Li, Fe, Al, Ca. Kim loại kiềm trong dãy là
Kim loại kiềm - Li, Na, K, Rb, Cs
Trong hợp chất hữu cơ luôn có nguyên tố
trong hợp chất hữu cơ luôn có nguyên tố cacbon
Sắt có số oxi hóa +2 trong hợp chất nào sau đây?
Sắt có số oxi hóa +2 trong hợp chất FeO
Số nguyên tử hiđro trong phân tử fructozơ là
CTPT fructozơ là C6H12O6
Dung dịch nào sau đây làm phenolphtalein đổi màu?
Dung dịch có tính bazơ làm phenolphtalein đổi màu - dung dịch metylamin
Cho 2,4 gam bột Mg tác dụng hoàn toàn với dung dịch CuSO4 dư, thu được m gam Cu. Giá trị của m là
Mg + CuSO4 → MgSO4 + Cu
0,1.....................................0,1
mCu = 0,1.64 = 6,4 gam
Kim loại sắt phản ứng với lượng dư dung dịch chất nào sau đây tạo ra muối sắt (II)?
Fe + H2SO4 loãng → FeSO4 + H2
Cho m gam NH2-CH2-COOH phản ứng hết với dung dịch KOH, thu được dung dịch chứa 13,56 gam muối. Giá trị của m là
H2N-CH2-COOH + KOH → H2N-CH2-COOK + H2O
0,12..........................................0,12
m = 0,12.75 = 9,00
Phát biểu nào sau đây không đúng?
Cao su buna có tính đàn hồi và độ bền thấp hơn cao su thiên nhiên.
Hiđroxit nào sau đây dễ tan trong nước ở điều kiện thường?
KOH dễ tan trong nước ở điều kiện thường
Đun 39,2 gam hỗn hợp M gồm hai este mạch hở X, Y (đều tạo bởi axit cacboxylic và ancol; X, Y hơn kém nhau một nguyên tử cacbon) với dung dịch KOH vừa đủ, thu được một ancol Z duy nhất và hỗn hợp T gồm các muối. Đốt cháy toàn bộ T cần 0,66 mol O2, thu được 0,3 mol K2CO3; 34,12 gam hỗn hợp gồm CO2 và nước. Phần trăm khối lượng của muối có khối lượng phân tử lớn nhất trong hỗn hợp T là
Bảo toàn khối lượng→ mmuối = 54,4
\(% MathType!MTEF!2!1!+- % feaahqart1ev3aqatCvAUfeBSjuyZL2yd9gzLbvyNv2CaerbuLwBLn % hiov2DGi1BTfMBaeXatLxBI9gBaerbd9wDYLwzYbItLDharqqtubsr % 4rNCHbGeaGqiVu0Je9sqqrpepC0xbbL8F4rqqrFfpeea0xe9Lq-Jc9 % vqaqpepm0xbba9pwe9Q8fs0-yqaqpepae9pg0FirpepeKkFr0xfr-x % fr-xb9adbaqaaeaaciGaaiaabeqaamaabaabaaGcbaGaamOBamaaBa % aaleaacaWGlbWaaSbaaWqaaiaaikdaaeqaaSGaam4qaiaad+eadaWg % aaadbaGaaG4maaqabaaaleqaaOGaeyypa0JaaGimaiaacYcacaaIZa % GaeyOKH4QaamOBamaaBaaaleaacaWGlbGaam4taiaadIeaaeqaaOGa % eyypa0JaaGimaiaacYcacaaI2aaaaa!4754! {n_{{K_2}C{O_3}}} = 0,3 \to {n_{KOH}} = 0,6\)
Bảo toàn khối lượng → mZ = 18,4
Z dạng R(OH)r (0,6/r mol)
→ mZ = (R + 17r).0,6/r = 18,4
→R = 41r/3 R = 41 và r = 3 là nghiệm phù hợp
Z là C3H5(OH)3 (0,2 mol)
Đốt T \(% MathType!MTEF!2!1!+- % feaahqart1ev3aqatCvAUfeBSjuyZL2yd9gzLbvyNv2CaerbuLwBLn % hiov2DGi1BTfMBaeXatLxBI9gBaerbd9wDYLwzYbItLDharqqtubsr % 4rNCHbGeaGqiVu0Je9sqqrpepC0xbbL8F4rqqrFfpeea0xe9Lq-Jc9 % vqaqpepm0xbba9pwe9Q8fs0-yqaqpepae9pg0FirpepeKkFr0xfr-x % fr-xb9adbaqaaeaaciGaaiaabeqaamaabaabaaGcbaGaeyOKH4Qaam % OBamaaBaaaleaacaWGdbGaam4tamaaBaaameaacaaIYaaabeaaaSqa % baGccqGH9aqpcaWG1bGaai4oaiaad6gadaWgaaWcbaGaamisamaaBa % aameaacaaIYaaabeaaliaad+eaaeqaaOGaeyypa0JaamODaaaa!4416! \to {n_{C{O_2}}} = u;{n_{{H_2}O}} = v\)
→ 44u + 18v = 34,12
nO(T) = 2nKOH = 1,2
Bảo toàn O: 2u + v + 0,3.3 = 0,66.2 + 1,2
→ u = 0,62 và v = 0,38
Bảo toàn C → nC(M) = 1,52
nM = nZ = 0,2 → Số C = nC(M)/nM = 7,6
→ X là C7HxO6 (0,08) và Y là C8HyO6 (0,12)
mM = 0,08(x + 180) + 0,12(y + 192) = 39,2
→ 2x + 3y = 44
Với và x,y đều chẵn nên x = 10 và y = 8 là nghiệm duy nhất
X là (HCOO)2(CH3COO)C3H5 : 0,08 mol
Y là (HCOO)2(CH≡C-COO)C3H5 : 0,12 mol
→ Muối gồm HCOOK (0,4), CH3COOK (0,08) và CH≡C-COOK (0,12)
→ % CH≡C-COOK = 23,82%
Hỗn hợp E gồm hai este mạch hở X, Y (đều tạo bởi axit cacboxylic và ancol; 74 < MX < MY < 180). Cho m gam E tác dụng vừa đủ với dung dịch NaOH, thu được hỗn hợp 2 muối và 20,2 gam hỗn hợp 2 ancol Z. Cho toàn bộ Z tác dụng với Na dư, thu được 7,28 lít khí H2. Mặt khác, đốt cháy hoàn toàn m gam hỗn hợp E thu được H2O và 57,2 gam CO2. Phần trăm khối lượng của Y trong E là
mCO2 = 57,2 gam → nCO2 = 1,3 mol → nC = 1,3 mol
nH2 = 0,325 mol → nOH/ancol = 2nH2 = 0,65 mol = nNaOH
→ nCOO = nNaOH = 0,65 → nO = 1,3 mo
nC = nO → số C bằng số O trong E
Mặt khác 74 < MX < MY < 180 và sản phẩm thu được 2 muối nên:
X là (COOCH3)2 (x mol) tương ứng với ancol CH3OH 2x mol
Y là (HCOO)3C3H5 ( y mol) tương ứng với ancol C3H5(OH)3 y mol
nOH/ancol = 2x + 3y = 0,65
mZ = 32.2x + 92y = 20,2
→ x = 0,1 và y = 0,15
→ mE = 0,15.176 + 0,1.118 = 38,2 gam
→ %Y = 69,11%
Cho các phát biểu sau:
(a) Nước ép của quả nho chín có khả năng tham gia phản ứng tráng bạc.
(b) Vải làm từ nilon-6,6 bền trong nước xà phòng có tính kiềm.
(c) Xăng sinh học E5 là xăng được pha chế (theo thể tích) từ 95% xăng A92 và 5% etanol
(d) Sử dụng xà phòng để giặt quần áo trong nước cứng sẽ làm vải nhanh mục.
(e) Glucozơ thuộc loại monosaccarit.
Số phát biểu đúng là
(a) đúng, nho chín chứa glucozơ
(b) sai, nilon-6,6 chứa –CONH- nên kém bền trong axit và kiềm
(c) đúng
(d) đúng, do tạo kết tủa (C17H35COO)2Ca bám vào sợ vải
(e) đúng
Hỗn hợp E gồm chất X (CnH2n+4O4N2, là muối amoni của axit cacboxylic đơn chức) và chất Y (CmH2m+3O5N3); X, Y hơn kém nhau một nguyên tử cacbon. Đốt cháy hoàn toàn a mol E cần vừa đủ 47,32 lít O2; thu được H2O; 1,65 mol CO2 và 7,28 lít N2. Mặt khác, cho a mol E tác dụng vừa đủ với dung dịch NaOH, đun nóng, thu được sản phẩm hữu cơ gồm 2 amin và b gam hỗn hợp 2 muối khan có cùng số nguyên tử cacbon trong phân tử (trong đó có một muối của α-aminoaxit). Giá trị của b là
X là CnH2n+4O4N2 (x mol)
Y là CmH2m+3O5N3 (y mol)
\(% MathType!MTEF!2!1!+- % feaahqart1ev3aqatCvAUfeBSjuyZL2yd9gzLbvyNv2CaerbuLwBLn % hiov2DGi1BTfMBaeXatLxBI9gBaerbd9wDYLwzYbItLDharqqtubsr % 4rNCHbGeaGqiVu0Je9sqqrpepC0xbbL8F4rqqrFfpeea0xe9Lq-Jc9 % vqaqpepm0xbba9pwe9Q8fs0-yqaqpepae9pg0FirpepeKkFr0xfr-x % fr-xb9adbaqaaeaaciGaaiaabeqaamaabaabaaGceaqabeaacaWGUb % WaaSbaaSqaaiaadoeacaWGpbWaaSbaaWqaaiaaikdaaeqaaaWcbeaa % kiabg2da9iaad6gadaWgaaWcbaGaamiwaaqabaGccqGHRaWkcaWGUb % WaaSbaaSqaaiaadMfaaeqaaOGaeyypa0JaaGymaiaacYcacaaI2aGa % aGynamaabmaabaGaaiOkaaGaayjkaiaawMcaaaqaaiaad6gadaWgaa % WcbaGaamOtamaaBaaameaacaaIYaaabeaaaSqabaGccqGH9aqpcaWG % 4bGaey4kaSIaaGymaiaacYcacaaI1aGaamyEaiabg2da9iaaicdaca % GGSaGaaG4maiaaikdacaaI1aaabaGaamOBamaaBaaaleaacaWGpbWa % aSbaaWqaaiaaikdaaeqaaaWcbeaakiabg2da9iaadIhadaqadaqaai % aaigdacaGGSaGaaGynaiaad6gacqGHsislcaaIXaaacaGLOaGaayzk % aaGaey4kaSIaamyEamaabmaabaGaaGymaiaacYcacaaI1aGaamyBai % abgkHiTiaaigdacaGGSaGaaG4naiaaiwdaaiaawIcacaGLPaaacqGH % 9aqpcaaIYaGaaiilaiaaigdacaaIXaGaaGOmaiaaiwdaaaaa!6E76! \begin{gathered} {n_{C{O_2}}} = {n_X} + {n_Y} = 1,65\left( * \right) \hfill \\ {n_{{N_2}}} = x + 1,5y = 0,325 \hfill \\ {n_{{O_2}}} = x\left( {1,5n - 1} \right) + y\left( {1,5m - 1,75} \right) = 2,1125 \hfill \\ \end{gathered} \)
→ x = 0,1 và y = 0,15
(*)→ 2n + 3m = 33
Kết hợp n,m kém hơn 1 đơn vị → n = 6 và m = 7
X là muối amoni của axit cacboxylic đơn chức nên X là (CH3COONH3)2C2H4
Hai muối cùng C và có 1 muối của a-amino axit nên Y là CH3COONH3-CH2-CONH-CH2-COONH3-CH3
Muối gồm CH3COONa (2x + y = 0,35) và GlyNa (2y = 0,3)
→ mmuối = 57,80 gam
Cho sơ đồ phản ứng theo đúng tỉ lệ mol:
(a) X + 2NaOH → X1 + X2 + X3. (b) X1 + HCl → X4 + NaCl.
(c) X4 + 2AgNO3 + 4NH3 + H2O → X6 + 2Ag + 2NH4NO3.
(d) X2 + HCl → X5 + NaCl (e) X3 + CO → X5
Biết X có công thức phân tử C6H8O4 và chứa hai chức este. Phát biểu nào sau đây đúng?
(e) → X3 là CH3OH, X5 là CH3COOH
(d) → X2 là CH3COONa
(a) → X là CH3COO-CH=CH-COO-CH3
X1 là OHC-CH2-COONa
(b) → X4 là OHC-CH2-COOH
(c) → X6 là CH2(COONH4)2
Cho các phát biểu sau:
(a) Phương pháp trao đổi ion có thể làm mềm nước có tính cứng vĩnh cửu.
(b) Nhúng thanh sắt vào dung dịch H2SO4 loãng, xảy ra ăn mòn điện hóa học.
(c) Trong công nghiệp, sắt được điều chế bằng phương pháp nhiệt luyện.
(d) Nhôm bị thụ động hóa bởi dung dịch HNO3 đặc, nguội.
(e) Tất cả kim loại kiềm thổ đều tan trong nước ở nhiệt độ thường.
Số phát biểu đúng là
(a) đúng
(b) sai, xảy ra ăn mòn hóa học
(c) đúng
(d) đúng
(e) sai, Be không phản ứng, Mg tan chậm
Đốt cháy hoàn toàn x mol một triglixerit X cần vừa đủ 0,77 mol khí O2 thu được 9,00 gam H2O. Nếu thủy phân hoàn toàn x mol X trong dung dịch KOH đun nóng thu được dung dịch chứa 9,32 gam muối. Mặt khác, hiđro hóa hoàn toàn 0,15 mol X thu được m gam triglixerit Y. Giá trị của m là
Quy đổi x thành (HCOO)3C3H5 (x), CH2 (y) và H2 (z)
\(% MathType!MTEF!2!1!+- % feaahqart1ev3aqatCvAUfeBSjuyZL2yd9gzLbvyNv2CaerbuLwBLn % hiov2DGi1BTfMBaeXatLxBI9gBaerbd9wDYLwzYbItLDharqqtubsr % 4rNCHbGeaGqiVu0Je9sqqrpepC0xbbL8F4rqqrFfpeea0xe9Lq-Jc9 % vqaqpepm0xbba9pwe9Q8fs0-yqaqpepae9pg0FirpepeKkFr0xfr-x % fr-xb9adbaqaaeaaciGaaiaabeqaamaabaabaaGceaqabeaacaWGUb % WaaSbaaSqaaiaad+eadaWgaaadbaGaaGOmaaqabaaaleqaaOGaeyyp % a0JaaGynaiaadIhacqGHRaWkcaaIXaGaaiilaiaaiwdacaWG5bGaey % 4kaSIaaGimaiaacYcacaaI1aGaamOEaiabg2da9iaaicdacaGGSaGa % aG4naiaaiEdaaeaacaWGUbWaaSbaaSqaaiaadIeadaWgaaadbaGaaG % OmaaqabaWccaWGpbaabeaakiabg2da9iaaisdacaWG4bGaey4kaSIa % amyEaiabgUcaRiaadQhacqGH9aqpcaaIWaGaaiilaiaaiwdaaaaa!5521! \begin{gathered} {n_{{O_2}}} = 5x + 1,5y + 0,5z = 0,77 \hfill \\ {n_{{H_2}O}} = 4x + y + z = 0,5 \hfill \\ \end{gathered} \)
Muối gồm HCOOK (3x), CH2 (y) và H2 (z)
mmuối = 84.3x + 14y + 2z = 9,32
→ x = 0,01; y = 0,49 và z = 0,03
→ mY = 176x + 14y = 8,62
Tỉ lệ : 0,01 mol X tạo ra mY = 8,62
→ 0,15 mol X tạo ra mY = 129,3
Hòa tan hoàn toàn 13,8 gam hỗn hợp X gồm Al, Fe vào dung dịch H2SO4 loãng, thu được 10,08 lít khí. Phần trăm về khối lượng của Al trong X là
Đặt x,y là số mol Al, Fe mX = 27x + 56y = 13,8
\(% MathType!MTEF!2!1!+- % feaahqart1ev3aqatCvAUfeBSjuyZL2yd9gzLbvyNv2CaerbuLwBLn % hiov2DGi1BTfMBaeXatLxBI9gBaerbd9wDYLwzYbItLDharqqtubsr % 4rNCHbGeaGqiVu0Je9sqqrpepC0xbbL8F4rqqrFfpeea0xe9Lq-Jc9 % vqaqpepm0xbba9pwe9Q8fs0-yqaqpepae9pg0FirpepeKkFr0xfr-x % fr-xb9adbaqaaeaaciGaaiaabeqaamaabaabaaGcbaGaamOBamaaBa % aaleaacaWGibWaaSbaaWqaaiaaikdaaeqaaaWcbeaakiabg2da9iaa % igdacaGGSaGaaGynaiaadIhacqGHRaWkcaWG5bGaeyypa0JaaGimai % aacYcacaaI0aGaaGynaaaa!42D6! {n_{{H_2}}} = 1,5x + y = 0,45\)
→x = 0,2 và y = 0,15
→%Al = 39,13%
Tiến hành các thí nghiệm theo các bước sau:
Bước 1: Cho vào hai ống nghiệm mỗi ống 2 ml etyl axetat.
Bước 2: Thêm 2 ml dung dịch H2SO4 20% vào ống thứ nhất; 4 ml dung dịch NaOH 30% vào ống thứ hai..
Bước 3: Lắc đều cả hai ống nghiệm, lắp ống sinh hàn, đun sôi nhẹ trong khoảng 5 phút, để nguội.
Cho các phát biểu sau:
(a) Sau bước 2, chất lỏng trong ống thứ nhất phân lớp, chất lỏng trong ống thứ hai đồng nhất.
(b) Sau bước 3, chất lỏng trong cả hai ống nghiệm đều đồng nhất.
(c) Sau bước 3, sản phẩm phản ứng thủy phân trong cả hai ống nghiệm đều tan tốt trong nước.
(d) Ở bước 3, có thể thay việc đun sôi nhẹ bằng đun cách thủy (ngâm trong nước nóng).
(e) Ống sinh hàn có tác dụng hạn chế sự thất thoát của các chất lỏng trong ống nghiệm.
Số phát biểu đúng là
(a) sai, sau bước 2 chưa có phản ứng gì xảy ra (do chưa đun nóng) nên cả 2 ống đều phân lớp
(b) sai, phản ứng thủy phân este trong môi trường axit thuận nghịch nên este luôn dư, không tan nên có phân lớp
(c) đúng, các sản phẩm CH3COONa, CH3COOH, C2H5OH đều tan tốt
(d) đúng
(e) đúng
Dẫn từ từ đến dư khí CO2 vào dung dịch chứa 0,2 mol Ba(OH)2. Sự phụ thuộc của số mol kết tủa (a mol) vào số mol khí CO2 tham gia phản ứng (b mol) được biểu diễn như đồ thị sau
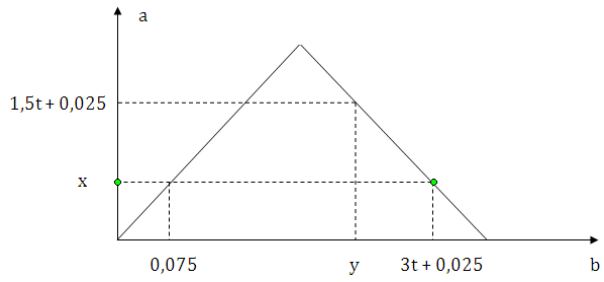
Tỉ lệ y : x là
Đoạn 1: CO2 + Ba(OH)2 → BaCO3 + H2O
→ x = 0,075
Đoạn 2: CO2 + H2O + BaCO3 → Ba(HCO3)2
+ Khi \(% MathType!MTEF!2!1!+- % feaahqart1ev3aqatCvAUfeBSjuyZL2yd9gzLbvyNv2CaerbuLwBLn % hiov2DGi1BTfMBaeXatLxBI9gBaerbd9wDYLwzYbItLDharqqtubsr % 4rNCHbGeaGqiVu0Je9sqqrpepC0xbbL8F4rqqrFfpeea0xe9Lq-Jc9 % vqaqpepm0xbba9pwe9Q8fs0-yqaqpepae9pg0FirpepeKkFr0xfr-x % fr-xb9adbaqaaeaaciGaaiaabeqaamaabaabaaGcbaGaamOBamaaBa % aaleaacaWGdbGaam4tamaaBaaameaacaaIYaaabeaaaSqabaGccqGH % 9aqpcaWG5bGaeyOKH4QaamOBamaaBaaaleaacaWGcbGaamyyaiaado % eacaWGpbWaaSbaaWqaaiaaiodaaeqaaaWcbeaakiabg2da9iaaigda % caGGSaGaaGynaiaadshacqGHRaWkcaaIWaGaaiilaiaaicdacaaIYa % GaaGynaaaa!4BAD! {n_{C{O_2}}} = y \to {n_{BaC{O_3}}} = 1,5t + 0,025\)
\(% MathType!MTEF!2!1!+- % feaahqart1ev3aqatCvAUfeBSjuyZL2yd9gzLbvyNv2CaerbuLwBLn % hiov2DGi1BTfMBaeXatLxBI9gBaerbd9wDYLwzYbItLDharqqtubsr % 4rNCHbGeaGqiVu0Je9sqqrpepC0xbbL8F4rqqrFfpeea0xe9Lq-Jc9 % vqaqpepm0xbba9pwe9Q8fs0-yqaqpepae9pg0FirpepeKkFr0xfr-x % fr-xb9adbaqaaeaaciGaaiaabeqaamaabaabaaGceaqabeaacaWGcb % GaamivaiaabccacaWGcbGaamyyaiabgkziUkaad6gadaWgaaWcbaGa % amOqaiaadggadaqadaqaaiaadIeacaWGdbGaam4tamaaBaaameaaca % aIZaaabeaaaSGaayjkaiaawMcaamaaBaaameaacaaIYaaabeaaaSqa % baGccqGH9aqpcaaIWaGaaiilaiaaigdacaaI3aGaaGynaiabgkHiTi % aaigdacaGGSaGaaGynaiaadshaaeaacaWGcbGaamivaiaabccacaqG % dbGaeyOKH46aaeWaaeaacaaIXaGaaiOlaiaaiwdacaWG0bGaey4kaS % IaaGimaiaacYcacaaIWaGaaGOmaiaaiwdaaiaawIcacaGLPaaacqGH % RaWkcaaIYaWaaeWaaeaacaaIWaGaaiilaiaaigdacaaI3aGaaGynai % abgkHiTiaaigdacaGGSaGaaGynaiaadshaaiaawIcacaGLPaaacqGH % 9aqpcaWG5bWaaeWaaeaacaaIXaaacaGLOaGaayzkaaaaaaa!6A8B! \begin{gathered} BT{\text{ }}Ba \to {n_{Ba{{\left( {HC{O_3}} \right)}_2}}} = 0,175 - 1,5t \hfill \\ BT{\text{ C}} \to \left( {1.5t + 0,025} \right) + 2\left( {0,175 - 1,5t} \right) = y\left( 1 \right) \hfill \\ \end{gathered} \)
+ Khi \(% MathType!MTEF!2!1!+- % feaahqart1ev3aqatCvAUfeBSjuyZL2yd9gzLbvyNv2CaerbuLwBLn % hiov2DGi1BTfMBaeXatLxBI9gBaerbd9wDYLwzYbItLDharqqtubsr % 4rNCHbGeaGqiVu0Je9sqqrpepC0xbbL8F4rqqrFfpeea0xe9Lq-Jc9 % vqaqpepm0xbba9pwe9Q8fs0-yqaqpepae9pg0FirpepeKkFr0xfr-x % fr-xb9adbaqaaeaaciGaaiaabeqaamaabaabaaGcbaGaamOBamaaBa % aaleaacaWGdbGaam4tamaaBaaameaacaaIYaaabeaaaSqabaGccqGH % 9aqpcaaIZaGaamiDaiabgUcaRiaaicdacaGGSaGaaGimaiaaikdaca % aI1aGaeyOKH4QaamOBamaaBaaaleaacaWGcbGaamyyaiaadoeacaWG % pbWaaSbaaWqaaiaaiodaaeqaaaWcbeaakiabg2da9iaaicdacaGGSa % GaaGimaiaaiEdacaaI1aaaaa!4CE6! {n_{C{O_2}}} = 3t + 0,025 \to {n_{BaC{O_3}}} = 0,075\)
\(% MathType!MTEF!2!1!+- % feaahqart1ev3aqatCvAUfeBSjuyZL2yd9gzLbvyNv2CaerbuLwBLn % hiov2DGi1BTfMBaeXatLxBI9gBaerbd9wDYLwzYbItLDharqqtubsr % 4rNCHbGeaGqiVu0Je9sqqrpepC0xbbL8F4rqqrFfpeea0xe9Lq-Jc9 % vqaqpepm0xbba9pwe9Q8fs0-yqaqpepae9pg0FirpepeKkFr0xfr-x % fr-xb9adbaqaaeaaciGaaiaabeqaamaabaabaaGceaqabeaacaWGcb % GaamivaiaabccacaWGcbGaamyyaiabgkziUkaad6gadaWgaaWcbaGa % amOqaiaadggadaqadaqaaiaadIeacaWGdbGaam4tamaaBaaameaaca % aIZaaabeaaaSGaayjkaiaawMcaamaaBaaameaacaaIYaaabeaaaSqa % baGccqGH9aqpcaaIWaGaaiilaiaaigdacaaIYaGaaGynaaqaaiaadk % eacaWGubGaaeiiaiaadoeacqGHsgIRcaaIWaGaaiilaiaaicdacaaI % 3aGaaGynaiabgUcaRiaaikdacaGGUaGaaGimaiaacYcacaaIXaGaaG % OmaiaaiwdacqGH9aqpcaaIZaGaamiDaiabgUcaRiaaicdacaGGSaGa % aGimaiaaikdacaaI1aWaaeWaaeaacaaIYaaacaGLOaGaayzkaaaaaa % a!613B! \begin{gathered} BT{\text{ }}Ba \to {n_{Ba{{\left( {HC{O_3}} \right)}_2}}} = 0,125 \hfill \\ BT{\text{ }}C \to 0,075 + 2.0,125 = 3t + 0,025\left( 2 \right) \hfill \\ \end{gathered} \)
(1)(2) → y = 0,225 và t = 0,1
→ y : x = 3

