Đề thi thử tốt nghiệp THPT QG môn Hóa năm 2020 - Trường THPT Chuyên Lương Văn Chánh Phú Yên lần 1
Đề thi thử tốt nghiệp THPT QG môn Hóa năm 2020 - Trường THPT Chuyên Lương Văn Chánh Phú Yên lần 1
-
Hocon247
-
40 câu hỏi
-
90 phút
-
32 lượt thi
-
Trung bình
Tham gia [ Hs Hocon247.com ] - Cộng Đồng Luyện Thi Trực Tuyến để được học tập những kiến thức bổ ích từ HocOn247.com
Ở điều kiện thường, kim loại nào sau đây không tan được trong dung dịch NaOH?
Fe không tan trong dung dịch NaOH
Sản phẩm của phản ứng nhiệt nhôm luôn có:
Sản phẩm của phản ứng nhiệt nhôm luôn có: Al2O3
Kim loại Fe tác dụng với dung dịch nào sau đây sinh ra khí H2?
Fe + 2HCl → FeCl2 + H2
Dựa trên tiêu chuẩn của Cơ quan Bảo vệ Môi trường Hoa Kỳ, nước bị ô nhiễm chì sẽ có chứa hàm lượng chi vượt mức cho phép là 0,015 mg/lít. Vậy nguồn nước nào dưới đây bị ô nhiễm?
0,02/0,5 = 0,04 > 0,015
Thể tích (ml) dung dịch KOH 0,5M cần dùng để hòa tan hết 5,1 gam bột nhôm oxit là
\(% MathType!MTEF!2!1!+- % feaahqart1ev3aqatCvAUfeBSjuyZL2yd9gzLbvyNv2CaerbuLwBLn % hiov2DGi1BTfMBaeXatLxBI9gBaerbd9wDYLwzYbItLDharqqtubsr % 4rNCHbGeaGqiVu0Je9sqqrpepC0xbbL8F4rqqrFfpeea0xe9Lq-Jc9 % vqaqpepm0xbba9pwe9Q8fs0-yqaqpepae9pg0FirpepeKkFr0xfr-x % fr-xb9adbaqaaeaaciGaaiaabeqaamaabaabaaGceaqabeaacaWGUb % WaaSbaaSqaaiaadgeacaWGSbWaaSbaaWqaaiaaikdaaeqaaSGaam4t % amaaBaaameaacaaIZaaabeaaaSqabaGccqGH9aqpcaaI1aGaaiilai % aaigdacaGGVaGaaGymaiaaicdacaaIYaGaeyypa0JaaGimaiaacYca % caaIWaGaaGynaaqaaiaadgeacaWGSbWaaSbaaSqaaiaaikdaaeqaaO % Gaam4tamaaBaaaleaacaaIZaaabeaakiabgUcaRiaaikdacaWGlbGa % am4taiaadIeacqGHsgIRcaaIYaGaam4saiaadgeacaWGSbGaam4tam % aaBaaaleaacaaIYaaabeaakiabgUcaRiaadIeadaWgaaWcbaGaaGOm % aaqabaGccaWGpbaabaGaaGimaiaacYcacaaIWaGaaGynaiaac6caca % GGUaGaaiOlaiaac6cacaGGUaGaaiOlaiaac6cacaGGUaGaaiOlaiaa % c6cacaGGUaGaaiOlaiaaicdacaGGSaGaaGymaaqaaiabgkziUkaadA % fadaWgaaWcbaGaaeizaiaabsgaaeqaaOGaeyypa0JaaGOmaiaaicda % caaIWaGaamyBaiaadYgaaaaa!6FC4! \begin{gathered} {n_{A{l_2}{O_3}}} = 5,1/102 = 0,05 \hfill \\ A{l_2}{O_3} + 2KOH \to 2KAl{O_2} + {H_2}O \hfill \\ \end{gathered} \)
0,05...........0,1
Vdd = 200 ml
Đun nóng vinyl axetat với một lượng vừa đủ dung dịch NaOH, sản phẩm thu được là
CH3COOCH=CH2 + NaOH → CH3COONa + CH3CH=O.
Kim loại kiềm nào được dùng trong tế bào quang điện?
Cs dùng trong tế bào quang điện
Chất không có khả năng tham gia phản ứng trùng hợp là:
toluen không có khả năng tham gia phản ứng trùng hợp
Cacbohiđrat nào say đây không tham gia phản ứng thủy phân?
fructozo là monosaccarit nên không tham gia phản ứng thủy phân
Chất không tác dụng với dung dịch HCl là:
Na2SO4 không tác dụng với dung dịch HCl
Mô tả nào dưới đây về tính chất vật lý của Al là không đúng?
Cu dẫn điện tốt hơn Al
Chất nào sau đây thuộc loại amin bậc một?
Amin bậc một có dạng RNH2
Kim loại nào sau đây không phải kim loại nhóm IIA?
Li là kim loại kiềm, kim loại nhóm IA
Hoà tan hoàn toàn 28 gam bột Fe vào dung dịch AgNO3 dư thì khối lượng chất rắn thu được là
nFe = 0,5
AgNO3 dư nên sản phẩm là Fe(NO3)3
→ nAg = 3nFe = 1,5 → mAg = 162 gam
Cho 2,52 gam kim loại M hóa trị 2 tác dụng với dung dịch H2SO4 loãng, vừa đủ, sau phản ứng thu được 6,84 gam muối sunfat trung hòa. Kim loại M là
\(% MathType!MTEF!2!1!+- % feaahqart1ev3aqatCvAUfeBSjuyZL2yd9gzLbvyNv2CaerbuLwBLn % hiov2DGi1BTfMBaeXatLxBI9gBaerbd9wDYLwzYbItLDharqqtubsr % 4rNCHbGeaGqiVu0Je9sqqrpepC0xbbL8F4rqqrFfpeea0xe9Lq-Jc9 % vqaqpepm0xbba9pwe9Q8fs0-yqaqpepae9pg0FirpepeKkFr0xfr-x % fr-xb9adbaqaaeaaciGaaiaabeqaamaabaabaaGcbaGaamOBamaaBa % aaleaacaWGtbGaam4tamaaDaaameaacaaI0aaabaGaaGOmaiabgkHi % TaaaaSqabaGccqGH9aqpdaqadaqaaiaaiAdacaGGSaGaaGioaiaais % dacqGHsislcaaIYaGaaiilaiaaiwdacaaIYaaacaGLOaGaayzkaaGa % ai4laiaaiMdacaaI2aGaeyypa0JaaGimaiaacYcacaaIWaGaaGinai % aaiwdaaaa!4B97! {n_{SO_4^{2 - }}} = \left( {6,84 - 2,52} \right)/96 = 0,045\)
Kim loại M có hóa trị x. Bảo toàn electron:
1,52x/M = 0,045.2 → M = 28x
→ x = 2 và M = 56: M là Fe.
Chất béo là trieste của axit béo với
Chất béo là trieste của axit béo với glixerol
Sắt bị ăn mòn điện hóa khi tiếp xúc với kim loại M ngoài không khí ẩm. Kim loại M là
Cặp Fe - Cu thì Fe sẽ bị ăn mòn điện hóa
Ở nhiệt độ thường, không khí oxi hoá được hiđroxit nào sau đây?
Fe(OH)2 bị oxi hóa bởi oxi trong không khí thành Fe(OH)3
Chất lỏng hòa tan được xenlulozơ là
Nước Svayde hòa tan được xenlulozo
Trong các chất dưới đây, chất nào là đipeptit?
H2N-CH2-CO-NH-CH(CH3)-COOH
Hợp chất X có công thức cấu tạo: CH3OOCCH2CH3. Tên gọi của X là
CH3OOCCH2CH3 - Metyl propionat
Hợp chất M2SO4.Al2(SO4)3.24H2O sẽ có tên gọi là phèn chua khi M+ là?
K2SO4.Al2(SO4)3.24H2O - phèn chua
Chất nào sau đây không dẫn điện được?
KCl ở thể rắn không dẫn được điện
Thành phần chính của đá vôi là canxi cacbonat. Công thức của canxi cacbonat là
Công thức của canxi cacbonat là CaCO3
Thí nghiệm nào sau đây không xảy ra sự oxi hóa kim loại.
Fe không tác dụng được với dung dịch Mg(NO3)2
Cho các phát biểu sau:
(1) Kim loại có nhiệt độ nóng chảy thấp nhất là Hg, kim loại dẫn điện tốt nhất là Ag.
(2) Cho Al tan trong dung dịch NaOH thì Al là chất khử còn NaOH là chất oxi hóa.
(3) Natri cacbonat là nguyên liệu quan trọng trong công nghiệp sản xuất thủy tinh.
(4) Nước chứa nhiều ion HCO3- là nước cứng tạm thời.
(5) Trong thiết bị điện phân, ở catot xảy ra quá trình khử.
Số phát biểu đúng là
(1) Đúng
(2) Sai, Al là chất khủ H2O là chất oxi hóa
(3) Đúng
(4) Sai, nước chứa nhiều Ca(HCO3)2, Mg(HCO3)2 là nước cứng tạm thời.
(5) Đúng.
Đốt cháy hoàn toàn 0,1 mol hỗn hợp X gồm metylamin, đimetylamin và trimetylamin cần dùng 0,3 mol O2, thu được CO2, H2O và N2. Nếu lấy 11,4 gam X trên tác dụng với dung dịch HNO3 dư, thu được lượng muối là
X có dạng CnH2n + 3N
\(% MathType!MTEF!2!1!+- % feaahqart1ev3aqatCvAUfeBSjuyZL2yd9gzLbvyNv2CaerbuLwBLn % hiov2DGi1BTfMBaeXatLxBI9gBaerbd9wDYLwzYbItLDharqqtubsr % 4rNCHbGeaGqiVu0Je9sqqrpepC0xbbL8F4rqqrFfpeea0xe9Lq-Jc9 % vqaqpepm0xbba9pwe9Q8fs0-yqaqpepae9pg0FirpepeKkFr0xfr-x % fr-xb9adbaqaaeaaciGaaiaabeqaamaabaabaaGceaqabeaacaWGdb % WaaSbaaSqaaiaad6gaaeqaaOGaamisamaaBaaaleaacaaIYaGaamOB % aiabgUcaRiaaiodaaeqaaOGaamOtaiabgUcaRmaabmaabaGaaGymai % aacYcacaaI1aGaamOBaiabgUcaRiaaicdacaGGSaGaaG4naiaaiwda % aiaawIcacaGLPaaacaWGpbWaaSbaaSqaaiaaikdaaeqaaOGaeyOKH4 % QaamOBaiaadoeacaWGpbWaaSbaaSqaaiaaikdaaeqaaOGaey4kaSYa % aeWaaeaacaWGUbGaey4kaSIaaGymaiaacYcacaaI1aaacaGLOaGaay % zkaaGaamisamaaBaaaleaacaaIYaaabeaakiaad+eacqGHRaWkcaaI % WaGaaiilaiaaiwdacaWGobWaaSbaaSqaaiaaikdaaeqaaaGcbaGaam % OBamaaBaaaleaacaWGybaabeaakiabg2da9iaaicdacaGGSaGaaGym % aiaacUdacaWGUbWaaSbaaSqaaiaad+eadaWgaaadbaGaaGOmaaqaba % aaleqaaOGaeyypa0JaaGimaiaacYcacaaIZaGaeyOKH4QaamOBaiab % g2da9iaaigdacaGGSaGaaGynaaaaaa!6D81! \begin{gathered} {C_n}{H_{2n + 3}}N + \left( {1,5n + 0,75} \right){O_2} \to nC{O_2} + \left( {n + 1,5} \right){H_2}O + 0,5{N_2} \hfill \\ {n_X} = 0,1;{n_{{O_2}}} = 0,3 \to n = 1,5 \hfill \\ \end{gathered} \)
X với HNO3:
\(% MathType!MTEF!2!1!+- % feaahqart1ev3aqatCvAUfeBSjuyZL2yd9gzLbvyNv2CaerbuLwBLn % hiov2DGi1BTfMBaeXatLxBI9gBaerbd9wDYLwzYbItLDharqqtubsr % 4rNCHbGeaGqiVu0Je9sqqrpepC0xbbL8F4rqqrFfpeea0xe9Lq-Jc9 % vqaqpepm0xbba9pwe9Q8fs0-yqaqpepae9pg0FirpepeKkFr0xfr-x % fr-xb9adbaqaaeaaciGaaiaabeqaamaabaabaaGcbaGaamOBamaaBa % aaleaacaWGybaabeaakiabg2da9iaad6gadaWgaaWcbaGaamisaiaa % d6eacaWGpbWaaSbaaWqaaiaaiodaaeqaaaWcbeaakiabg2da9iaaic % dacaGGSaGaaG4maiabgkziUkaad2gadaWgaaWcbaGaamyBaaqabaGc % cqGH9aqpcaWGTbWaaSbaaSqaaiaadIfaaeqaaOGaey4kaSIaamyBam % aaBaaaleaacaWGibGaamOtaiaad+eadaWgaaadbaGaaG4maaqabaaa % leqaaOGaeyypa0JaaG4maiaaicdacaGGSaGaaG4maiaac6caaaa!51DE! {n_X} = {n_{HN{O_3}}} = 0,3 \to {m_m} = {m_X} + {m_{HN{O_3}}} = 30,3.\)
Cho 0,15 mol axit glutamic vào 150 ml dung dịch HCl 2M, thu được dung dịch X. Cho 350 ml dung dịch NaOH 2M vào dung dịch X. Sau khi các phản ứng xảy ra hoàn toàn, cô cạn dung dịch thu được m gam chất rắn khan. Giá trị của m là:
nHCl = 0,3; nNaOH = 0,7
Chất rắn gồm NH2-C3H5(COO-)2 (0,15), Cl- (0,3), Na+ (0,7), bảo toàn điện tích → nOH = 0,1
→ m rắn = 50,2 gam.
Bộ dụng cụ như hình bên mô tả cách tách chất theo phương nào sau đây?
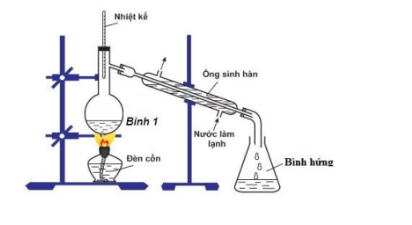
Bộ dụng cụ như hình bên mô tả phương pháp chưng cất.
Hỗn hợp chất lỏng tan vào nhau, có nhiệt độ sôi khác nhau được cho vào bình cầu có nhánh. Nhệt kế giúp a điều chỉnh đèn cồn sao cho chất có nhiệt độ sôi thấp hơn sẽ sôi và bay ra trước. Chất này được ngưng tụ bằng ống sinh hàn rồi chảy vào hình hứng.
Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cho vào ống nghiệm 1-2 giọt dung dịch CuSO4 2% và 1 ml dung dịch NaOH 30%.
Bước 2: Cho tiếp vào ống nghiệm 4 ml dung dịch lòng trắng trứng, lắc nhẹ ống nghiệm. Phát biểu nào sau đây sai?
Bước 1: Điều chế Cu(OH)2
CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4
Bước 2: Phản ứng màu biurê của protein (lòng trắng trứng) với Cu(OH)2, tạo dung dịch màu tím.
Xà phòng hóa hoàn toàn 3,7 gam HCOOC2H5 bằng một lượng dung dịch NaOH vừa đủ. Cô cạn dung dịc sau phản ứng, thu được m gam muối khan. Giá trị của m là
\(% MathType!MTEF!2!1!+- % feaahqart1ev3aqatCvAUfeBSjuyZL2yd9gzLbvyNv2CaerbuLwBLn % hiov2DGi1BTfMBaeXatLxBI9gBaerbd9wDYLwzYbItLDharqqtubsr % 4rNCHbGeaGqiVu0Je9sqqrpepC0xbbL8F4rqqrFfpeea0xe9Lq-Jc9 % vqaqpepm0xbba9pwe9Q8fs0-yqaqpepae9pg0FirpepeKkFr0xfr-x % fr-xb9adbaqaaeaaciGaaiaabeqaamaabaabaaGceaqabeaacaWGUb % WaaSbaaSqaaiaadIeacaWGdbGaam4taiaad+eacaWGobGaamyyaaqa % baGccqGH9aqpcaWGUbWaaSbaaSqaaiaadIeacaWGdbGaam4taiaad+ % eacaWGdbWaaSbaaWqaaiaaikdaaeqaaSGaamisamaaBaaameaacaaI % 1aaabeaaaSqabaGccqGH9aqpcaaIWaGaaiilaiaaicdacaaI1aaaba % GaeyOKH4QaamOBamaaBaaaleaacaWGibGaam4qaiaad+eacaWGpbGa % amOtaiaadggaaeqaaOGaeyypa0JaaG4maiaacYcacaaI0aGaam4zai % aadggacaWGTbaaaaa!56EE! \begin{gathered} {n_{HCOONa}} = {n_{HCOO{C_2}{H_5}}} = 0,05 \hfill \\ \to {n_{HCOONa}} = 3,4gam \hfill \\ \end{gathered} \)
Cho các đặc tính sau:
(1) Dạng tinh thể tan tốt trong nước, có vị ngọt;
(2) Làm mất màu nước brom;
(3) Trong y học, được dùng làm thuốc tăng lực;
(4) Trong công nghiệp, được dùng tráng gương, tráng ruột phích;
(5) Hòa tan được Cu(OH)2 ở điều kiện thường tạo phức xanh lam.
Sổ đặc tính đúng khi nói về glucozơ là.
Tất cả các đặc tính đều đúng.
Cho dãy các chất: C2H2, CH3CHO, CH3COOH, HCOOH, HCOOCH3. Số chất trong dãy tham gia được phản ứng tráng gương là:
Các chất tham gia phản ứng tráng gương: CH3CHO, HCOOH, HCOOCH3.
Cho hơi nước đi qua tan nóng đỏ thu được 78,4 lít hỗn hợp khí X (đo đktc) gồm khí CO, CO2, H2. Oxi hóa hết 1/2 hỗn hợp X bằng CuO dư nung nóng thu được chất rắn Y. Hoà tan hoàn toàn Y trong dung dịch HNO3 loãng thu được 22,4 lít (đo đktc) khí NO (sản phẩm khử duy nhất của N+5). Phần trăm thể tích khí CO trong X là
Đặt a, b, c là số mol CO, CO2, H2 trong mỗi phần.
→ a + b + c = 1,75
Bảo toàn electron:
\(% MathType!MTEF!2!1!+- % feaahqart1ev3aqatCvAUfeBSjuyZL2yd9gzLbvyNv2CaerbuLwBLn % hiov2DGi1BTfMBaeXatLxBI9gBaerbd9wDYLwzYbItLDharqqtubsr % 4rNCHbGeaGqiVu0Je9sqqrpepC0xbbL8F4rqqrFfpeea0xe9Lq-Jc9 % vqaqpepm0xbba9pwe9Q8fs0-yqaqpepae9pg0FirpepeKkFr0xfr-x % fr-xb9adbaqaaeaaciGaaiaabeqaamaabaabaaGceaqabeaacaaIYa % GaamOBamaaBaaaleaacaWGdbGaam4taaqabaGccqGHRaWkcaaI0aGa % amOBamaaBaaaleaacaWGdbGaam4tamaaBaaameaacaaIYaaabeaaaS % qabaGccqGH9aqpcaaIYaGaamOBamaaBaaaleaacaWGibWaaSbaaWqa % aiaaikdaaeqaaaWcbeaakiabgkziUkaaikdacaWGHbGaey4kaSIaaG % inaiaadkgacqGH9aqpcaaIYaGaam4yaaqaaiaaikdacaWGUbWaaSba % aSqaaiaadoeacaWGpbaabeaakiabgUcaRiaaikdacaWGUbWaaSbaaS % qaaiaadIeadaWgaaadbaGaaGOmaaqabaaaleqaaOGaeyypa0JaaG4m % aiaad6gadaWgaaWcbaGaamOtaiaad+eaaeqaaOGaeyOKH4QaaGOmai % aadggacqGHRaWkcaaIYaGaam4yaiabg2da9iaaigdacaGGUaGaaG4m % aaaaaa!6220! \begin{gathered} 2{n_{CO}} + 4{n_{C{O_2}}} = 2{n_{{H_2}}} \to 2a + 4b = 2c \hfill \\ 2{n_{CO}} + 2{n_{{H_2}}} = 3{n_{NO}} \to 2a + 2c = 1.3 \hfill \\ \end{gathered} \)
→ a = 0,5; b = 0,25; c = 1
→ %VCO = 28,57%
Hỗn hợp X chứa ba este đều no, mạch hở gồm một este đơn chức và hai este hai chức, trong mỗi phân tử este chỉ chứa một loại nhóm chức. Đun nóng 0,2 mol X với dung dịch NaOH vừa đủ, thu được muối natri axetat duy nhất và hỗn hợp Y gồm ba ancol, trong đó có hai ancol hơn kém nhau một nguyên tử cacbon. Đốt cháy toàn bộ Y cần dùng 0,545 mol O2, thu được 10,62 gam H2O. Phần trăm khối lượng của este hai chức có khối lượng phân tử lớn trong X là:
\(% MathType!MTEF!2!1!+- % feaahqart1ev3aqatCvAUfeBSjuyZL2yd9gzLbvyNv2CaerbuLwBLn % hiov2DGi1BTfMBaeXatLxBI9gBaerbd9wDYLwzYbItLDharqqtubsr % 4rNCHbGeaGqiVu0Je9sqqrpepC0xbbL8F4rqqrFfpeea0xe9Lq-Jc9 % vqaqpepm0xbba9pwe9Q8fs0-yqaqpepae9pg0FirpepeKkFr0xfr-x % fr-xb9adbaqaaeaaciGaaiaabeqaamaabaabaaGceaqabeaacaWGUb % WaaSbaaSqaaiaadMfaaeqaaOGaeyypa0JaaGimaiaacYcacaaIYaGa % ai4oaiaad6gadaWgaaWcbaGaamisamaaBaaameaacaaIYaaabeaali % aad+eaaeqaaOGaeyypa0JaaGimaiaacYcacaaI1aGaaGyoaaqaaiaa % d6gadaWgaaWcbaGaamywaaqabaGccqGH9aqpcaWGUbWaaSbaaSqaai % aadIeadaWgaaadbaGaaGOmaaqabaWccaWGpbaabeaakiabgkHiTiaa % d6gadaWgaaWcbaGaam4qaiaad+eadaWgaaadbaGaaGOmaaqabaaale % qaaOGaeyOKH4QaamOBamaaBaaaleaacaWGdbGaam4tamaaBaaameaa % caaIYaaabeaaaSqabaGccqGH9aqpcaaIWaGaaiilaiaaiodacaaI5a % aabaGaeyOKH4Qaam4qaiabg2da9iaad6gadaWgaaWcbaGaam4qaiaa % d+eadaWgaaadbaGaaGOmaaqabaaaleqaaOGaai4laiaad6gadaWgaa % WcbaGaamywaaqabaGccqGH9aqpcaaIXaGaaiilaiaaiMdacaaI1aaa % aaa!66C4! \begin{gathered} {n_Y} = 0,2;{n_{{H_2}O}} = 0,59 \hfill \\ {n_Y} = {n_{{H_2}O}} - {n_{C{O_2}}} \to {n_{C{O_2}}} = 0,39 \hfill \\ \to C = {n_{C{O_2}}}/{n_Y} = 1,95 \hfill \\ \end{gathered} \)
→Y chứa CH3OH (a) và CnH2n+2O2 (b)
nY = a + b = 0,2
Bảo toàn O → a + 2b = 0,28
→ a = 0,12 và b = 0,08
\(% MathType!MTEF!2!1!+- % feaahqart1ev3aaatCvAUfeBSjuyZL2yd9gzLbvyNv2CaerbuLwBLn % hiov2DGi1BTfMBaeXatLxBI9gBaerbd9wDYLwzYbItLDharqqtubsr % 4rNCHbGeaGqiVu0Je9sqqrpepC0xbbL8F4rqqrFfpeea0xe9Lq-Jc9 % vqaqpepm0xbba9pwe9Q8fs0-yqaqpepae9pg0FirpepeKkFr0xfr-x % fr-xb9adbaqaaeaaciGaaiaabeqaamaabaabaaGceaqabeaacqGHsg % IRcaWGUbWaaSbaaSqaaiaadoeacaWGpbWaaSbaaWqaaiaaikdaaeqa % aaWcbeaakiabg2da9iaaicdacaGGSaGaaGymaiaaikdacqGHRaWkca % aIWaGaaiilaiaaicdacaaI4aGaamOBaiabg2da9iaaicdacaGGSaGa % aG4maiaaiMdaaeaacqGHsgIRcaWGUbGaeyypa0JaaG4maiaacYcaca % aIZaGaaG4naiaaiwdaaaaa!4FC0! \begin{gathered} \to {n_{C{O_2}}} = 0,12 + 0,08n = 0,39 \hfill \\ \to n = 3,375 \hfill \\ \end{gathered} \)
→ C3H8O2 (0,05) và C4H10O2 (0,03)
X gồm:
CH3COOCH3 (0,12)
(CH3COO)2C3H6 (0,05)
(CH3COO)2C4H8 (0,03) → % = 23,62%
Cho 0,2 mol hỗn hợp E gồm chất X (CnH2n + 4O4N2) và chất Y (CmH2m + 3O2N) đều mạch hở tác dụng vừa đủ với 0,25 mol NaOH, đun nóng, thu được hỗn hợp sản phẩm hữu cơ gồm 21,25 gam hỗn hợp X gồm hai muối và 5,5 gam hỗn hợp hai khí làm quỳ tím ẩm hóa xanh có tỉ khối so với H2 là 13,75. Khối lượng lớn nhất của X có thể đạt được trong 0,2 mol hỗn hợp E gần với giá trị nào nhất?
nE = nX + nY = 0,2
nNaOH = 2nX + nY = 0,25
→ nX = 0,05 và nY = 0,15
M khí = 27,5 → n khí = 0,2
Dễ thấy n khí = nX + nY nên từ X thoát ra 1 khí X’ và từ Y thoát ra 1 khí Y’.
M khí = 0,05X’ + 0,15Y’ = 5,5
→ X’ + 3Y’ = 110
Để mX đạt max thì ta chọn X’ lớn nhất có thể.
→ X’ = 59 (C3H9N) và Y’ = 17 (NH3) là nghiệm phù hợp.
Do sản phẩm chỉ có 2 muối nên:
X là ACOO-NH3-B-COO-NH(CH3)3 (0,05)
Y là ACOO-NH4 (0,15)
Muối gồm ACOONa (0,2) và NH2-B-COONa (0,05)
m muối = 0,2(A + 67) + 0,05(B + 83) = 21,25
→ 4A + B = 74
Để mX đạt max thì ta chọn B lớn nhất có thể → A = 1; B = 70 là nghiệm phù hợp.
X là HCOO-NH3-C5H10-COO-NH(CH3)3 (0,05)
Y là HCOO-NH4 (0,15)
→ mX max = 11,8 gam.
Một bình kín chứa hỗn hợp X gồm 0,06 mol axetilen; 0,09 mol vinyl axetilen; 0,16 mol H2 và một ít bột Ni. Nung hỗn hợp X thu được hỗn hợp Y có tỉ khối hơi đối với H2 là 328/15 trong đó không có but-1-in). Cho toàn bộ hỗn hợp Y đi qua bình đựng dung dịch AgNO3/NH3 dư, thu được m gam kết tủa vàng nhạt và 1,792 lít hỗn hợp khí Z thoát ra khỏi bình. Để làm no hoàn toàn hỗn hợp X cần vừa đúng 50 ml dung dịch Br2 1M. Các phản ứng xảy ra hoàn toàn. Giá trị của m là
Y chứa CH≡CH (a); CH≡C-CH=CH2 (n); CH2=CH2, CH3-CH3, CH2=CH-CH=CH2, CH3-CH2-CH2-CH3
Bảo toàn khối lượng → mY = mX = 6,56
MY = 656/15 → nY = 0,15
→ a + b + 0,08 = 0,15 (1)
\(% MathType!MTEF!2!1!+- % feaahqart1ev3aqatCvAUfeBSjuyZL2yd9gzLbvyNv2CaerbuLwBLn % hiov2DGi1BTfMBaeXatLxBI9gBaerbd9wDYLwzYbItLDharqqtubsr % 4rNCHbGeaGqiVu0Je9sqqrpepC0xbbL8F4rqqrFfpeea0xe9Lq-Jc9 % vqaqpepm0xbba9pwe9Q8fs0-yqaqpepae9pg0FirpepeKkFr0xfr-x % fr-xb9adbaqaaeaaciGaaiaabeqaamaabaabaaGcbaGaamOBamaaBa % aaleaacaWGibWaaSbaaWqaaiaaikdaaeqaaaWcbeaaaaa!38D2! {n_{{H_2}}}\) phản ứng = nX – nY = 0,16
Bảo toàn liên kết pi: 0,06.2 + 0,09.3 = 0,16 + 2a + 3b + 0,05 (2)
(1) (2) → a = 0,03 và b = 0,04
\(% MathType!MTEF!2!1!+- % feaahqart1ev3aqatCvAUfeBSjuyZL2yd9gzLbvyNv2CaerbuLwBLn % hiov2DGi1BTfMBaeXatLxBI9gBaerbd9wDYLwzYbItLDharqqtubsr % 4rNCHbGeaGqiVu0Je9sqqrpepC0xbbL8F4rqqrFfpeea0xe9Lq-Jc9 % vqaqpepm0xbba9pwe9Q8fs0-yqaqpepae9pg0FirpepeKkFr0xfr-x % fr-xb9adbaqaaeaaciGaaiaabeqaamaabaabaaGcbaGaeyOKH4Qaam % yBaiabgoziVkabg2da9iaad2gadaWgaaWcbaGaam4qamaaBaaameaa % caaIYaaabeaaliaadIeadaWgaaadbaGaaGOmaaqabaaaleqaaOGaey % 4kaSIaamyBamaaBaaaleaacaWGdbGaamyqaiaadEgacqGHHjIUcaWG % dbGaeyOeI0Iaam4qaiaadIeacqGH9aqpcaWGdbGaamisamaaBaaame % aacaaIYaaabeaaaSqabaGccqGH9aqpcaaIXaGaaG4maiaacYcacaaI % 1aGaaGOnaaaa!523E! \to m \downarrow = {m_{{C_2}{H_2}}} + {m_{CAg \equiv C - CH = C{H_2}}} = 13,56\)
Hợp chất hữu cơ X mạch hở có công thức phân tử C4H6O4. Biết rằng khi đun X với dung dịch NaOH dư, thu được hai muối và một ancol no, đơn chức, mạch hở. Cho 0,2 mol X tác dụng với 450 ml dung dịch KOH 1M, cô cạn dung dịch sau phản ứng thu được khối lượng chất rắn khan là
X + NaOH dư → 2 muối + Ancol no, đơn chức nên X là HCOO-CH2-COO-CH3
nX = 0,2 và nKOH = 0,45 → Chất rắn gồm HCOOK (0,2), HO-CH2-COOK (0,2), KOH dư (0,05)
→ m rắn = 42,4.
Đốt cháy hoàn toàn m gam hỗn hợp X gồm xenlulozơ và saccarozơ cần dùng 0,96 mol O2, thu được CO2 và H2O. Nếu đun nóng m gam X với dung dịch H2SO4 loãng, dư; thu lấy toàn bộ sản phẩm hữu cơ cho tác dụng với dung dịch AgNO3/NH3 (dùng dư), thu được x gam Ag. Giá trị của x là
X có dạng Cn(H2O)m → \(% MathType!MTEF!2!1!+- % feaahqart1ev3aqatCvAUfeBSjuyZL2yd9gzLbvyNv2CaerbuLwBLn % hiov2DGi1BTfMBaeXatLxBI9gBaerbd9wDYLwzYbItLDharqqtubsr % 4rNCHbGeaGqiVu0Je9sqqrpepC0xbbL8F4rqqrFfpeea0xe9Lq-Jc9 % vqaqpepm0xbba9pwe9Q8fs0-yqaqpepae9pg0FirpepeKkFr0xfr-x % fr-xb9adbaqaaeaaciGaaiaabeqaamaabaabaaGcbaGaamOBamaaBa % aaleaacaWGdbGaam4tamaaBaaameaacaaIYaaabeaaaSqabaGccqGH % 9aqpcaWGUbWaaSbaaSqaaiaad+eadaWgaaadbaGaaGOmaaqabaaale % qaaOGaeyypa0JaaGimaiaacYcacaaI5aGaaGOnaaaa!4195! {n_{C{O_2}}} = {n_{{O_2}}} = 0,96\)
\(% MathType!MTEF!2!1!+- % feaahqart1ev3aqatCvAUfeBSjuyZL2yd9gzLbvyNv2CaerbuLwBLn % hiov2DGi1BTfMBaeXatLxBI9gBaerbd9wDYLwzYbItLDharqqtubsr % 4rNCHbGeaGqiVu0Je9sqqrpepC0xbbL8F4rqqrFfpeea0xe9Lq-Jc9 % vqaqpepm0xbba9pwe9Q8fs0-yqaqpepae9pg0FirpepeKkFr0xfr-x % fr-xb9adbaqaaeaaciGaaiaabeqaamaabaabaaGcbaGaeyOKH4Qaam % OBamaaBaaaleaacaWGdbWaaSbaaWqaaiaaiAdaaeqaaSGaamisamaa % BaaameaacaaIXaGaaGOmaaqabaWccaWGpbWaaSbaaWqaaiaaiAdaae % qaaaWcbeaakiabg2da9iaaicdacaGGSaGaaGyoaiaaiAdacaGGVaGa % aGOnaiabgkHiTiaaicdacaGGSaGaaGymaiaaiAdaaaa!4848! \to {n_{{C_6}{H_{12}}{O_6}}} = 0,96/6 - 0,16\)
→ nAg = 0,32
→ mAg = 34,56

