Đề thi thử THPT QG môn Hóa học năm 2018 - Trường THPT Nguyễn Đình Chiểu - Bến Tre
Đề thi thử THPT QG môn Hóa học năm 2018 - Trường THPT Nguyễn Đình Chiểu - Bến Tre
-
Hocon247
-
40 câu hỏi
-
90 phút
-
20 lượt thi
-
Trung bình
Tham gia [ Hs Hocon247.com ] - Cộng Đồng Luyện Thi Trực Tuyến để được học tập những kiến thức bổ ích từ HocOn247.com
Oxit nào sau đây là oxit axit
CrO, Fe2O3 là oxit bazơ, CrO3 là oxit axit, Al2O3 là oxit lưỡng tính.
Kim loại nào sau đây là kim loại kiềm thổ
CTPT của glucozơ là C6H12O6 có %O =53,33
Phần trăm khối lượng của nguyên tố oxi trong glucozơ là
CTPT của glucozơ là C6H12O6 có %O = 53,33%
Tơ nào sau đây thuộc tơ nhân tạo
Tơ nhân tạo (tơ bán tổng hợp) là tơ có nguồn gốc từ thiên nhiên được pha chế thêm bằng phương pháp hóa học như tơ visco, tơ xenlulozơ axetat …
Nhiệt phân hiđroxit Fe (II) trong không khí đến khi khối lượng không đổi thu được
Phương trình: 4Fe(OH)2 + O2(không khí) → 2Fe2O3 + H2O
Phản ứng nào sau đây là sai
Trong môi trường axit, muối Cr(III) thể hiện tính oxi hóa và dễ bị những chất khử như Zn khử thành muối Cr(II):
Zn + 2CrCl3 → ZnCl2 + 2CrCl2
Dung dịch anilin (C6H5NH2) không phản ứng được với chất nào sau đây
Dung dịch anilin (C6H5NH2) không phản ứng được với NaOH.
Trường hợp nào sau đây tạo sản phẩm là ancol và muối natri của axit cacboxylic
A. HCOOCH=CH-CH3 + NaOH → HCOONa + CH3-CH2-CHO → muối + andehit
B. HCOOCH2CH=CH2 + NaOH → HCOONa + CH2=CH-CH2-OH → muối + ancol
C. HCOOC(CH3)=CH2 + NaOH → HCOONa + CH3COCH3 → muối + xeton
D. CH2=C(CH3)COOH + NaOH → CH2=C(CH3)COONa + H2O → muối + nước
Trong công nghiệp, Al được điều chế bằng cách nào dưới đây
Trong công nghiệp, Al được điều chế bằng cách điện phân nóng chảy Al2O3.
Nhận định nào sau đây là đúng
A. Sai, Nước cứng là nước chứa nhiều ion Ca2+ và Mg2+
B. Sai, Phương pháp đun nóng chỉ có thể làm mềm được nước cứng tạm thời vì trong nước cứng tạm thời có chứa các ion Mg2+, Ca2+ và khi đun nóng:
\(2HCO_3^ - \to CO_3^{2 - } + C{O_2} + {H_2}O\) khi đó \(M{g^{2 + }},C{a^{2 + }} + CO_3^{2 - } \to MgC{O_3},CaC{O_3}$\) (kết tủa)
Lọc bỏ kết tủa ta sẽ thu được nước mềm.
C. Đúng, Trong nước tự nhiên chứa nhiều các ion Ca2+, Mg2+ và , , nên có cả tính cứng tạm thời và tính cứng vĩnh cửu.
Một phân tử xenlulozơ có phân tử khối là 15.106, biết rằng chiều dài mỗi mắc xích C6H10O5 khoảng 5.10-7 (mm). Chiều dài của mạch xenlulozơ này gần đúng là
M mắt xích = M/162 = 92592
chiều dài mắt xích l = n.d = 0,046 mm = 4m5.10-2 (mm)
Đốt cháy 0,01 mol este X đơn chức bằng lượng oxi vừa đủ, thu được 448 ml khí CO2 (đktc). Mặt khác đun nóng 6,0 gam X với dung dịch KOH vừa đủ, thu được lượng muối là:
Ta có: \({C_X} = \frac{{{n_{C{O_2}}}}}{{{n_X}}} = 2:\) X là C2H4O2 có công thức cấu tạo: HCOOCH3
- Khi cho 0,1 mol X tác dụng với KOH thu được muối là HCOOK: 0,1 mol => mmuối = 8,4 gam
Cho 2a mol bột Fe vào dung dịch chứa 5a mol AgNO3, sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch gồm các chất.
Vì \(2{n_{Fe}} < {n_{AgN{O_3}}} < 3{n_{Fe}}\) nên trong dung dịch sau phản ứng chỉ chứa Fe(NO3)2 và Fe(NO3)3.
Điều khẳng định nào sau đây là sai
A. Đúng, Các phản ứng của Al(OH)3: \(\left\{ \begin{array}{l}
Al{(OH)_3} + 3HCl \to AlC{l_3} + 3{H_2}O\\
Al{(OH)_3} + NaOH \to Na[Al{(OH)_4}]
\end{array} \right.\)
B. Đúng, Al là một kim loại có tính khử mạnh, dễ bị nhường e và chuyển thành Al3+.
C. Đúng, Phương trình: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
D. Sai, Chiều giảm dần độ dẫn điện của kim loại: Ag > Cu > Au > Al > Fe.
Hòa tan hết 3,24 gam bột Al trong dung dịch HNO3 dư, thu được 0,02 mol khí X duy nhất và dung dịch Y chứa 27,56 gam muối. Khí X là
\( \to {n_{Al{{(N{O_3})}_3}}} = {n_{Al}} = 0,12\;mol \Rightarrow {n_{N{H_4}N{O_3}}} = \frac{{{m_Y} - 213{n_{Al{{(N{O_3})}_3}}}}}{{80}} = 0,025\,mol\)
Goị a là số e nhận của X áp dụng: \(\to 0,02a = 3{n_{Al}} - 8{n_{N{H_4}N{O_3}}} = 0,16 \to a = 8\). Vậy X là N2O
Xà phòng hóa hoàn toàn triglyxerit X trong dung dịch NaOH dư, thu được glyxerol, natri oleat, natri stearat và natri panmitat. Phân tử khối của X là
X là (C17H33COO)(C17H35COO)(C15H31COO)C3H5
→ MX = 860
Để phân biệt các dung dịch riêng biệt: anilin, glucozơ và alanin, ta dùng dung dịch nào sau đây
Sử dụng dung dịch brom
Anilin: mất màu dung dịch brom có kết tủa trắng
Glucozo: mất màu dung dịch brom
Alanin: không hiện tượng gì
Hỗn hợp X gồm FeCl2 và KCl có tỉ lệ mol tương ứng là 1 : 2. Hòa tan hoàn toàn 16,56 gam X vào nước dư thu được dung dịch Y. Cho dung dịch AgNO3 dư vào Y, kết thúc phản ứng thu được m gam kết tủa. Giá trị m là
nFeCl2 = 0,06 mol và nKCl = 0,12 mol
nAgCl = nCl- = 0,24 mol
nAg = nFe2+ = 0,06 mol
m kết tủa = 40,92 gam
Số đồng phân cấu tạo ứng với amin có công thức phân tử C4H11N là.
|
Đồng phân amin bậc 1 |
n- C4H9NH2, CH3CH(CH3)CH2NH2, CH3CH2CH(CH3)NH2 và (CH3)3CNH2. |
|
Đồng phân amin bậc 2 |
C2H5NHC2H5, n-C3H7NHCH3 và (CH3)2CHNHCH3. |
|
Đồng phân amin bậc 3 |
C2H5NH(CH3)2. |
Vậy amin có CTPT là C4H11N có 8 đồng phân cấu tạo.
Phát biểu nào sau đây là đúng
A. Sai, Xenlulozơ không tan trong nước ngay cả khi đun nóng và không tan trong dung môi hữu cơ như benzene, ete (trong đó có đimetyl ete)….
B. Sai, Saccarozơ không có khả năng tham gia phản ứng tráng gương.
C. Đúng, Glucozơ (C6H12O6) thể hiện tính oxi hóa khi tác dụng với H2 (xt Ni, t0) tạo sorbitol (C6H14O6)
D. Sai, Amilozơ và amilopectin là thành chính của tinh bột có công thức là (C6H10O5)n trong đó phân tử khối của amilopectin lớn hơn so với amilozơ, vì vậy 2 chất trên không phải đồng phân của nhau.
Cho V1 ml dung dịch NaOH 0,4M vào V2 ml dung dịch H2SO4 0,6M. Sau khi kết thúc phản ứng thu được dung dịch chỉ chứa một chất tan duy nhất. Tỉ lệ V1 : V2 là
- Phương trình: \(2NaOH + {H_2}S{O_4} \to N{a_2}S{O_4} + {H_2}O\)
mol: 0,4V1 0,6V2
- Vì sau phản ứng chỉ thu được 1 chất tan nên phản ứng trên vừa đủ \( \Rightarrow \frac{{0,4{V_1}}}{2} = 0,6{V_2} \to \frac{{{V_1}}}{{{V_2}}} = \frac{3}{1}\)
Hòa tan hết m gam hỗn hợp X gồm Cu và Fe trong dung dịch HCl loãng dư, thu được 0,09 mol khí H2. Nếu cho m gam X trên vào dung dịch HNO3 loãng dư, thu được 0,15 mol khí NO (sản phẩm khử duy nhất của N+5). Giá trị của m là
- Khi cho X tác dụng với HCl loãng ta có: \({n_{{H_2}}} = {n_{Fe}} = 0,09\;mol\)
- Khi cho X tác dụng với HNO3 loãng ta có: \(\to {n_{Cu}} = \frac{{3{n_{Fe}} - 3{n_{NO}}}}{2} = 0,09\;mol \Rightarrow {m_X} = 10,8gam\)
Thí nghiệm nào sau đây có phản ứng hóa học xảy ra
A . Fe(NO3)2 + AgNO3 : không phản ứng.
B. Cr2O3 chỉ phản ứng với NaOH đặc nóng.
C. 3Br2 + 2NaCrO2 + 8NaOH → 2Na2CrO4 + 6NaBr + 4H2O
D. Cr, Fe và Al bị thụ động hóa với HNO3 và H2SO4 đặc nguội.
Nhận định nào sau đây là sai
A. Đúng, Ở điều kiện thường, các amino axit là chất rắn, dễ tan trong nước.
B. Đúng, Trong phân tử amino axit, nhóm NH2 và nhóm COOH tương tác với nhau tạo ion lưỡng cực. Vì vậy amino axit kết tinh tồn tại ở dạng ion lưỡng cực. Trong dung dịch, dạng ion lưỡng cực chuyển một phần nhỏ thành dạng phân tử
C. Đúng Axit glutamic là thuốc hổ trợ thần kinh.
D. Sai, Trùng ngưng axit 6-aminohexanoic thu được nilon-6 có chứa liên kết peptit.
Hiđro hóa hoàn toàn a mol chất hữu cơ X mạch hở cần dùng a mol H2 (xúc tác Ni, t0) thu được este Y có công thức phân tử C4H8O2. Số đồng phân thỏa mãn của X là
Phương trình:
C4H6O2 (X) + H2 → C4H8O2 (Y)
a a a
Vậy X là este mạch hở, không no (có một liên kết C = C) và đơn chức. X có 6 đồng phân là:
HCOOCH=CHCH3 (cis – trans), HCOOC(CH3)=CH2, HCOOCH2CH=CH2
CH3COOCH=CH2 và CH2=CHCOOCH3
Cho hỗn hợp gồm Na, Ba và Al vào lượng nước dư, thấy thoát ra V lít khí H2 (đktc); đồng thời thu được dung dịch X và còn lại 1,08 gam rắn không tan. Sục khí CO2 dư vào X, thu được 12,48 gam kết tủa. Giá trị của V là
Chất rắn không tan Y là Al dư
Đặt công thức chung của 3 kim loại Na, K, Ba là M, hóa trị chung là x, có số mol là a (mol)
PTHH: 2M + xH2O → 2M(OH)x + xH2↑ (1)
a → a → 0,5ax (mol)
2Al + 2M(OH)x + xH2O → 2M(AlO2)x + 3H2↑ (2)
a → a → 1,5ax (mol)
Vì Al dư sau phản ứng nên phản ứng (2) M(OH)x phản ứng hết.
Vậy dd X thu được là M(AlO2)x: a(mol). Cho CO2 vào dd X thu được nAl(OH)3 = 12,48:78 = 0,16 (mol)
xCO2 + 2xH2O + M(AlO2)x → xAl(OH)3↓ + M(HCO3)x
a → ax (mol)
Ta có: nAl(OH)3 = ax = 0,16 (mol)
Mà: ∑ nH2 = 0,5ax + 1,5ax = 2ax → nH2 = 2.0,16 = 0,32 (mol)
→ VH2(đktc) = 0,32.22,4 = 7,168 lít.
Cho 15,94 gam hỗn hợp gồm alanin và axit glutamic tác dụng vừa đủ với 200 ml dung dịch NaOH 1M, thu được dung dịch X. Cho 450 ml dung dịch HCl 0,8M vào dung dịch X, cô cạn dung dịch sau phản ứng thu được m gam rắn khan. Giá trị m là
- Ta có: \(\left\{ \begin{array}{l}
89{n_{Ala}} + 147{n_{Glu}} = 15,94\\
{n_{Ala}} + 2{n_{Glu}} = {n_{NaOH}} = 0,2
\end{array} \right. \Rightarrow \left\{ \begin{array}{l}
{n_{Ala}} = 0,08\,mol\\
{n_{Glu}} = 0,06\,mol
\end{array} \right.\)
\( \to {n_{NaCl}} = {n_{NaOH}} = 0,2\;mol \Rightarrow {m_X} = 125,5{n_{AlaHCl}} + 183,5{n_{GluHCl}} + 58,5{n_{NaCl}} = 32,75(gam)\)
Đun nóng 0,2 mol hỗn hợp X chứa etyl fomat và etyl axetat với dung dịch AgNO3/NH3 (dùng dư) thu được 17,28 gam Ag. Nếu thủy phân hoàn toàn 28,84 gam X với dung dịch KOH vừa đủ, thu được m gam muối. Giá trị của m là
nHCOOC2H5 = nAg ÷ 2 = 0,08 mol
⇒ nCH3COOC2H5 = 0,12 mol.
⇒ mX = 0,08.74 + 0,12.88 = 16,48(g)
⇒ TN2 dùng gấp 1,75 lần TN1.
Muối gồm 0,14 mol HCOOK và 0,21 mol CH3COOK.
⇒ m = 0,14.84 + 0,21.98 = 32,34(g)
⇒ chọn D
Thực hiện các phản ứng sau:
(1) Cho Na vào dung dịch CuSO4.
(2) Điện phân dung dịch CuSO4 bằng điện cực trơ.
(3) Thổi luồng khí H2 đến dư qua ống nghiệm chứa CuO.
(4) Nung nóng hỗn hợp gồm Al và CuO trong khítrơ.
(5) Cho bột Fe vào dung dịch CuCl2.
Sau khi kết thúc thí nghiệm, số trường hợp thu được Cu đơn chất là
- Cả 4 trường hợp thu được Cu đơn chất là (2), (3), (4), (5). Các phản ứng xảy ra:
(1) 2Na + CuSO4 + 2H2O → Cu(OH)2 + Na2SO4 + H2
(2) 2CuSO4 + 2H2O → 2Cu + 2H2SO4 + O2
(3) H2 + CuO→ Cu + H2O
(4) 2Al + 3CuO → Al2O3 + 3Cu
(5) Fe + CuCl2 → FeCl2 + Cu
Đốt cháy hoàn toàn 14,24 gam hỗn hợp X chứa 2 este đều no, đơn chức, mạch hở thu được CO2 và H2O có tổng khối lượng là 34,72 gam. Mặt khác đun nóng 14,24 gam X với dung dịch NaOH vừa đủ, thu được hỗn hợp Y chứa 2 ancol kế tiếp và hỗn hợp Z chứa 2 muối của 2 axit cacboxylic kế tiếp, trong đó có a gam muối A và b gam muối B (MA < MB). Tỉ lệ gần nhất của a : b là
- Khi đốt X chứa 2 este no, đơn chức, mạch hở thì ta luôn có: \({n_{C{O_2}}} = {n_{{H_2}O}} = 0,56\;mol\)
nO2 = (mCO2+ mH2O - mX) : 32 = 0,64 mol
→ nX = (2nCO2 + nH2O - 2nO2) : 2 = 0,2 mol
- Ta có: \({C_X} = \frac{{0,56}}{{0,2}} = 2,8\). Vì khi cho X tác dụng với NaOH thu được 2 ancol kế tiếp và 2 muối của 2 axit cacboxylic kế tiếp nên 2 este trong X lần lượt là:
\(\left\{ \begin{array}{l}
HCOOC{H_3}:x\;mol\\
C{H_3}COO{C_2}{H_5}:y\;mol
\end{array} \right. \to \left\{ \begin{array}{l}
x + y = 0,2\\
2x + 4y = 0,56
\end{array} \right. \to \left\{ \begin{array}{l}
x = 0,12\\
y = 0,08
\end{array} \right.\)
Hỗn hợp muối Z gồm HCOONa (A): 0,12 mol và CH3COONa (B): 0,08 mol => a:b = 1,243
Cho hỗn hợp gồm Fe2O3 và Cu vào lượng dư dung dịch H2SO4 loãng thu được dung dịch X và còn lại một phần rắn không tan. Dung dịch X tác dụng được với bao nhiêu chất trong số các chất sau: Fe, NaNO3, Cl2 và KMnO4
- Dung dịch X tác dụng được với 4 chất sau:
\(Fe + CuS{O_4} \to Cu + FeS{O_4}{\rm{ }}\;{\rm{; }}\;{\rm{Fe + }}{{\rm{H}}_2}S{O_4} \to FeS{O_4} + {H_2}\)
\(3F{e^{2 + }} + N{O_3}^ - + 4{H^ + } \to 3F{e^{3 + }} + NO + 2{H_2}O\)
\(6FeS{O_4} + 3C{l_2} \to 2F{e_2}{(S{O_4})_3} + 2FeC{l_3}\)
\(10FeS{O_4} + 2KMn{O_4} + 8{H_2}S{O_4} \to 5F{e_2}{(S{O_4})_3} + {K_2}S{O_4} + 2MnS{O_4} + 8{H_2}O\)
Hỗn hợp X chứa hai hợp chất hữu cơ gồm chất Y (C2H7O2N) và chất Z (C4H12O2N2). Đun nóng 9,42 gam X với dung dịch NaOH dư, thu được hỗn hợp T gồm hai amin kế tiếp có tỉ khối so với He bằng 9,15. Nếu cho 9,42 gam X tác dụng với dung dịch HCl loãng dư, thu được dung dịch có chứa m gam muối của các hợp chất hữu cơ. Giá trị của m là
- Hướng tư duy 1: Tính theo khối lượng của từng muối
\(\left\{ \begin{array}{l}
77{\rm{x}} + 120y = 9,42\\
31{\rm{x}} + 45y = 36,6.(x + y)
\end{array} \right. \to \left\{ \begin{array}{l}
x = 0,06\\
y = 0,04
\end{array} \right.\)
=> m muối = 11,77 (gam)
- Hướng tư duy 2: Bảo toàn khối lượng
+ Ta có: nHCl = x + 2y = 0,14 mol => mmuối = mX + mHCl - mHCOOH = 11,77
Cho 17,82 gam hỗn hợp gồm Na, Na2O, Ba, BaO (trong đó oxi chiếm 12,57% về khối lượng) vào nước dư, thu được a mol khí H2 và dung dịch X. Cho dung dịch CuSO4 dư vào X, thu được 35,54 gam kết tủa. Giá trị của a là.
- Quy đổi hỗn hợp thành Na, Ba và O. Ta có :
\(\left\{ \begin{array}{l}
23{n_{Na}} + 137{n_{Ba}} = 17,82 - 16{n_O}\\
98{n_{Cu{{(OH)}_2}}} + 233{n_{BaS{O_4}}} = 35,54
\end{array} \right. \to \left\{ \begin{array}{l}
23{n_{Na}} + 137{n_{Ba}} = 15,58\\
98\frac{{{n_{N{a^ + }}} + 2{n_{B{a^{2 + }}}}}}{2} + 233{n_{B{a^{2 + }}}} = 35,54
\end{array} \right. \Rightarrow \left\{ \begin{array}{l}
{n_{Na}} = 0,32\,mol\\
{n_{Ba}} = 0,06\,mol
\end{array} \right.\)
\( \to {n_{{H_2}}} = \frac{{{n_{Na}} + 2{n_{Ba}} - 2{n_O}}}{2} = 0,08mol\)
Cho dãy các chất: triolein; saccarozơ; nilon-6,6; tơ lapsan; xenlulozơ và glyxylglyxin. Số chất trong dãy cho được phản ứng thủy phân trong môi trường kiềm là
Có 4 chất thủy phân trong môi trường kiềm là: triolein; nilon-6,6; tơ lapsan; glyxylglyxin.
Thực hiện các thí nghiệm sau
(1) Cho bột Al vào dung dịch NaOH (dư).
(2) Điện phân dung dịch NaCl bằng điện cực trơ, không màng ngănxốp.
(3) Cho dung dịch KI vào dung dịch chứa Na2Cr2O7 và H2SO4.
(4) Dẫn luồng khí NH3 qua ống sứ chứa CrO3.
(5) Cho bột Fe vào lượng dư dung dịch FeCl3.
Số thí nghiệm thu được đơn chất là.
- Có 4 thí nghiệm thu được đơn chất là (1), (2), (3) và (4). Phương trình phản ứng:
(1) 2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
(2) 2NaCl + 2H2O → 2NaOH + Cl2 + H2
(3) 6KI + Na2Cr2O7 + 7H2SO4 → 4K2SO4 + Cr2(SO4)3 + Na2SO4 + 3I2 + 7H2O
(4) 2NH3 + 2CrO3 → N2 + Cr2O3 + 3H2O
Hỗn hợp X chứa các este đều mạch hở gồm hai este đơn chức và một este đa chức, không no chứa một liên kết đôi C=C. Đốt cháy hoàn toàn 0,24 mol X cần dùng 1,04 mol O2, thu được 0,93 mol CO2 và 0,8 mol H2O. Nếu thủy phân X trong NaOH, thu được hỗn hợp Y chứa 2 ancol có cùng số nguyên tử cacbon và hỗn hợp Z chứa 2 muối. Phần trăm khối lượng của este đơn chức có khối lượng phân tử lớn trong X là
- Ta có: \({\overline C _X} = \frac{{0,93}}{{0,24}} = 3,875\). Vì khi thủy phân X trong NaOH thu được 2 ancol có cùng cacbon và 2 muối
=> Trong X có 1 chất là HCOOC2H5 (A), este đơn chức còn lại là RCOOC2H5 (B), este 2 chức (C) được tạo từ etylenglicol C2H4(OH)2 và hai axit cacboxylic HCOOH; RCOOH (trong gốc –R có 1 liên kết đôi C=C)
+ Lúc này kA = 1 ; kB = 2 ; kC = 3. Áp dụng \({n_B} + 2{n_C} = {n_{C{O_2}}} - {n_{{H_2}O}} = 0,13\) (1)
\(\to 2{n_A} + 2{n_B} + 4{n_C} = 2{n_{C{O_2}}} + {n_{{H_2}O}} - 2{n_{{O_2}}} = 0,58\) (2) và nA + nB + nC = 0,24 (3)
+ Từ (1), (2), (3) ta tính được: nA = 0,16 mol ; nB = 0,03 mol ; nC = 0,05 mol
\(\to 3.0,16 + 0,03.{C_B} + 0,05.{C_C} = 0,93\) (4) (với CB > 4, CC > 5)
+ Nếu CB = 5 thay vào (4) ta có: CC = 6 => Thỏa (nếu CB càng tăng thì CC < 6 nên ta không cần xét nữa).
Vậy (B) là CH2=CH-COOC2H5: 0,03 mol => \(\% {m_C} = \frac{{7,25}}{{22,04}} = 13,61\)
Thực hiện sơ đồ phản ứng (đúng với tỉ lệ mol các chất) sau:
(1) X + NaOH → X1 + X2 + 2H2O
(2) X1 + H2SO4 → Na2SO4 + X3
(3) nX2 + nX4 → Nilon-6,6 + 2nH2O
(4) nX3 + nX5 → Tơ lapsan + 2nH2O
Nhận định nào sau đây là sai?
(1) X + 2NaOH → X1 + X2 + H2O
(2) X1 + H2SO4 → X3 + Na2SO4
Từ (1,2) → X là este, X1 là muối natri, X2 là ancol
(3) nX2 + nY → poli(etylen terephtalat) + 2nH2O
[ poli(etylen terephtalat) là (-O-CH2-CH2-O-CO-[CH2]4-CO-)n ]
→ X2: HOCH2CH2OH; Y: HOOC-[CH2]4-COOH
(4) nX3 + nZ → tơ nilon-6,6 + 2nH2O
[ nilon-6,6 là (-NH-[CH2]6-NH-CO-[CH2]4-CO-)n ]
→ X3: HOOC-[CH2]4-COOH; Z: H2N-[CH2]6-NH2
→ X1 là NaOOC-[CH2]4-COONa
Mà 1 mol X tác dụng với 2 mol NaOH sinh ra 1 mol X1, 1 mol X2 và 1 mol H2O
→ X là HOOC-[CH2]4COOCH2CH2OH có CTPT là C8H14O5
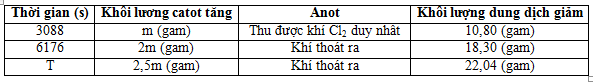
Tiến hành điện phân dung dịch CuSO4 và NaCl bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện không đổi, ta có kết quả ghi theo bảng sau:
Giá trị của t là :
- Gọi a là số mol của NaCl. Quá trình điện phân xảy ra như sau:
|
Thời gian (s) |
Tại catot |
Tại anot |
|
t = 3088 ne = 2x |
Cu2+ + 2e → Cu x 2x x |
2Cl- → 2e + Cl2 2x 2x x |
|
t = 6176 ne = 4x = 0,32 |
Cu2+ + 2e → Cu 0,16 0,32 0,16
|
2Cl- → 2e + Cl2 a → 0,5a 2H2O → 4e + 4H+ + O2 0,32 - a → 0,08 - 0,25a |
|
t = ? |
Cu2+ + 2e → Cu 0,2 0,4 0,2 2H2O + 2e → 2OH- + H2 2y y |
2Cl- → 2e + Cl2 0,2 0,2 0,1 2H2O → 4e + 4H+ + O2 2a (0,4 + 2y) - 0,2 → 0,5y + 0,05 |
- Tại thời điểm t = 3088 có: \({m_{dd{\rm{ giam}}}} = 64{n_{Cu}} + 71{n_{C{l_2}}} \Rightarrow 135x = 10,8 \Rightarrow x = 0,06\;mol\)
- Tại thời điểm t = 6176 (s) có: \({m_{dd{\rm{ giam}}}} = 64{n_{Cu}} + 71{n_{C{l_2}}} + 32{n_{{O_2}}} = 18,3 \Rightarrow a = 0,2\;mol\)
- Tại thời điểm t (s) có:\({m_{dd{\rm{ giam}}}} = 64{n_{Cu}} + 71{n_{C{l_2}}} + 32{n_{{O_2}}} + 2{n_{{H_2}}} = 22,04 \Rightarrow y = 0,03\;mol\)
\(\Rightarrow {n_{e{\rm{(trao doi)}}}} = 2{n_{Cu}} + 2{n_{{H_2}}} = 2.0,2 + 2.0,03 = 0,46\;mol \Rightarrow t = \frac{{0,46}}{{0,16}}.3088 = 8878s\)
Hỗn hợp E chứa ba peptit đều mạch hở gồm peptit X (C4H8O3N2), peptit Y (C7HxOyNz) và peptit Z (C11HnOmNt). Đun nóng 28,42 gam E với dung dịch NaOH vừa đủ, thu được hỗn hợp T gồm 3 muối của glyxin, alanin và valin. Đốt cháy toàn bộ T cần dùng 1,155 mol O2, thu được CO2, H2O, N2 và 23,32 gam Na2CO3. Phần trăm khối lượng của X trong hỗn hợp E là
\({n_{AlaNa,\,GlyNa,\,ValNa}} = 2{n_{N{a_2}C{O_3}}} = 0,44\;mol\)
mà \({n_{Ala,\,Gly,Val}} = \frac{4}{3}(1,5{n_{C{O_2}}} - {n_{{O_2}}}) \Rightarrow {n_{C{O_2}}} = 0,99\;mol\)
- Quy đổi hỗn hợp E thành C2H3ON, CH2 và H2O. Lập hệ sau:
\(\left\{ \begin{array}{l}
57{n_{{C_2}{H_3}ON}} + 14{n_{C{H_2}}} + 18{n_{{H_2}O}} = 28,42\\
\to 2{n_{{C_2}{H_3}ON}} + {n_{C{H_2}}} = {n_{C{O_2}}} = 0,99\\
2,25{n_{{C_2}{H_3}ON}} + 1,5{n_{C{H_2}}} = {n_{{O_2}}} = 1,155
\end{array} \right. \to \left\{ \begin{array}{l}
{n_{{C_2}{H_3}ON}} = 0,44\\
{n_{C{H_2}}} = 3{n_{Val}} + {n_{Ala}} = 0,11\\
{n_{{H_2}O}} = {n_X} + {n_Y} + {n_Z} = 0,1
\end{array} \right. \Rightarrow \)
\({\bar n_{{\rm{mat x}}i{\rm{ch}}}} = \frac{{{n_{Gly,\,Ala,Val}}}}{{{n_X} + {n_Y} + {n_Z}}} = 4,4\)
=> Trong E có chứa peptit có số mắc xích lớn 4,4 (5, 6 hoặc 7…). Vậy Z là pentapeptit (Gly)4Ala, X là đipeptit (Gly)2 và Y là đipeptit AlaVal (không thể là tripeptit (Gly)2Ala vì khi đó thủy phân hỗn hợp E sẽ không thu được muối của Val).
\(\left\{ \begin{array}{l}
\to 4{n_X} + 7{n_Y} + 11{n_Z} = {n_{C{O_2}}} = 0,99\\
2{n_X} + 2{n_Y} + 5{n_Z} = 2{n_{NaOH}} = 0,44\\
132{n_X} + 174{n_Y} + 317{n_Z} = 28,42
\end{array} \right. \to \left\{ \begin{array}{l}
{n_X} = 0,01\\
{n_Y} = 0,01\\
{n_Z} = 0,08
\end{array} \right.\,\,\, \Rightarrow \% {m_X} = \frac{{0,01.132}}{{28,42}}.100\% = 4,64\)
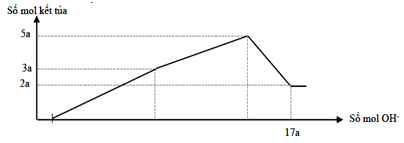
Hòa tan hết 12,06 gam hỗn hợp gồm Mg và Al2O3 trong dung dịch chứa HCl 0,5M và H2SO4 0,1M. Sau khi kết thúc phản ứng thu được dung dịch X. Cho từ từ dung dịch NaOH 1M vào dung dịch X, phản ứng được biểu diễn theo đồ thị sau:
Nếu cho từ từ V ml dung dịch NaOH 0,3M và Ba(OH)2 0,1M vào dung dịch X, thu được kết tủa lớn nhất, lấy kết tủa nung ngoài không khí đến khối lượng không đổi thu được m gam rắn khan. Giá trị của m là
Dd X + NaOH → Mg(OH)2 + Al(OH)3
Lượng kết tủa khi NaOH dư là nMg(OH)2 = 2a
→ lượng kết tủa tối đa là nAl(OH)3 = n↓ - nMg(OH)2 = 5a - 2a =3a
→ nMg : nAl2O3 = 2a : = 4 : 3
Mà mhỗn hợp = 24nMg + 102nAl2O3 = 12,06 → nMg = 0,12 mol và nAl2O3 = 0,09 mol
→ a = 0,06 mol → nOH = 17a = 1,02 = nH+ (X) + 2nMg + 8nAl2O3 = nH+(X) + 0,96 → nH+(X) = 0,06 mol
Bảo toàn điện tích trong dung dịch X có nH+(X) + 2nMg2+ + 3nAl3+ = nCl- + 2nSO4 = 0,84
Mà nCl : nSO4 = 5 : 1 nên nCl- = 0,6 mol và nSO4 = 0,12 mol
X có Cl- : 0,6 mol SO42- : 0,12 mol, H+ : 0,06 mol, Al3+ : 0,18 mol và Mg2+ : 012 mol
Dd thêm vào có Ba2+ : x mol, Na+ : 3x mol ; OH- : 5x mol
Để thu được kết tủa tối đa thì ta có tạo kết tủa Al(OH)3 và Mg(OH)2 tối đa
nOH- = 5x = 0,18.3 +0,12.2 =0,78 mol
Khi đó Ba2+ : 0,156 → nBaSO4= 0,12 → ↓ BaSO4 : 0,12 mol; Al(OH)3 : 0,18 mol; Mg(OH)2 : 0,12 mol
→ nung thu được 0,12 mol BaSO4; 0,09 mol Al2O3 và 0,12 mol MgO
→ m =41,94