Đề thi thử THPT QG môn Hóa học năm 2019 - Trường Chuyên Lam Sơn - Thanh Hóa lần 2
Đề thi thử THPT QG môn Hóa học năm 2019 - Trường Chuyên Lam Sơn - Thanh Hóa lần 2
-
Hocon247
-
40 câu hỏi
-
90 phút
-
20 lượt thi
-
Trung bình
Tham gia [ Hs Hocon247.com ] - Cộng Đồng Luyện Thi Trực Tuyến để được học tập những kiến thức bổ ích từ HocOn247.com
Phần trăm khối lượng của nguyên tố oxi trong glucozơ là
CTPT của glucozơ là C6H12O6 có %O = 53,33%
Đáp án B
Kim loại nào sau đây thuộc nhóm kim loại kiềm thổ?
Ca thuộc nhóm kim loại kiềm thổ → Đáp án B
Chất ít tan trong nước là
Chất ít tan trong nước là CO2.
Đáp án C
Chất tham gia phản ứng màu biure là
Chất tham gia phản ứng màu biure là anbumin.
Đáp án C
Dung dịch anilin (C6H5NH2) không phản ứng với chất nào sau đây
+ Anilin là 1 bazo ⇒ dễ dàng tác dụng với axit HCl và HCOOOH.
+ Anilin + Br2 tạo kết tủa trắng.
Đáp án A
Kim loại dẫn điện tốt thứ hai sau kim loại Ag là
Kim loại dẫn điện tốt thứ hai sau kim loại Ag là Cu
Đáp án D
Polime nào sau đây thuộc loại tơ poliamit?
Tơ nilon-6,6 thuộc loại tơ poliamit
Đáp án A
Công thức của crom (VI) oxit là
Công thức của crom (VI) oxit là CrO3
Đáp án B
Chất bị thủy phân trong môi trường kiềm là
Chất bị thủy phân trong môi trường kiềm là Gly-Ala-Gly.
Đáp án C
Tôn là sắt được tráng
Tôn là sắt được tráng kim loại Zn.
Đáp án C
Muối nào sau đây dễ bị nhiệt phân?
Các muối NaCl, NaNO2, Na2CO3 đều không bị nhiệt phân hủy.
NH4HCO3 dễ bị nhiệt phân
Kết luận nào sau đây không đúng?
Ống thép (dẫn nước, dẫn dầu, dẫn khí đốt) ở dưới đất được bảo vệ chủ yếu bởi một lớp sơn dày → Sai
Đáp án C
Cho dãy các chất: Cu, Na, Zn, Mg, Ba, Ni. Số chất trong dãy phản ứng với dung dịch FeCl3 dư có sinh ra kết tủa là
Chỉ có Na, Ba thõa mãn
Đốt cháy 0,01 mol este X đơn chức bằng lượng oxi vừa đủ, thu được 448 ml khí CO2 (đktc). Mặt khác, đun nóng 6,0 gam X với dung dịch KOH vừa đủ, thu được lượng muối là
nCO2 = 0,02 mol
Số C = nCO2/nX = 2 → X là HCOOCH3
nHCOOK = nHCOOCH3 = 0,1 mol
→ mHCOOK = 8,4 gam
Sục từ từ 10,08 lít CO2 ở đktc vào dung dịch chứa 0,2 mol Ca(OH)2 và a mol KOH, sau khi phản ứng hoàn toàn, lọc bỏ kết tủa, lấy dung dịch nước lọc đun nóng lại thu được 5 gam kết tủa. Tính a
nCO2 = 0,45 mol
Đun nóng nước lọc thu được 0,05 mol CaCO3:
Ca(HCO3)2 → CaCO3 + CO2 + H2O
→ Các sản phẩm phản ứng bao gồm Ca(HCO3)2 (0,05), CaCO3 ( 0,2 - 0,05 = 0,15), KHCO3 (a)
BTNT(C): a + 0,15 + 0,05.2 = 0,45 → a = 0,2 mol
Phân tử khối trung bình của xenlulozơ (C6H10O5)n là 162000 đvC. Giá trị của n là
M = 162n = 1620000 → n = 10000
X là một α-amino axit chứa 1 nhóm NH2.Cho m gam X phản ứng vừa đủ với 25 ml dung dịch HCl 1M, thu được 3,1375 gam muối. X là
nmuối = nHCl = 0,025 mol
→ Mmuối = 3,1375/0,025 = 125,5
→ MX = Mmuối - 36,5 = 89
→ Alanin
Xà phòng hóa hoàn toàn 17,24 gam một triglixerit cần vừa đủ 0,06 mol NaOH. Cô cạn dung dịch sau phản ứng thu được khối lượng xà phòng là
nC3H5(OH)3 = nNaOH/3 = 0,02 mol
BTKL: mxà phòng = 17,8 gam
Khi đốt 0,1 mol một chất X (dẫn xuất của benzen), khối lượng CO2 thu được nhỏ hơn 35,2 gam. Biết rằng, 1 mol X chỉ tác dụng được với 1 mol NaOH. Công thức cấu tạo thu gọn của X là
nCO2 < 8
→ Số C = nCO2/nX < 8
1 mol X tác dụng với 1 mol NaOH nên X là HOC6H4CH2OH
Nhiệt phân hidroxit Fe (II) trong không khí đến khi khối lượng không đổi thu được
Phương trình: 4Fe(OH)2 + O2(không khí) → 2Fe2O3 + H2O
Hỗn hợp X gồm Mg và Al. Cho 0,75 gam X phản ứng với HNO3 đặc, nóng, dư, thu được 1,568 lít NO2 (sản phẩm khử duy nhất ở đktc), tiếp tục cho thêm dung dịch NaOH dư vào, sau khi các phản ứng hoàn toàn thu được m gam kết tủa. Tìm m?
X gồm Mg (a) và Al (b)
mX = 24a + 27b = 0,75
nNO2 = 2a + 3b = 0,07
→ a = 0,02 và b = 0,01
→ mMg(OH)2 = 58a = 1,16 gam
Este X được điều chế từ aminoaxit A và ancol B. Hóa hơi 2,06 gam X hoàn toàn chiếm thể tích bằng thể tích của 0,56 gam nitơ ở cùng điều kiện nhiệt độ, áp suất. Biết rằng từ B có thể điều chế cao su Buna bằng 2 giai đoạn. Hợp chất X có công thức cấu tạo là
nX = nN2 = 0,02 mol → MX = 103
Từ ancol B điều chế cao su Buna bằng 2 giai đoạn → B là C2H5OH (C2H5OH → C4H6 → Cao su Buna)
X là NH2-CH2-COO-C2H5.
Cho các chất và dung dịch sau: K2O, dung dịch HNO3, dung dịch KMnO4/H+, dung dịch AgNO3, dung dịch NaNO3, dung dịch nước brom, dung dịch NaOH, dung dịch CH3NH2, dung dịch H2S. Số chất và dung dịch phản ứng được với dung dịch FeCl2 mà tạo thành sản phẩm không có chất kết tủa là
Các dung dịch thỏa mãn: dung dịch HNO3, dung dịch KMnO4/H+ , dung dịch nước brom:
Fe2+ + H+ + NO3- → Fe3+ + NO + H2O
Fe2+ + H+ + MnO4- → Fe3+ + Mn2+ + H2O
Cl- + H+ + MnO4- → Cl2 + Mn2+ + H2O
Fe2+ + Br2 → Fe3+ + Br-
Các dung dịch NaOH, CH3NH2 không thõa mãn vì tạo kết tủa Fe(OH)2
Các dung dịch NaNO3, H2S không thõa mãn vì không phản ứng.
Trong các chất sau, chất nào sau đây có nhiệt độ sôi cao nhất?
Axit cacboxylic có nhiệt độ sôi cao nhất so với các chất este, amin, ancol có khối lượng phân tử xấp xỉ nhau
Thủy phân 200 gam dung dịch saccarozơ 6,84%, sau một thời gian, lấy hỗn hợp sản phẩm cho tác dụng với dung dịch AgNO3/NH3 dư, sau phản ứng thu được 12,96 gam Ag. Tính hiệu suất phản ứng thủy phân
nC12H22O11 ban đầu = 200.6,84%/342 = 0,04 mol
C12H22O11 → 2C6H12O6 → 4Ag
0,03 0,12
→ H = 0,03/0,04 = 75%
X là hidrocacbon mạch hở có công thức phân tử C4Hx, biết X không tạo kết tủa khi tác dụng với dung dịch AgNO3/NH3. Số công thức cấu tạo phù hợp với X là
X không tác dụng với AgNO3/NH3 nên X không có nối ba đầu mạch:
CH3-CH2-CH2-CH3
(CH3)3C
CH2=CH-CH2-CH3
CH3-CH=CH-CH3
CH2=C(CH3)2
CH2=C=CH-CH3
CH2=CH-CH=CH2
CH3-CC-CH3
CH2=C=C=CH2
Cho hỗn hợp X gồm Na, Ba có cùng số mol vào 125 ml dung dịch gồm H2SO4 1M và CuSO4 1M, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Y, m gam kết tủa và 3,36 lít khí (đktc). Giá trị của m là
nNa = nBa = x mol
Bảo toàn electron: x + 2x = 0,15.2 → x = 0,1
nH2SO4 = nCuSO4 = 0,125
nOH- = 2nH2 = 0,3
nOH- = nH+ + 2nCu(OH)2 → nCu(OH)2 = 0,025 mol
nBaSO4 = nBa = 0,1 mol → m = 25,75
Kết quả thí nghiệm của chất vô cơ X với thuốc thử được ghi ở bảng sau:
X làm dd phenolphtalein chuyển sang màu hồng → X là chất có môi trường bazo
X phản ứng với Cl2 tạo khói trắng → X + HCl tạo ra chất có dạng RNH3Cl (khói trắng)
→ X là NH3
A. đúng vì phân đạm cung cấp nguyên tố dinh dưỡng nito cho cây trồng.
B. đúng
C. đúng, từ NH3 có thể sản xuất ra NH4HCO3 dùng làm bột nở trong công nghiệp sản xuất bánh kẹo.
D. Sai vì Al(OH)3 không tan khi cho dd NH3 dư
3NH3 + AlCl3 + 3H2O → 3NH4Cl + Al(OH)3↓
Đáp án cần chọn là: D
Cho các polime sau: PVC, teflon, PE, cao su Buna, tơ axetat, tơ nitron, cao su isopren, tơ nilon-6,6. Số polime được điều chế từ phản ứng trùng hợp là
Các polime thỏa mãn là PVC; teflon; PE; Cao su Buna; tơ nitron; cao su isopren
⇒ chọn C.
Cho các ứng dụng: dùng làm dung môi (1): dùng để tráng gương (2); dùng làm nguyên liệu để sản xuất một số chất dẻo, dược phẩm (3); dùng trong công nghiệp thực phẩm (4). Những ứng dụng của este là
Các este có khả năng hòa tan nhiều chất hữu cơ → làm dung môi → 1 đúng
Các este thường có mùi thơm được dùng trong công nghiệp thực phẩm → 4 đúng
Một số este ví dụ như asprin ( este của axit salixylic )được dùng làm thuốc chữa bệnh đau đầu → 3 đúng
Trong công nghiệp chất được dùng để tráng gương là glucozo.
Đáp án A.
Trong công nghiệp, nhôm được sản xuất bằng phương pháp điện phân Al2O3 nóng chảy với các điện cực làm bằng than chì. Khi điện phân nóng chảy Al2O3 với dòng điện cường độ 9,65A trong thời gian 3000 giây thu được 2,16 gam Al. Phát biểu nào sau đây sai?
ne = It/F = 0,3 mol
nAl = 0,08 mol → Hiệu suất = 0,08.3/0,3 = 80%
D sai, sau một thời gian điện phân phải thay thế anot do O2 sinh ra từ anot đã đốt cháy anot
Nhỏ từ từ V lít dung dịch chứa Ba(OH)2 0,5M vào dung dịch chứa x mol NaHCO3 và y mol BaCl2. Đồ thì sau đây biểu diễn sự phụ thuộc giữa số mol kết tủa và thể tích dung dịch Ba(OH)2.
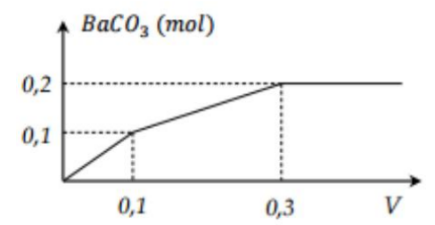
Giá trị x, y tương ứng là
Tính từ gốc tọa độ:
+ Đoạn đồ thị đầu tiên:
Ba(OH)2 + BaCl2 + 2NaHCO3 → 2BaCO3 + 2NaCl + 2H2O
→ nBaCl2 = y = nBaCO3/2 = 0,05 mol
Sau phản ứng này nNaHCO3 dư = x - 0,1
+ Đoạn đồ thị tiếp theo:
Ba(OH)2 + NaHCO3 → BaCO3 + NaOH + H2O
→ nNaHCO3 = x - 0,1 = nBaCO3 → x = 0,2
Vậy x = 0,2 và y = 0,05
Hỗn hợp X gồm metyl fomat, đimetyl oxalat và este Y đơn chức, có hai liên kết pi trong phân tử, mạch hở. Đốt cháy hoàn toàn 0,5 mol X cần dùng 1,25 mol O2 thu được 1,3 mol CO2 và 1,1 mol H2O. Mặt khác, cho 0,4 mol X tác dụng vừa đủ với dung dịch NaOH, thu được dung dịch Z (giả thiết chỉ xảy ra phản ứng xà phòng hóa). Cho toàn bộ Z tác dụng với lượng dư dung dịch AgNO3 trong NH3, đun nóng. Sau khi các phản ứng xảy ra hoàn toàn, khối lượng Ag tối đa thu được là
X gồm:
C2H4O2: a mol
C4H6O4: b mol
CnH2n-2O2: c mol
nX = a + b + c = 0,5
nCO2 = 2a + 4b + nc = 1,3
nH2O = 2a + 3b + nc - c = 1,1
nO = 2a + 4b + 2c = 1,2
→ a = 0,3; b = 0,1; c = 0,1; n =3
→ Y là HCOOCH=CH2
Thủy phân 0,5 mol X → HCOONa (a + c = 0,4), CH3CHO (0,1) → nAg = 1
Tỉ lệ: Từ 0,5 mol X thu được 1 mol Ag
→ Từ 0,3 mol X thu được 0,3.1/0,5 = 0,6 mol Ag
→ mAg = 64,8 gam
X là đipeptit Val-Ala, Y là tripeptit Gly-Ala-Glu. Đun nóng m gam hỗn hợp X và Y có tỉ lệ số mol nX : nY = 3 : 2 với dung dịch KOH vừa đủ, sau khi phản ứng kết thúc thu được dung dịch Z. Cô cạn dung dịch Z thu được 17,72 gam muối. Giá trị của m gần nhất với?
nX = 3x (mol) → nY = 2x (mol)
Bảo toàn các mắt xích → Dung dịch Z chứa:
nGlyK = 2x
nAlaK = 5x
nValK = 3x
nGluK2 = 2x
mmuối = 117,72 → x = 0,01
→ m = mX + mY = 11,14 gam
Cho các phát biểu sau:
(1) Fe trong gang và thép bị ăn mòn điện hóa trong không khí ẩm.
(2) Nước để lâu ngoài không khí có pH < 7.
(3) Điều chế poli (etylen terephtalat) có thể thực hiện bằng phản ứng trùng hợp hoặc trùng ngưng.
(4) Axit nitric còn được dùng để sản xuất thuốc nổ TNT, sản xuất thuốc nhuộm, dược phẩm.
(5) Nitơ lỏng dùng để bảo quản máu và các mẫu sinh học khác.
(6) Triolein tác dụng được với H2 (xúc tác Ni, t°), dung dịch Br2, Cu(OH)2.
(7) Photpho dùng để sản xuất bom, đạn cháy, đạn khói.
(8) Xăng E5 là xăng sinh học được pha 5% bio-ethanol (sản xuất chủ yếu từ lương thực như ngô, sắn, ngũ cốc và củ cải đường), 95% còn lại là xăng Ron A92 “truyền thống”.
Số phát biểu đúng là
(1) Đúng, cặp điện cức Fe-C
(2) Đúng, dó có hòa tan CO2
(3) sai, đồng trùng ngưng C2H4(OH)2 và p-C6H4(COOH)
(4) Đúng
(5) Đúng
(6) Sai, triolein không tác dụng với Cu(OH)2
(7) Đúng
(8) Đúng
Cho muối X có công thức phân tử C3H12N2O3. Cho X tác dụng hết với dung dịch NaOH đun nóng, sau phản ứng thu được hỗn hợp khí Z (làm hóa xanh quỳ tím tẩm nước cất) và muối axit vô cơ. Có bao nhiêu công thức cấu tạo của X thỏa mãn điều kiện?
X + NaOH → Hỗn hợp khí nên X là muối amoni tạo bởi 2 cation khác nhau.
Các cấu tạo của X:
C2H5-NH3-CO3-NH4
(CH3)2NH2-CO3-NH4
Hỗn hợp X gồm MgO, Al2O3, Mg, Al. Hòa tan m gam hỗn hợp X bằng dung dịch HCl vừa đủ thì thu được dung dịch chứa (m + 70,295) gam muối. Cho 2m gam hỗn hợp X tác dụng với dung dịch H2SO4 đặc, nóng dư thu được 26,656 lít SO2 (đktc, sản phẩm khử duy nhất). Nếu cho 2m gam hỗn hợp X tác dụng với dung dịch HNO3 loãng, dư thu được 7,616 lít hỗn hợp khí NO và N2O (đktc) có tỉ khối so với hidro là 318/17, dung dịch Y. Cô cạn dung dịch Y thu được 324,3 gam muối khan. Giá trị của m gần giá trị nào nhất sau đây?
nSO2 = 0,595 mol
BT electron: nH2 = 0,595 mol
Đặt nO(A) = x → nH2O = x
BTNT(H): nHCl = 2x + 1,19
mmuối = m - 16x + 35,5(2x + 1,19) = m + 70,295
→ x = 0,51
Với HNO3:
nNO = 0,08 và nN2O = 0,09
BT electron → 0,595.2 = 3nNO + 8nN2O + 8nNH4NO3 → nNH4NO3 = 0,02875
mmuối = ( m - 16x) + 62.( 0,595.2 + 2x) + 80.0,02875 = 162,15
→ m = 30,99
Cho hỗn hợp Z gồm peptit mạch hở X và amino axit Y (MX > 4MY) với tỉ lệ mol tương ứng 1 : 1. Cho m gam Z tác dụng vừa đủ với dung dịch NaOH, thu được dung dịch T chứa (m + 12,24) gam hỗn hợp muối natri của glyxin và alanin. Dung dịch T phản ứng tối đa với 360 ml dung dịch HCl 2M, thu được dung dịch chứa 63,72 gam hỗn hợp muối. Các phản ứng xảy ra hoàn toàn. Kết luận nào sau đây đúng?
Quy đổi Z thành: C2H3ON (a mol), CH2 (b mol), H2O (c mol)
nNaOH = a và nH2O = c
→ 40a - 18c = 12,24 (1)
nHCl = nN + nNaOH → a + a = 0,72 (2)
mmuối = mGlyNa + mAlaNa + mHCl
→ 57a + 14b + 40a + 0,72.36,5 = 63,72 (3)
(1)(2)(3) → a = 0,36; b = 0,18; c = 0,12
nAla = b = 0,18 → nGly = a - b = 0,18
Số N trung bình = a/c = 3, tỉ lệ mol 1:1 và Y có 1N nên X có 5N → B sai
nX = nY = c/2 = 0,06
Nếu Y là Ala thì X có số Ala = (0,18 - 0,06)/0,06 = 2 và số Gly = 0,18/0,06 = 3
→ X là (Gly)3(Ala)2 : Không thõa mãn giả thiết MX > 4MY, loại.
Vậy Y là Gly và X là (Gly)2(Ala)3
→ Kết luận D đúng.
Hỗn hợp X gồm một axit, một este và một ancol đều no, đơn chức, mạch hở. Cho m gam hỗn hợp X tác dụng vừa đủ với dung dịch NaHCO3 thu được 28,8 gam muối. Nếu cho a gam hỗn hợp X tác dụng vừa đủ với dung dịch NaOH thì thu được 3,09 gam hỗn hợp muối được tạo ra bởi hai axit là đồng đẳng kế tiếp và 0,035 mol một ancol duy nhất Y, biết tỉ khối hơi của ancol Y so với hidro nhỏ hơn 25 và ancol Y không điều chế trực tiếp được từ chất vô cơ. Đốt cháy hoàn toàn 3,09 gam 2 muối trên bằng oxi thì thu được muối Na2CO3, hơi nước và 2,016 lít CO2 (đktc). Giá trị gần nhất của m là
MY < 50 và không điều chế trực tiếp từ các chất vô cơ nên Y là C2H5OH
2CnH2n-1O2Na + O2 → (2n - 1) CO2 + (2n - 1) H2O + Na2CO3
nCO2 = 0,09 → nmuối = 0,18/(2n-1)
mmuối = (14n + 54).0,18/(2n - 1) = 3,09 gam
→ n = 3,5
→ Muối gồm C2H5COONa (0,015) và C3H7COONa (0,015)
TH1: X gồm C2H5COOH (0,015), C3H7COOC2H5 ( 0,015) và C2H5OH (0,02)
→ mX = 3,77
X + NaHCO3 → C2H5COONa (0,015) → mmuối = 1,44 gam
Tỉ lệ: 3,77 gam X tạo ra 1,44 gam muối
→ m gam X tạo ra 28,8 gam muối → m = 75,4 gam
TH2: X gồm C3H7COOH (0,015), C2H5COOC2H5 (0,015) và C2H5OH (0,02)
→ mX = 3,77
X + NaHCO3 → C3H7COONa (0,015) → mmuối = 1,65
Tỉ lệ: 3,77 gam X tạo ra 1,65 gam muối → m gam X tạo ra 28,8 gam muối
→ m = 65,80 gam
Hòa tan hoàn toàn m gam hỗn hợp X gồm Mg, Fe, FeCO3, Cu(NO3)2 vào dung dịch chứa NaNO3 (0,045 mol) và H2SO4, thu được dung dịch Y chỉ chứa các muối trung hòa có khối lượng 62,605 gam và 3,808 lít (đktc) hỗn hợp khí Z (trong đó có 0,02 mol H2). Tỉ khối hơi của Z so với O2 bằng 19/17. Thêm tiếp dung dịch NaOH 1M vào Y đến khi thu được lượng kết tủa lớn nhất là 31,72 gam thì vừa hết 865 ml. Mặt khác, cho Y tác dụng vừa đủ với dung dịch BaCl2 được hỗn hợp T. Cho lượng dư dung dịch AgNO3 vào T thu được 256,04 gam kết tủa. Giá trị của m là
Trong Y đặt MgSO4, FeSO4, CuSO4 và (NH4)2SO4 lần lượt là a, b, c, d mol.
Ta có: nNa2SO4 trong Y = 0,0225 mol
→ 120a + 152b + 160c + 132d + 0,0225.142 = 62,605 (1)
nNaOH = 2a + 2b + 2c + 2d = 0,865
mkết tủa = 58a + 90b + 98c = 31,72 gam (2)
Sản phẩm sau đó là Na2SO4 → nNa2SO4 = 0,4325 + 0,0225 = 0,455
nBaCl2 = 0,455 → Vừa đủ để tạo ra nBaSO4 = 0,455
sau đó thêm tiếp AgNO3 dư → Tạo thêm nAgCl = 0,455.2 = 0,91 và nAg = nFe2+ = b
→ mkết tủa = 108b + 0,91.143,5 + 0,455.233 = 256,04 gam (3)
Từ (1)(2)(3) → a = 0,2; b = 0,18; c = 0,04; d = 0,0125
Như trên đã có nH2SO4 = nNa2SO4 tổng = 0,455 mol
BTNT(H): 2nH2SO4 = 8n(NH4)2SO4 + 2nH2 + 2nH2O → nH2O = 0,385 mol
BTKL: mA + mNaNO3 + mH2SO4 = mmuối + mkhí + mH2O
→ mA = 27,2 gam

