Đề thi thử THPT QG năm 2021 môn Hóa học - Trường THPT Lý Thường Kiệt
Đề thi thử THPT QG năm 2021 môn Hóa học - Trường THPT Lý Thường Kiệt
-
Hocon247
-
40 câu hỏi
-
90 phút
-
28 lượt thi
-
Trung bình
Tham gia [ Hs Hocon247.com ] - Cộng Đồng Luyện Thi Trực Tuyến để được học tập những kiến thức bổ ích từ HocOn247.com
Cho các chất sau: NaHCO3, Al, (NH4)2CO3, Al2O3, ZnO, Sn(OH)2, Cr(OH)3, Ala, axit glutamic. Số chất có tính lưỡng tính là:
Số chất có tính lưỡng tính là 8 (NaHCO3, (NH4)2CO3, Al2O3, ZnO, Sn(OH)2, Cr(OH)3, Ala, axit glutamic)
Cho các phát biểu sau:
(1). Các amin đều phản ứng được với dung dịch HCl.
(2). Tripanmitin, tristearin đều là chất rắn ở điều kiện thường.
(3). Phản ứng thủy phân chất béo trong (NaOH, KOH) là phản ứng xà phòng hóa.
(4). Sản phẩm trùng ngưng metylmetacrylat được dùng làm thủy tinh hữu cơ.
(5). Các peptit đều có phản ứng màu biure.
(6). Tơ nilon – 6 có chứa liên kết peptit.
(7). Dùng H2 oxi hóa glucozơ hay fructozơ đều thu được sobitol.
Tổng số phát biểu đúng là:
Tổng số phát biểu đúng là 3: 1, 2, 3
Cho các thí nghiệm sau:
(1). Cho NO2 vào dung dịch NaOH. (2). Cho HCl vào dung dịch K2Cr2O7
(3). Cho HCl vào dung dịch Fe(NO3)3 (4). Cho BaCl2 vào dung dịch K2CrO4
(5). Cho Cu vào dung dịch hỗn hợp KNO3 và HCl (6). Đốt Ag ở nhiệt độ cao ngoài không khí.
Số thí nghiệm xảy ra phản ứng oxi hóa khử là:
Số thí nghiệm xảy ra phản ứng oxi hóa khử là: 1, 2, 5
Cho 8,905 gam Ba tan hết vào V ml dung dịch Al2(SO4)3 0,1M. Sau khi các phản ứng kết thúc thấy khối lượng dung dịch giảm 7,545 gam so với ban đầu. Giá trị của V gần nhất với giá trị nào sau đây?
\({n_{Ba}} = 0,065\xrightarrow{{}}{m_ \downarrow } = 16,32\xrightarrow{{}}\left\{ \begin{gathered} BaS{O_4}:a \hfill \\ Al{(OH)_3}:b \hfill \\ B{a^{2 + }}:0,065 - a \hfill \\ AlO_2^ - :0,13 - 2a \hfill \\ \end{gathered} \right.\)
\(\xrightarrow{{}}\left\{ \begin{gathered} 233a + 78b = 16,32 \hfill \\ a = 1,5(b + 0,13 - 2a) \hfill \\ \end{gathered} \right.\xrightarrow{{}}\left\{ \begin{gathered} a = 0,06 \hfill \\ b = 0,03 \hfill \\ \end{gathered} \right.\xrightarrow[{}]{}V = 200(ml)\)
Đốt cháy hoàn toàn 6,75 gam hỗn hợp E chứa 3 este đều đơn chức, mạch hở cần vừa đủ 8,904 lít O2 (đktc) thu được CO2 và 4,95 gam H2O. Mặt khác, thủy phân hoàn toàn lượng E trên bằng dung dịch chứa NaOH (vừa đủ) thu được 2 ancol (no, đồng đẳng liên tiếp) và hai muối X, Y có cùng số C (MX>MY và nX <nY) . Đốt cháy hoàn toàn lượng ancol trên cần vừa đủ 0,18 mol O2. Tỷ số nX:nY là?
Đốt cháy E \(\xrightarrow{{}}6,75 + 0,3975.32 = 44{n_{C{O_2}}} + 0,275.18\xrightarrow{{}}{n_{C{O_2}}} = 0,33\)
\(\xrightarrow{{BTKL}}n_O^{trong\,E} = 0,14\xrightarrow{{}}{n_E} = {n_{COO}} = 0,07\)
Ta có: \({n_{NaOH}} = 0,07\xrightarrow{{}}{n_E} = 0,07\xrightarrow{{}}{n_{ancol}} = 0,07\xrightarrow{{chay}}\left\{ \begin{gathered} C{O_2}:a \hfill \\ {H_2}O:a + 0,07 \hfill \\ \end{gathered} \right.\)
\(\xrightarrow{{BTNT.O}}a = 0,12\xrightarrow{{}}n_C^{axit} = 0,21\xrightarrow{{}}{C_3}\) và \(\left\{ \begin{gathered} C{H_3}OH:0,02 \hfill \\ {C_2}{H_5}OH:0,05 \hfill \\ \end{gathered} \right.\)
\(\xrightarrow{{}}n_H^{trong\,RCOO} = 0,24\xrightarrow{{}}\overline H = 3,43\xrightarrow{{}}\left\{ \begin{gathered} {C_2}{H_5}COO:0,015 \hfill \\ {C_2}{H_3}COO:0,055 \hfill \\ \end{gathered} \right.\xrightarrow{{}}3:11\)
Cho m gam hỗn hợp chứa KCl và CuSO4 vào nước thu được dung dịch X. Điện phân dung dịch X trong thời gian t giây thu được dung dịch Y có khối lượng dung dịch giảm đi 9,3 gam. Nếu điện phân dung dịch X trong thời gian 2t giây thu được dung dịch có khối lượng giảm 12,2 gam và thoát ra 0,05 mol khí ở catot. Giá trị của m là:
\(\xrightarrow{{}}\left\{ \begin{gathered} \xrightarrow{{2t}}catot\left\{ \begin{gathered} Cu:a \hfill \\ {H_2}:0,05 \hfill \\ \end{gathered} \right.\xrightarrow{{}}anot\left\{ \begin{gathered} C{l_2}:b \hfill \\ {O_2}:\frac{{2a + 0,1 - 2b}}{4} \hfill \\ \end{gathered} \right. \hfill \\ \xrightarrow{t}catot\left\{ \begin{gathered} Cu:0,5a + 0,025 \hfill \\ {H_2}:0 \hfill \\ \end{gathered} \right.\xrightarrow{{}}anot\left\{ \begin{gathered} C{l_2}:b \hfill \\ {O_2}:\frac{{a + 0,05 - 2b}}{4} \hfill \\ \end{gathered} \right. \hfill \\ \end{gathered} \right.\)
\(\xrightarrow{{}}\left\{ \begin{gathered} 80a + 55b + 0,9 = 12,2 \hfill \\ 40a + 55b + 2 = 9,3 \hfill \\ \end{gathered} \right.\xrightarrow{{}}\left\{ \begin{gathered} a = 0,1 \hfill \\ b = 0,06 \hfill \\ \end{gathered} \right.\xrightarrow{{}}m = 24,94\left\{ \begin{gathered} CuS{O_4}:0,1 \hfill \\ KCl:0,12 \hfill \\ \end{gathered} \right.\)
Hòa tan hoàn toàn m gam hỗn hợp X chứa Fe, Mg, Fe2O3 và Fe(NO3)2 trong dung dịch chứa 0,01 mol HNO3 và 0,51 mol HCl thu được dung dịch Y chỉ chứa (m + 14,845) gam hỗn hợp muối và 1,12 lít hỗn hợp khí Z (đktc) gồm hai đơn chất khí với tổng khối lượng là 0,62 gam. Cho NaOH dư vào Y thu được 17,06 gam kết tủa. Phần trăm khối lượng của Fe2O3 có trong X là:
\(\xrightarrow{{BTKL}}m + 19,245 = m + 14,845 + 0,62 + 18{n_{{H_2}O}}\xrightarrow{{}}{n_{{H_2}O}} = 0,21(mol)\)
\({n_Z} = 0,05\left\{ \begin{gathered} {H_2}:0,03\xrightarrow{{BTNT.H}}{n_{NH_4^ + }} = 0,01 \hfill \\ {N_2}:0,02\xrightarrow{{BTNT.N}}{n_{Fe{{(N{O_3})}_2}}} = 0,02 \hfill \\ \end{gathered} \right.\)
\(\xrightarrow{{{H^ + }}}{n_O} = 0,06\xrightarrow{{}}{n_{F{e_2}{O_3}}} = 0,02\)
Điền số điện tích cho kết tủa \(\xrightarrow{{}}17,06\left\{ \begin{gathered} O{H^ - }:0,51 - 0,01 = 0,5 \hfill \\ \xrightarrow{{BTKL}}Mg,Fe:8,56\,(gam) \hfill \\ \end{gathered} \right.\)
\(\xrightarrow{{}}m = 12\xrightarrow{{}}\% F{e_2}{O_3} = 26,67\% \)
Đốt cháy hoàn toàn 19,32 gam hỗn hợp E gồm hai peptit mạch hở, hơn kém nhau hai nguyên tử cacbon, đều được tạo từ Gly và Ala (MX <MY) cần dùng 0,855 mol O2, sản phẩm cháy gồm CO2, H2O và N2 được dẫn qua dung dịch Ca(OH)2 dư, thấy khối lượng bình tăng 42,76 gam. Phần trăm khối của X trong E gần nhất?
\(\xrightarrow{{BTKL}}19,32 + 0,855.32 = 42,76 + 28{n_{{N_2}}}\xrightarrow{{}}{n_{{N_2}}} = 0,14\)
\(42,76\left\{ \begin{gathered} C{O_2}:a \hfill \\ {H_2}O:b \hfill \\ \end{gathered} \right.\xrightarrow{{}}\left\{ \begin{gathered} 44a + 18b = 42,76 \hfill \\ \xrightarrow{{NAP.332}}3a - 3.0,14 = 2.0,855 \hfill \\ \end{gathered} \right.\xrightarrow{{}}\left\{ \begin{gathered} a = 0,71 \hfill \\ b = 0,64 \hfill \\ \end{gathered} \right.\)
Dồn chất \(\xrightarrow{{}}{n_X} = 0,07\xrightarrow{{}}\overline C = 10,14\xrightarrow{{}}\left\{ \begin{gathered} {C_9}:0,03 \hfill \\ {C_{11}}:0,04 \hfill \\ \end{gathered} \right.\)
Và \(\overline {mat\,xich} = 4,0\xrightarrow{{}}\left\{ \begin{gathered} Gl{y_3}Ala:0,03\xrightarrow{{}}40,37\% \hfill \\ Gly - Va{l_3}:0,04 \hfill \\ \end{gathered} \right.\)
X là este no, hai chức; Y là este tạo bởi glyxerol và một axit cacboxylic đơn chức, không no chứa một liên kết C=C (X,Y đều mạch hở và không chứa nhóm chức khác). Đốt cháy hoàn toàn 17,02 gam hỗn hợp E chứa X, Y thu được 18,144 lít CO2 (đktc). Mặt khác đun nóng 0,12 mol E cần dùng 570 ml dung dịch NaOH 0,5 M; cô cạn dung dịch sau phản ứng thu được hỗn hợp chứa 3 muối trong đó có hai muối no (Z, T) và hai ancol có cùng số nguyên tử cacbon. Số cặp (Z, T) thỏa mãn là?
\(\left\{ \begin{gathered} {n_{NaOH}} = 0,285 \hfill \\ {n_E} = 0,12 \hfill \\ \end{gathered} \right.\xrightarrow{{}}\left\{ \begin{gathered} {n_Y} = 0,045 \hfill \\ {n_X} = 0,075 \hfill \\ \end{gathered} \right.\)
Với 17,02 gam E \(\left\{ \begin{gathered} {n_X} = x \hfill \\ {n_Y} = y \hfill \\ \end{gathered} \right.\xrightarrow{{chay}}\left\{ \begin{gathered} C{O_2}:0,81 \hfill \\ {H_2}O:z \hfill \\ \end{gathered} \right.\xrightarrow{{}}\left\{ \begin{gathered} 3x - 5y = 0 \hfill \\ x + 5y = 0,81 - z \hfill \\ 0,81.12 + 2z + 32(2x + 3y) = 17,02 \hfill \\ \end{gathered} \right.\)
\(\xrightarrow{{}}\left\{ \begin{gathered} x = 0,05 \hfill \\ y = 0,03 \hfill \\ z = 0,61 \hfill \\ \end{gathered} \right.\xrightarrow{{}}\left\{ \begin{gathered} C{H_2} = CH - COONa:0,03 \hfill \\ {C_6}:0,05 \hfill \\ \end{gathered} \right.\xrightarrow{{}}\left\{ \begin{gathered} \left\{ \begin{gathered} {C_2} \hfill \\ {C_4} \hfill \\ \end{gathered} \right.\xrightarrow{{}}2 \hfill \\ \left\{ \begin{gathered} {C_1} \hfill \\ {C_5} \hfill \\ \end{gathered} \right.\xrightarrow{{}}4 \hfill \\ \end{gathered} \right.\)
Ion kim loại nào sau đây có tính oxi hóa yếu nhất?
Ion kim loại Mg2+ có tính oxi hóa yếu nhất
Trong số các phương pháp làm mềm nước cứng, phương pháp nào chỉ khử được độ cứng tạm thời?
Trong số các phương pháp làm mềm nước cứng, phương pháp đun sôi nước chỉ khử được độ cứng tạm thời?
Một chất có chứa nguyên tố oxi, dùng để làm sạch nước và có tác dụng bảo vệ các sinh vật trên Trái Đất không bị bức xạ cực tím. Chất khí này là
Chất khí này là Ozon
Este nào sau đây tác dụng với dung dịch kiềm cho 2 muối và nước?
Este HCOOC6H5 tác dụng với dung dịch kiềm cho 2 muối và nước
Chất nào sau tác dụng được với dung dịch HCl nhưng không tác dụng với dung dịch NaOH?
Chất NaAlO2 tác dụng được với dung dịch HCl nhưng không tác dụng với dung dịch NaOH
Chất nào sau đây không bị oxi hoá bởi H2SO4 đặc, nóng là
Chất CuO không bị oxi hoá bởi H2SO4 đặc, nóng
Cho vài giọt dung dịch NaOH vào dung dịch FeCl3 hiện tượng xảy ra là
Cho vài giọt dung dịch NaOH vào dung dịch FeCl3 hiện tượng xảy ra là có kết tủa màu nâu đỏ xuất hiện.
Polime nào sau đây không chứa nguyên tố nitơ trong phân tử?
Polietilen không chứa nguyên tố nitơ trong phân tử
Chất X là một bazơ mạnh, được sử dụng rộng rãi trong nhiều ngành công nghiệp như sản xuất nước gia-ven, nấu xà phòng,… Công thức của X là
Công thức của X là NaOH
Nhận xét nào sau đây đúng?
Amilopectin có cấu trúc mạch phân nhánh.
Lên men ancol etylic (xúc tác men giấm), thu được chất hữu cơ X. Tên gọi của X là
Lên men ancol etylic (xúc tác men giấm), thu được chất hữu cơ axit axetic.
Ancol và amin nào sau đây cùng bậc?
CH3CHNH2CH3 và CH3CH2OH có cùng bậc
Khi đốt cháy hoàn toàn một polime X chỉ thu được CO2 và hơi nước với tỉ lệ số mol tương ứng là 1:1. X có thể là polime nào dưới đây ?
X có thể là polipropilen
Cho các chất sau: mononatri glutamat, phenol, glucozơ, etylamin, Gly-Ala. Số chất trong dãy tác dụng với dung dịch HCl loãng là
Số chất trong dãy tác dụng với dung dịch HCl loãng là 3
Hình vẽ bên mô tả thu khí X trong phòng thí nghiệm. (Thông Hiểu)
Khí X và Y có thể lần lượt là những khí nào sau đây?
Khí X và Y có thể lần lượt là N2 và NO2
Hợp chất hữu cơ X mạch hở có công thức phân tử là C4H8O4. Đun nóng X với dung dịch NaOH vừa đủ, thu được chất hữu cơ Y và ancol Z. Biết Y cho được phản ứng tráng bạc. Công thức của Z là
Công thức của Z là C3H5(OH)3
Thực hiện các thí nghiệm sau:
(a) Nhúng thanh Fe nguyên chất vào dung dịch CuSO4.
(b) Cho bột Fe vào dung dịch HNO3 đặc, nguội.
(c) Đốt cháy dây kim loại Fe trong khí Cl2.
(d) Cho hợp kim Fe-Cu vào dung dịch H2SO4 loãng.
(e) Nhúng miếng tôn (Fe-Zn) vào dung dịch muối ăn.
Số thí nghiệm xảy ra ăn mòn kim loại là
Số thí nghiệm xảy ra ăn mòn kim loại là 5
Cho các chất sau: vinylaxetilen, metyl acrylat, glixerol, polibutađien, toluen, fructozơ và anilin. Số chất làm mất màu dung dịch brom là
Số chất làm mất màu dung dịch brom là 4
Thực hiện các thí nghiệm sau:
- Cho hỗn hợp gồm 2a mol Na và a mol Al vào lượng nước dư.
- Cho a mol bột Cu vào dung dịch chứa a mol Fe2(SO4)3.
- Cho dung dịch chứa a mol KHSO4 vào dung dịch chứa a mol KHCO3.
- Cho dung dịch chứa a mol BaCl2 vào dung dịch chứa a mol CuSO4.
- Cho dung dịch chứa a mol Fe(NO3)2 vào dung dịch chứa a mol AgNO3.
- Cho a mol Na2O vào dung dịch chứa a mol CuSO4.
Sau khi kết thúc thí nghiệm, số trường hợp thu được dung dịch chứa hai muối là
Sau khi kết thúc thí nghiệm, số trường hợp thu được dung dịch chứa hai muối là 1
Cho a mol Fe tác dụng với a mol khí Cl2 thu được hỗn hợp rắn X. Cho X vào nước, thu được dung dịch Y (biết các phản ứng xảy ra hoàn toàn). Cho các chất (hoặc hỗn hợp các chất) sau: AgNO3, NaOH, Cu, HCl, hỗn hợp KNO3 và H2SO4 loãng. Số chất (hoặc hỗn hợp các chất) có thể tác dụng được với dung dịch Y là
Số chất (hoặc hỗn hợp các chất) có thể tác dụng được với dung dịch Y là 3
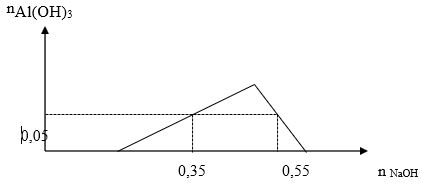
Một dung dịch X có chứa các ion: x mol H+, y mol Al3+, z mol SO42– và 0,1 mol Cl-. Khi nhỏ từ từ đến dư dung dịch NaOH vào dung dịch X, kết quả thí nghiệm được biểu diễn trên đồ thị sau:
Cho 300 ml dung dịch Ba(OH)2 0,9M tác dụng với dung dịch X thu được kết tủa Y và dung dịch Z. Khối lượng kết tủa Y là (các phản ứng xảy ra hoàn toàn)
- Tại vị trí n NaOH = 0, 35 mol ta có: nH+ = nNaOH - 3nAl(OH)3 = 0, 2 mol
- Tại vị trí n NaOH = 0, 55 mol ta có: nAl3+ = 0,1 mol
- Xét dung dịch X , áp dụng bảo toàn điện tích ta suy ra: z = 0,2 mol.
- Khi cho 0,27 mol Ba(OH)2 tác dụng với dung dịch X thì kết tủa thu được gồm BaSO4 và Al(OH)3 với
n BaSO4 = n SO42- = 0,2 mol và n Al(OH)3 = 4 nAl3+ - nOH- + nH+ = 0,06 mol
- M kết tủa = 51,28 g
Cho các phát biểu và nhận định sau:
- Xenlulozơ trinitrat có chứa 16,87% nitrơ.
- Glixerol, glucozơ và alanin là những hợp chất hữu cơ tạp chức.
- Thủy phân chất béo trong môi trường axit hoặc kiềm đều thu được glixerol.
- Đốt cháy hoàn toàn một đipeptit mạch hở, luôn thu được CO2 và H2O có tỉ lệ mol 1 : 1.
- Nhỏ dung dịch NaCl bão hoà vào dung dịch lòng trắng trứng thấy hiện tượng đông tụ lại.
- Isopropylamin là amin bậc hai.
Số phát biểu không đúng là
Số phát biểu không đúng là 4
Cho 14,35 gam muối MSO4.nH2O vào 300 ml dung dịch NaCl 0,6M thu được dung dịch X. Tiến hành điện phân dung dịch X bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện không đổi trong thời gian t giây, thấy khối lượng catot tăng m gam; đồng thời ở anot thu được 0,1 mol khí. Nếu thời gian điện phân là 2t giây, tổng thể tích khí thoát ra ở 2 cực là 7,28 lít (đktc). Giả sử hiệu suất của phản ứng điện phân là 100%. Giá trị của m là
|
Thời điểm |
Tại catot |
Tại anot |
|
- Tại t (s) |
M 2+ + 2eà M H2O + 2eà H2 + 2OH- |
2Cl - à Cl 2 + 2e 0,18mol 0,09mol 2H2O à 4H+ + 4e+ O2 |
|
- Tại 2t (s) |
M 2+ + 2eà M H2O + 2eà H2 + 2OH- |
2Cl - à Cl 2 + 2e 0,18mol 0,09mol 2H2O à 4H+ + 4e+ O2 |
- Xét quá trình điện phân tại thời điểm t (s):
- Ta có : nO2 = 0,1- nCl2 = 0,01mol à ne trao đổi = 2nCl2 + 4nO2 = 0,22mol
* Xét quá trình điện phân tại thời điểm 2t (s)
Ta có ne trao đổi = 2.0,22 = 0,44mol
- Tại anot : nO2 = (ne trao đổi-2nCl-) /4= 0,065 mol
Tại Catot : n H2 = 0,035- n Cl2 – nO2 = 0,17 mol →Bte: n M = (0,44 - 2nH2)/2 = 0,05 mol
- Xét muối ta có: n MSO4.nH2O= nM = 0,05mol → M MSO4.nH2O=14,35/0,05 = 287 àn=7, M=65 (Zn).
Vậy tại thời điểm t (s) thì tại catot tăng là 3,25g.
Cho hỗn hợp X dạng hơi gồm este Y (CnH2nO2) và este Z (CmH2m+1O2N); trong đó Z là este của amino axit. Đốt cháy hoàn toàn 33,95 gam X cần dùng 1,6625 mol O2. Mặt khác đun nóng 33,95 gam X với 400 ml dung dịch NaOH 1M (vừa đủ), thu được hỗn hợp chứa hai muối có cùng số nguyên tử cacbon. trong đó có a gam muối A và b gam muối B (MA < MB). Tỉ lệ gần nhất của a : b là
- Khi cho X tác dụng với NaOH thì: nX = nNaOH = 0,4mol →MX= 33,95/ 0,4 = 84,875
→ Este Y có CTPT là C2H4O2 hoặc C3H6O2 (vì MY > 85)
- Mặc khác theo dữ kiện đề bài thì hỗn hợp chứa 2 muối có cùng số nguyên tử C.
Từ hai dữ kiện trên ta suy ra được CTPT của X và Y lần lượt là CH3COOCH3 và NH2CH2COOR.
Giả sử R là –C2H5. Khi đó ta có hệ sau:
nY + nZ = 0,4
74nY + 103nZ = 33,95
nY = 0,25; nZ = 0,15
- Thử lại với dữ kiện oxi ta nhận thấy:
nO2 =3,5nCH3COOCH3 + 5,25nNH2CH2 COOC2H5 = 1,6625mol
Y là NH2CH2COOC2H5. Hỗn hợp muối gồm CH3COOH : 0,25 mol và H2NCH2COOH : 0,15 mol
mCH3COOH/mH2NCH2COOH = 1,4089
Kết quả thí nghiệm của các dung dịch X, Y, Z với thuốc thử được ghi ở bảng sau:
Dung dịch X, Y, Z lần lượt là Ba(OH)2, MgCl2, Al2(SO4)3.
Hỗn hợp X chứa ba este đều no, mạch hở và không chứa nhóm chức khác. Đốt cháy hoàn toàn 0,24 mol X với lượng oxi vừa đủ, thu được 60,72 gam CO2 và 22,14 gam H2O. Mặt khác, đun nóng 0,24 mol X với dung dịch KOH vừa đủ, thu được hỗn hợp gồm hai ancol đều đơn chức có tổng khối lượng là 20,88 gam và hỗn hợp Z chứa hai muối của hai axit cacboxylic có mạch không phân nhánh, trong đó có x gam muối X và y gam muối Y (MX < MY). Tỉ lệ gần nhất của x : y là
Nhận thấy khi đốt hỗn hợp X nCO2 > nH2O . Nên trong X có chứa este đa chức (B).
* Giả sử B là este hai chức và A là este đơn chức khi đó :
Áp dụng độ bất bão hòa khi đốt X ta có nB = nCO2 - nH2O = 0,15mol → nA = nX - nB = 0,09mol
- Ta có n -COO = 2nB + nA = 0,39mol suy ra mX = 12nCO2 + 2nH2O + 32 n -COO = 31,5(g)
- Khi cho X tác dụng với KOH thì nKOH = n -COO = 0,39mol
- BTKL: mZ = mX + 56nKOH - mancol = 32,46(g)
Muối gồm có : n A(COOK)2 = 0,15 mol và BCOOK = 0,09 mol
- m muối= 0,15.(A+166) + 0,09. (B+83) = 32,64 g
- 5A + 3B = 3
- A=0 và B= 1 là thỏa
Các muối gồm: HCOOK: x= 7,56g; (COOK)2: y = 24,9 gam
- x :y gần nhất với 0,3
Hai dung dịch nào sau đây đều tác dụng với kim loại Fe?
Hai dung dịch \(CuS{O_4},HCl.\) đều tác dụng với kim loại Fe
Chất nào sau đây không phản ứng với H2 (xúc tác Ni, to )?
Tristearin không phản ứng với H2 (xúc tác Ni, to )
Công thức đơn giản nhất của một hidrocabon là CnH2n+2 Hidrocacbon đó thuộc dãy đồng đẳng của
Ankan có công thức đơn giản nhất của một hidrocabon là CnH2n+2
Có thể dùng NaOH (ở thể rắn) để làm khô các chất khí nào?
Có thể dùng NaOH (ở thể rắn) để làm khô các chất khí \(N{H_3},{O_2},{N_2},C{H_4},{H_2}.\)
Nhỏ vài giọt nước brom vào ống nghiệm chứa anilin, hiện tượng quan sát được là
Nhỏ vài giọt nước brom vào ống nghiệm chứa anilin, hiện tượng quan sát được là có kết tủa màu trắng