Đề thi thử THPT QG năm 2022 môn Hóa học - Trường THPT Xuân Hòa
Đề thi thử THPT QG năm 2022 môn Hóa học - Trường THPT Xuân Hòa
-
Hocon247
-
40 câu hỏi
-
90 phút
-
83 lượt thi
-
Trung bình
Tham gia [ Hs Hocon247.com ] - Cộng Đồng Luyện Thi Trực Tuyến để được học tập những kiến thức bổ ích từ HocOn247.com
Chất nào sau đây có phản ứng trùng hợp?
Chọn D
CH2=C(CH3)COOCH3
Amin nào sau đây chứa nhân benzen trong phân tử?
Chọn B
C6H5NH2
Hợp chất nào sau đây được dùng làm phân đạm?
Chọn D
Các muối dùng làm phân đạm: NH4NO3, NH4Cl, (NH4)2SO4…
Thủy phân tripanmitin trong dung dịch NaOH, thu được glixerol và muối X. Công thức phân tử của X là
Chọn D
(C15H31COO)3C3H5 + 3NaOH → 3C15H31COONa + C3H5(OH)3
Chất nào sau đây dễ bị nhiệt phân khi đun nóng?
Chọn B
Ca(HCO3)2 → CaCO3 + CO2 + H2O
Este nào sau đây có công thức phân tử C4H8O2?
Chọn A
CH3COO-C2H5 hay C4H8O2
Chất nào sau đây là chất điện li mạnh?
Chọn B
NaCl → Na+ + Cl-
Dung dịch NaOH dư tác dụng với chất nào sau đây tạo ra kết tủa có màu trắng hơi xanh?
Chọn C
FeSO4 + 2NaOH → Na2SO4 + Fe(OH)2![]()
Số nguyên tử cacbon trong phân tử saccarozơ là
Chọn D
C12H22O11
Hợp chất nào sau đây có khả năng tham gia phản ứng tráng bạc với dung dịch AgNO3 trong NH3?
Chọn D
HOCH2(CHOH)4CHO+ 2AgNO3 + 3NH3 + H2O →HOCH2(CHOH)4COONH4 + 2Ag + 2NH4NO3
Giải Nobel Hoá học năm 2021 được trao cho 2 nhà khoa học trẻ Benjamin List và David W.C. MacMillan "cho sự phát triển quá trình xúc tác hữu cơ bất đối xứng", mở ra các ứng dụng trong việc xây dựng phân tử. Trong đó Benjamin List đã sử dụng prolin làm xúc tác cho phản ứng cộng andol. Prolin có công thức cấu tạo như sau :
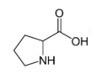
Phát biểu nào sau đây đúng?
Chọn B
Propin: phân tử mạch vòng, hợp chất hữu cơ tạp chức chứa 1 chức -COOH (cacboxyl); 1 chức amin bậc 2 (-NH-) và có CTPT: C5H9NO2
Xà phòng hoá hoàn toàn 4,4 gam este X (C4H8O2) thu được muối Y và dưới 2,3 gam ancol Z. Chất Y là muối của axit cacboxylic nào sau đây?
Chọn D
RCOOR1 + NaOH → RCOONa + R1OH
0,05 0,05 mol
mZ= 0,05.MZ < 2,3 nên MZ < 46 hay Z là CH3OH và X là C2H5COOCH3
nên axit tạo muối Y là C2H5COOH
Phát biểu nào sau đây sai?
Chọn A vì C6H5NH2: ít tan trong nước
Trong phòng thí nghiệm, khí Z (làm mất màu dung dịch thuốc tím) được điều chế từ chất rắn X, dung dịch Y đặc, đun nóng và thu vào bình tam giác bằng phương pháp đẩy không khí như hình vẽ sau:
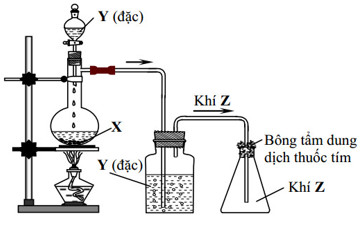
Các chất X, Y, Z lần lượt là
Chọn C
Khí Z nặng hơn không khí và làm mất màu dung dịch KMnO4 nên Z là SO2
Phát biểu nào sau đây đúng?
Trong dung dịch, cation Cu2+ không oxi hóa được Ag.
Chọn A
Insulin là hoocmon của cơ thể có tác dụng điều tiết lượng đường trong máu. Thủy phân một phần insulin thu được heptapeptit (X) mạch hở. Khi thủy phân không hoàn toàn X thu được hỗn hợp các peptit gồm: Ser-His-Leu; Val-Glu-Ala; His-Leu-Val; Gly-Ser-His. Vậy amino axit đầu N và amino axit đầu C trong X lần lượt là
Chọn D
X (heptapeptit) + H2O → Ser-His-Leu + Val-Glu-Ala+ His-Leu-Val+ Gly-Ser-His
CTCT của X là Gly-Ser-His-Leu-Val-Glu-Ala
Đầu N đầu C
Tiến hành thí nghiệm với bốn dung dịch X, Y, Z, T chứa trong các lọ riêng biệt, kết quả được ghi nhận ở bảng sau:
Chọn C
K2CO3 + Ca(OH)2 → CaCO3 ![]() + 2KOH
+ 2KOH
(X) (T)
K2CO3 + 2KHSO4 → 2K2SO4 + CO2 ![]() + H2O
+ H2O
(X) (T)
Ca(HCO3)2 + 2KHSO4 → CaSO4 + K2SO4 + 2CO2![]() + 2H2O
+ 2H2O
(Z) (T)
K2CO3 + Ca(HCO3)2 → CaCO3 ![]() + 2KHCO3
+ 2KHCO3
(X) (Z)
Ca(OH)2 + Ca(HCO3)2 → 2CaCO3 + 2H2O
(T) (Z)
Đốt cháy hoàn toàn x mol hiđrocacbon X (40 < MX < 70) mạch hở, thu được CO2 và 0,3 mol H2O. Mặt khác, cho x mol X tác dụng với AgNO3 dư trong dung dịch NH3, thì có 0,3 mol AgNO3 phản ứng. Sau phản ứng thu được m gam kết tủa. Giá trị của m là
Chọn A
X có dạng (CH\( \equiv \)C)aR và chứa 4C hoặc 5C do 40 < MX < 70 và tạo kết tủa với AgNO3 trong NH3
TH1: a = 1
R-C\( \equiv \)CH + AgNO3 + NH3 → R-C\( \equiv \)CAg + NH4NO3
0,3 0,3 mol
NX = 0,3 = nH2O nên X có 2 nguyên tử H (loại vì C4H2 có 2 nối ba đầu mạch)
TH2: a =2
R(C\( \equiv \)CH)2 + 2AgNO3 + 2NH3 → R(C\( \equiv \)CAg)2+ NH4NO3
0,15 0,3 mol
nên nX = 0,5 mol nên nH2O = 2nX vậy X có 4 nguyên tử H và CTCT của X là
CH\( \equiv \)C-CH2-C\( \equiv \)CH và kết tủa là CAg\( \equiv \)C-CH2-C\( \equiv \)CAg: 0,15 mol
m= 278.0,15 = 41,7 gam
Cho các phát biểu sau:
(a) Poli(vinyl clorua) được dùng làm vật liệu cách điện.
(b) Glucozơ có phản ứng tráng bạc.
(c) Thành phần phân tử của protein luôn có nguyên tố nitơ.
(d) Benzyl axetat có mùi thơm của hoa nhài.
(e) Xenlulozơ có nhiều trong gỗ và bông nõn.
Số phát biểu đúng là
(a) Poli(vinyl clorua) được dùng làm vật liệu cách điện.
(b) Glucozơ có phản ứng tráng bạc.
(c) Thành phần phân tử của protein luôn có nguyên tố nitơ.
(d) Benzyl axetat có mùi thơm của hoa nhài.
(e) Xenlulozơ có nhiều trong gỗ và bông nõn.
Đáp án C
Đốt cháy hoàn toàn 18,54 gam amino axit X mạch hở (phân tử chứa một nhóm -NH2), thu được N2, a mol CO2 và b mol H2O (b > a). Mặt khác, cho 0,15 mol X vào 1 lít dung dịch gồm KOH 0,4M và Ba(OH)2 0,3M, thu được dung dịch Y. Thêm dung dịch HCl dư vào Y, sau phản ứng hoàn toàn cô cạn thu được 113,125 gam chất rắn khan. Giá trị của tổng (a+b) gần nhất với giá trị nào sau đây?
Chọn C
Vì b > a nên X chứa 1 chức -COOH và no, mạch hở
113,125 gam chất rắn gồm: H3N+RCOOH: 0,15 mol; K+: 0,4 mol; Ba2+: 0,3 mol và Cl-: x mol
Vì hỗn hợp rắn trung hoà điện: x = 1,15 mol
113,125 = (17+ R+45).0,15 + 0,4.39 + 0,3.137 + 1,15.35,5 nên R = 42 (C3H6)
X là H2NC3H6COOH
2H2NC3H6COOH → 8CO2 + 9H2O + N2
0,18 0,72 0,81 mol
Nên a + b = 0,72 + 0,81 = 1,53 mol
Theo quy ước, một đơn vị độ cứng ứng với 0,5 milimol Ca2+ hoặc Mg2+ trong 1,0 lít nước. Một loại nước cứng chứa đồng thời các ion Ca2+, HCO3- và Cl-. Để làm mềm 10 lít nước cứng đó cần dùng vừa đủ 100 ml dung dịch chứa NaOH a(M) và Na3PO4 0,2M, thu được nước mềm (không chứa Ca2+) và 6,1 gam kết tủa. Số đơn vị độ cứng có trong nước cứng đó là
Chọn B
Ca2+ + HCO3- + OH- → CaCO3 + H2O và 3Ca2+ + 2PO43- → Ca3(PO4)2 ![]()
x x 0,03 0,02 0,01
nên m kết tủa = 100.x + 310.0,01 = 6,1 nên x = 0,03
CM (Ca2+) = (x+0,03): 10 = (0,03 + 0,03): 10 = 0,006 mol/ lít hay 6 milimol/lít
Số đơn vị độ cứng của nước bằng: 6 : 0,5 = 12
Hiđro hóa hoàn toàn m gam triglixerit X (xúc tác Ni, to) thu được (m + 0,8) gam triglixerit no Y . Đốt cháy hoàn toàn m gam X cần dung vừa đủ 15,5 mol O2, thu được CO2 và 10,2 mol H2O. Mặt khác, thủy phân hoàn toàn m gam X trong dung dịch KOH dư đun nóng, thu được a gam muối. Giá trị của a là
Chọn A
TN1: nH2 = [(m + 0,8)-m]: 2 = 0,4 mol
TN2: X gồm (HCOO)3C3H5: x mol; CH2: y mol và H2: -0,4 mol
X + O2 → CO2 + H2O
15,5 mol 6x+ y 10,2 mol
nên 4x + y-0,4 = 10,2 hay 4x + y = 10,6 (I)
Bảo toàn O: 6x + 15,5.2 = 12x + 2y + 10,2 (II)
Nên x = 0,2 và y = 9,8
TN3: a gam muối gồm: HCOOK: 0,6 mol; CH2: 9,8 mol và H2: -0,4 mol
a=186,8 gam
Cho các phát biểu sau:
(a) Hỗn hợp NaOH và Al2O3 (tỉ lệ mol 3 : 1 tương ứng) tan hết trong nước dư.
(b) Poli(hexametylen ađipamit) được điều chế bằng phản ứng trùng hợp.
(c) Cao su lưu hóa có tính đàn hồi, lâu mòn và khó tan hơn cao su thường.
(d) Cho Mg vào dung dịch FeCl3 dư, luôn thu được Fe.
(e) Hợp kim Cu-Zn để trong không khí ẩm có xảy ra ăn mòn điện hóa.
Số phát biểu đúng là
Chọn B
(a): đúng
(b):sai vì poli (hexametylen ađipamit) được điều chế bằng phản ứng trùng ngưng: H2N(CH2)6NH2 và HOOC(CH2)4COOH
(c ) đúng
(d) sai vì Mg + 2FeCl3 dư → MgCl2 + 2FeCl2
(e) đúng
Tiến hành thí nghiệm điều chế etyl axetat theo các bước sau đây:
- Bước 1: Cho 1 ml C2H5OH, 1 ml CH3COOH và vài giọt dung dịch H2SO4 đặc vào ống nghiệm;
- Bước 2: Lắc đều ống nghiệm, đun cách thủy trong nồi nước nóng khoảng 5 - 6 phút ở 65 - 700C;
- Bước 3: Làm lạnh, sau đó rót 2 ml dung dịch NaCl bão hòa vào ống nghiệm.
Cho các phát biểu sau về các bước thí nghiệm trên:
(a) H2SO4 đặc có vai trò vừa làm chất xúc tác vừa làm tăng hiệu suất tạo sản phẩm;
(b) Mục đích chính của việc thêm dung dịch NaCl bão hòa là để nhận ra sản phẩm este bị tách lớp;
(c) Sau bước 2, trong ống nghiệm vẫn còn C2H5OH và CH3COOH;
(d) Sau bước 3 thu được chất lỏng đồng nhất trong ống nghiệm.
Số phát biểu đúng là
Chọn A
CH3COOH + C2H5OH ⇔ CH3COOC2H5 + H2O
(a): đúng
(b): đúng
(c ) đúng
(d) sai
Nung nóng m gam hỗn hợp gồm Al và Fe3O4 trong điều kiện không có không khí. Sau khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp rắn X. Cho X tác dụng với dung dịch NaOH (dư) thu được dung dịch Y, chất rắn Z và 6,72 lít khí H2 (đktc). Sục khí CO2 (dư) vào dung dịch Y, thu được 46,8 gam kết tủa. Gía trị của m là
Bảo toàn Al:
nAl = nAl(OH)3 = 0,6 mol
Nhiệm vụ của Al
8Al + 3Fe3O4 → 4Al2O3 + 9Fe (1)
0,4 0,15 mol
2Al +2 NaOH + 2H2O → 2NaAlO2 + 3H2 (2)
0,2 0,3 mol
Nên m = 0,6.27 + 0,15.232 = 51,00 gam
Hỗn hợp gồm Fe3O4, Mg và FeCO3. Hòa tan hết 43,20 gam X trong m gam dung dịch chứa HCl 10% và 0,14 mol HNO3, thu được (m + 35,84) gam dung dịch Y và hỗn hợp khí Z (gồm CO2; 4a mol NO và a mol N2) có tỉ khối so với He bằng 9,2. Cho dung dịch AgNO3 đến dư vào dung dịch Y, thu được dung dịch A, 271,12 gam kết tủa và 0,025 mol khí NO (NO là sản phẩm khử duy nhất của N+5). Nồng độ phần trăm của muối Fe(II) trong dung dịch Y là
Bước 1: Tính số mol các khí trong Z
Z gồm CO2: b mol; N2: a mol và NO: 4a mol
mZ= 43,2-35,84 = 7,36 gam hay nZ = 7,36: 36,8 = 0,2 mol
nZ = 5a + b = 0,2 và mZ = 148a + 44b = 7,36 nên a =0,02 và b = 0,1 mol
Bước 2: Tính số mol các chất trong X
Fe3O4
Mg + HCl + HNO3 → H2O + (CO2 + NO + N2) + dd Y(Mg2+, Fe2+, Fe3+, NH4+, H+, Cl- (1)
FeCO3 0,14 0,1 0,08 0,02
Ag+ + Cl- → AgCl ![]() (2)
(2)
3Fe2+ + 4H+ + NO3- → 3Fe3+ + NO + H2O (3)
Ag+ + Fe2+ → Fe3+ + Ag ![]() (4)
(4)
Từ (1): Bảo toàn C: FeCO3: 0,1 mol
Bảo toàn N: NH4+: 0,02 mol
X gồm Fe3O4: a mol; Mg: b mol và FeCO3: 0,1 mol nên 232a + 24b = 43,2 -0,1.116 = 31,6 (I)
Từ (3) thì nH+ trong Y = 0,025.4 = 0,1 mol
Y gồm:
Mg2+: b mol; NH4+: 0,02 mol; H+: 0,1 mol; Fe2+: c mol; Fe3+: (3a+ 0,1-c) mol và Cl-: 9a+2b-c+ 0,42 mol (bảo toàn điện tích)
Nhiệm vụ H+: nHCl + nHNO3 = 8nFe3O4 + 2nCO2 + 4nNO + 12nN2 + 10nNH4+ + nH+ trong Y
nHCl = 8a + 0,2 + 0,32 + 0,24 + 0,2 + 0,1 -0,14 = 8a + 0,92
Bảo toàn Cl: nHCl = nCl- trong Y nên 8a + 0,92 = 9a + 2b - c + 0,42 hay a + 2b - c = 0,5 (II)
Từ (1), (2) và (3) thì kết tủa gồm: AgCl: (8a + 0,92) mol
Ag: (c- 0,075) mol
143,5 (8a + 0,92) + 108 (c-0,075) = 271,12
1148a + 108c = 147,2 (III)
Từ (I), (II) và (III) thi a = 0,1 b= 0,35 c= 0,3
Bước 3: Tính C%
nHCl =8a + 0,92 = 1,72 mol nên mdd axit = 1,72.36,5: 10.100 = 627,8 gam
Bảo toàn khối lượng: mdd Y = 43,2 + 627,8 – 7,36 = 663,64 gam
C%FeCl2 = 0,3.127: 663,64.100 = 5,74%
Xà phòng hoá hoàn toàn m gam hỗn hợp X hai este đơn chức, mạch hở E, F (ME < MF) trong 700 ml dung dịch NaOH 1M, cô cạn hỗn hợp sau phản ứng thu được hỗn hợp Y (gồm 2 ancol là đồng đẳng liên tiếp) và 41,6 gam chất rắn Z. Nung toàn bộ chất rắn Z với CaO cho đến khi phản ứng xảy ra hoàn toàn, thu được 6,72 lít hỗn hợp khí T (đktc). Đun nóng hỗn hợp Y với H2SO4 đặc ở nhiệt độ thích hợp thu được H2O và hỗn hợp A gồm ancol dư, anken và 0,08 mol 3 ete (có khối lượng 6,48 gam). Đốt cháy hết A cần dung vừa đủ 1,35 mol khí O2. Phần trăm khối lượng chất E trong hỗn hợp hai este ban đầu bằng
Chọn C
Bước 1: Tìm 2 ancol và số mol của nó trong Y
Các este: ROR: 0,08 mol hay 6,48 gam nên 0,08 (2R + 16) = 6,48 nên R = 32,5 nên 2 ancol trong Y là C2H5OH và C3H7OH (do là đồng đẳng kế tiếp)
Lượng O2 đốt cháy A bằng lượng O2 đốt cháy Y nên
C2H5OH + 3O2 → 2CO2 + 3H2O (1) và C3H7OH + 4,5O2 → 3CO2 + 4H2O (2)
x mol y mol
nO2 = 3x + 4,5y = 1,35 (a)
TH1: nKhí =nancol = neste = 0,3 mol nên x + y = 0,3 (b)
Từ (a), (b) thì x = 0 và y = 0,3 loại
TH2: n khí = nNaOH = 0,3 mol nên nY = neste = 0,7-0,3 = 0,4 mol
x + y = 0,4 (c)
Từ (a) và (c) thì x = 0,3 và y = 0,1
Y gồm: C2H5OH: 0,3 mol và C3H7OH: 0,1 mol
Bước 2: Tìm 2 este
CTPT của 2 este là RCOOC2H5: 0,3 mol và R1COOC3H7: 0,1 mol
41,6 gam Z gồm: RCOONa: 0,3 mol; R1COONa: 0,1 mol và NaOH: 0,3 mol
Nên 41,6 = 0,3R + 0,1R1 + 0,4.67 + 0,3.40 nên 3R + R1 = 28
Nên R = 1 (H) và R1 = 25 (C2H-)
E là HCOOC2H5 : 0,3 mol và F : C2HCOOC3H7 : 0,1 mol
%E = 66,47%
Tiến hành điều chế Fe(OH)2 theo các bước sau:
- Bước 1: Cho đinh sắt đã đánh thật sạch vào ống nghiệm (1). Cho 3 – 4 ml dung dịch HCl loãng vào, đun nóng nhẹ.
- Bước 2: Đun sôi 4 – 5 ml dung dịch NaOH trong ống nghiệm (2).
- Bước 3: Rót nhanh 2 – 3 ml dung dịch thu được ở bước 1 vào dung dịch NaOH, ghi nhận ngay màu kết tủa quan sát được.
- Bước 4: Ghi nhận màu kết tủa quan sát được sau 2 – 3h thí nghiệm.
Cho các phát biểu sau:
(a) Sau bước 1, thu được chất khí không màu và dung dịch có màu vàng nhạt.
(b) Cho 1 ml dung dịch HNO3 vào 1 ml dung dịch thu được ở bước 1, nút ống nghiệm bằng bông tẩm dung dịch NaOH. Sau một thời gian, dung dịch chuyển sang màu vàng nâu và có khí màu vàng lục thoát ra khỏi dung dịch.
(c) Mục đích chính của bước 2 là đẩy khí O2 hòa tan có trong dung dịch NaOH.
(d) Sau bước 3, thu được kết tủa màu trắng hơi xanh.
(e) Ở bước 4, thu được kết tủa màu nâu đỏ.
Số phát biểu đúng là
(a) Sai vì sau bước 1 thu được chất khí không màu (H2) và dung dịch có màu xanh nhạt (màu
của Fe2+).
(b) Sai vì khí thoát ra là NO không màu gặp oxi trong ống nghiệm chuyển sang nâu đỏ
(c) Đúng vì để điều chế được Fe(OH)2 ta phải đẩy lượng khí O2 hòa tan có trong dung dịch NaOH để
tránh hiện tượng Fe(OH)2 bị O2 oxi hóa thành Fe(OH)3.
(d) Đúng, sau bước 3 ta thu được kết tủa màu trắng hơi xanh Fe(OH)2.
(e) Đúng, đến cuối buổi thí nghiệm thì kết tủa Fe(OH)2 có màu trắng xanh sẽ bị O2 trong không khí oxi
hóa thành Fe(OH)3 có màu nâu đỏ.
Cho các phát biểu sau:
(1) Sử dụng xà phòng để giặt quần áo trong nước cứng sẽ làm vải nhanh mục.
(2) Nếu nhỏ dung dịch I2 vào lát cắt của quả chuối xanh thì xuất hiện màu xanh tím.
(3) Khi nấu canh cua, hiện tượng riêu cua nổi lên trên là do sự đông tụ protein.
(4) Một số este có mùi thơm được dùng làm chất tạo hương trong công nghiệp thực phẩm.
(5) Vải làm từ nilon-6,6 kém bền trong nước xà phòng có tính kiềm.
Số phát biểu đúng là
Cả 5 ý đều đúng
Điện phân (điện cực trơ, màng ngăn xốp) dung dịch gồm CuSO4 và NaCl (tỉ lệ mol tương ứng 1 : 3) với cường độ dòng diện 1,34A. Sau thời gian t giờ, thu được dung dịch Y (chứa hai chất tan) có khối lượng giảm 10,375 gam so với dung dịch ban đầu. Cho bột Al dư vào Y, thu được 1,68 lít khí H2 (đktc). Biết các phản ứng xảy ra hoàn toàn, hiệu suất điện phân 100%, bỏ qua sự hòa tan của khí trong nước và sự bay hơi của nước. Giá trị của t là
Dung dịch Y chứa NaOH và Na2SO4.
Đặt số mol của CuSO4 và NaCl lần lượt là x và 3x mol.
Khi cho Al tác dụng với dung dịch Y thì: \({n_{NaOH}} = \frac{2}{3}{n_{{H_2}}} = 0,05\;mol\)
\( \to {n_{N{a_2}S{O_4}}} = \frac{{3x - 0,05}}{2}\) mà \({n_{N{a_2}S{O_4}}} = {n_{CuS{O_4}}} = x \Rightarrow x = 0,05\;mol\)
Tại catot thu được Cu (0,05) và H2 (a) còn tại anot thu được khí Cl2 (0,075) và O2 (b).
Ta có:
\(\left\{ \begin{array}{l}
2.0,05 + 2a = 0,075.2 + 4b\\
64.0,05 + 2a + 0,075.71 + 32b = 10,375
\end{array} \right. \Rightarrow \left\{ \begin{array}{l}
a = 0,125\\
b = 0,05
\end{array} \right. \Rightarrow {n_e} = 0,35\;mol \Rightarrow t = 7h\)
Nhiệt phân hoàn toàn 14,175 gam một muối khan X, thu được chất rắn Y và hỗn hợp khí Z. Hấp thụ hết Z vào 200 ml dung dịch KOH 1M, thu được dung dịch T, cô cạn T thu được 17,95 gam chất rắn khan. Biết các phản ứng xảy ra hoàn toàn. Phần trăm khối lượng của kim loại trong X là
\({n_{N{O_2}}} = {n_{HN{O_3}}} = x(mol) \to {m_{HN{O_3}}} + {m_{KOH}} = {m_{CR}} + {m_{{H_2}O}}\)
Vì KOH dư nên
\(\begin{array}{l}
{n_{{H_2}O}} = {n_{HN{O_3}}} = x(mol) \to 63x + 0,2.56 = 17,95 + 18x \to x = 0,15(mol)\\
\to n_{NO_3^ - }^{trong X} = {n_{N{O_2}}} = 0,15(mol) \to \% m_{NO_3^ - }^{trong X} = \frac{{0,15.62}}{{14,175}}.100\% = 65,61\% \\
\to \% {m_{KL}} = 34,39\%
\end{array}\)
Nung nóng hỗn hợp X gồm metan, etilen, propin, vinyl axetilen và a mol H2 có Ni xúc tác (chỉ xảy ra phản ứng cộng H2) thu được 0,2 mol hỗn hợp Y (gồm các hiđrocacbon) có tỉ khối so với H2 là 14,5. Biết 0,2 mol Y phản ứng tối đa với 0,1 mol Br2 trong dung dịch. Giá trị của a là
* Xét phản ứng của Y và Br2:
nY = 0,2 mol; nBr2 = 0,1 mol.
Đặt CT trung bình của Y là CnH2n+2-2k.
CnH2n+2-2k + kBr2 → CnH2n+2-2kBr2k
0,2 → 0,2k (mol)
Mà nBr2 = 0,2k = 0,1 → k = 0,5.
Do MY = 14,5.MH2 = 29 nên 14n + 2 - 2k = 29 → n = 2.
→ CT trung bình của Y: C2H5.
* Do các hiđrocacbon trong X đều có 4H và phản ứng cộng không làm thay đổi số C
⟹ CT trung bình của X: C2H4.
* Xét phản ứng X + H2 (a mol):
C2H4 + 0,5H2 → C2H5
0,1 ← 0,2 (mol)
Vậy a = 0,1 mol.
Cho sơ đồ chuyển hoá sau: Mg → X → MgO
Cho các chất: (1) Mg(OH)2 ; (2) MgCO3; (3) Mg(NO3)2 ; (4) MgSO4; (5) MgS
X có thể là những chất nào ?
(2) không được vì từ Mg không ra được MgCO3
(4) không được vì từ MgSO4 không ra được MgO
Cho các phát biểu:
(a) Các nguyên tố ở nhóm IA đều là kim loại.
(b) Tính dẫn điện của kim loại giảm dần theo thứ tự: Ag, Cu, Au, Al, Fe.
(c) Kim loại Na khử được ion Cu2+ trong dung dịch thành Cu.
(d) Nhôm bị ăn mòn điện hóa khi cho vào dung dịch chứa Na2SO4 và H2SO4.
(e) Cho Fe vào dung dịch AgNO3 dư, sau phản ứng thu được dung dịch chứa hai muối.
(f) Cho Mg vào dung dịch FeCl3 dư, sau phản ứng thu được Fe.
Số phát biểu đúng là
(a) Sai, H là phi kim, từ Li về cuối là kim loại kiềm.
(c) Sai, Na khử H2O trước.
(d) Sai, Al bị ăn mòn hóa học.
(f) Sai, Mg + FeCl3 dư → \(MgC{l_2} + FeC{l_2}\)
Từ 16,20 tấn xenlulozơ người ta sản xuất được m tấn xenlulozơ trinitrat (biết hiệu suất phản ứng tính theo xenlulozơ là 90%). Giá trị của m là
[C6H7O2(OH)3]n + 3nHNO3 → [C6H7O2(ONO2)3]n + 3nH2O
0,1 0,1
mxenlo trinitrat = 0,1.297.90% = 26,73(tấn)
Cho m gam Fe vào 200 ml dung dịch CuSO4 sau phản ứng thu được (m + 0,32) gam chất rắn gồm hai kim loại. Nồng độ mol của dung dịch CuSO4 ban đầu là
mKL tăng = 0,32(g) = mCu – mFe(pứ) = 64x – 56x → x = 0,04(mol)
CM(CuSO4) = 0,04/0,2 = 0,2(M)
Cho các loại tơ: Tơ visco, tơ tằm, tơ olon, tơ nilon-6, tơ nilon 6,6. Số tơ có chứa nguyên tố N là
Tơ có chứa nguyên tử N gồm: tơ tằm (protein), tơ olon, tơ nilon-6, tơ nilon-6,6
Kim loại sắt không phản ứng được với chất hoặc dung dịch nào sau đây?
Fe không khử được Al2O3
Đốt cháy hoàn toàn m gam hỗn hợp gồm tinh bột, glucozơ và saccarozơ cần 5,376 lít O2(đktc), thu được 3,96 gam nước. Giá trị của m là
nO2 = nCO2 = nC = 0,24(mol)
mhh = mC + mH2O = 0,24.12 + 3,96 = 6,84(g)
Este tác dụng với NaOH, thu được sản phẩm không có khả năng tham gia phản ứng tráng gương
Este thủy phân sản phẩm có khả năng tham gia tráng bạc gồm dạng: HCOOR’ và RCOOCH=CH-R’

