Đề thi thử tốt nghiệp THPT QG môn Hóa năm 2020 - Trường THPT Bình Chiểu
Đề thi thử tốt nghiệp THPT QG môn Hóa năm 2020 - Trường THPT Bình Chiểu
-
Hocon247
-
40 câu hỏi
-
90 phút
-
35 lượt thi
-
Trung bình
Tham gia [ Hs Hocon247.com ] - Cộng Đồng Luyện Thi Trực Tuyến để được học tập những kiến thức bổ ích từ HocOn247.com
Loại than nào có khả năng dẫn điện, được dùng làm điện cực, làm nồi để nấu chảy các hợp kim chịu nhiệt, chế tạo chất bôi trơn, làm bút chì đen?
Đáp án D
Dựa vào: quen thuộc cực điện phân bằng than chì;
ruột bút chì đương nhiên làm từ than chì
⇒ Loại than được nhắc đến là than chì.
Phenol là những hợp chất hữu cơ có nhóm –OH liên kết trực tiếp với nguyên tử cacbon của vòng benzen. Hợp chất thơm nào sau đây không thuộc họ phenol?
Đáp án D
D. C6H5CH2OH có nhóm OH không đính trực tiếp vào vòng benzen
→ đây là ancol benzylic, không thuộc họ phenol.
Tơ tổng hợp X có hình sợi dài, mảnh và giữ nhiệt tốt nên thường được dùng để dệt vải may quần áo ấm hoặc bện thành sợi “len” đan áo rét. Tơ X bền với nhiệt và không bị thủy phân trong môi trường axit và bazơ. Tơ X là
Đáp án A
Tơ X được nhắc đến là tơ nitron (hay còn gọi là tơ olon) được điều chế từ poliacrilonitrin:
Polime thiên nhiên X được sinh ra trong quá trình quang hợp của cây xanh. Ở nhiệt độ thường, X tạo với dung dịch iot hợp chất có màu xanh tím. Polime X là
Đáp án C
Polime X được nhắc đến là tinh bột:
Được sinh ra trong quá trình quang hợp của cây xanh:
\(6nC{O_2}\,\,\,\,\, + \,\,\,\,5n{H_2}O\,\, \to {\left[ {{C_6}{H_{10}}{O_5}} \right]_n}\,\,\,\, + \,\,\,\,6n{O_2} \uparrow \)
Với I2: phân tử tinh bột có tạo mạch ở dạng xoắn có lỗ rỗng (giống như lò xo):
.png)
→ các phân tử iot có thể chui vào và bị hấp phụ, tạo “hợp chất” màu xanh tím.
Phân tử amino axit nào sau đây có hai nhóm amino?
Đáp án A
Cấu tạo phân tử tương ứng của các amino axit:
A. Lysin: H2N–[CH2]4–CH(NH2)COOH.
B. Valin: (CH3)2CHCH(NH2)COOH.
C. Axit glutamic: HOOCCH2CH2CH(NH2)COOH.
D. Alanin: H2NCH(CH3)COOH.
Công thức phân tử của tristearin là
Đáp án A
tristearin có 3 gốc stearat (C17H35COO) kết hợp với gốc hiđrocacbon của glixerol là C3H5
→ công thức của tristearin là (C17H35COO)3C3H5 → CTPT là C57H110O6.
Kim loại nào sau đây được mạ lên sắt để bảo vệ sắt và dùng để chế tạo thép không gỉ (dùng làm thìa, dao, dụng cụ y tế)?
Đáp án C
Cr là kim loại cứng nhất; bền do có lớp màng oxit bảo vệ.
Ion Ca2+ (Z = 20) đóng vai trò thiết yếu trong việc phát triển xương, giúp duy trì hoạt động của cơ bắp, kích thích máu lưu thông, phát tín hiệu cho các tế bào thần kinh, đồng thời điều tiết một số loại hormone. Tổng số proton và electron của ion Ca2+ là
Đáp án C
Z = 20 ⇒ Ca2+ có 20 – 2 = 18 electron.
Số proton không thay đổi là 20 ⇒ ∑(số p + số e) = 20 + 18 = 38.
Muối mỏ chứa nhiều tạp chất nên không dùng làm thực phẩm cho con người. Ở các nước ôn đới, muối mỏ được dải lên các tuyến đường bị phủ băng để làm tan băng. Tác dụng này là do khi muối mỏ tan vào nước đã làm cho nước
Đáp án D
Đơn giản chỉ là muối mỏ làm giảm nhiệt độ đóng băng → nước khó đóng băng hơn thôi.
Thành phần chính của hồng ngọc và saphia (hai loại đá quí thường được sử dụng làm đồ trang sức) là tinh thể oxit nào?
Đáp án B
Thành phần chính của hồng ngọc và saphia (hai loại đá quí thường được sử dụng làm đồ trang sức) là tinh thể oxit Al2O3. Tinh thể này gọi là corinđon trong suốt không màu, lẫn tạp chất Cr2O3 có màu đỏ nên gọi là hồng ngọc (ruby); lẫn TiO2 và Fe3O4 có màu xanh nên gọi là saphia.
.png)
Một số chất vô cơ và hữu cơ như cacbon, photpho, lưu huỳnh, etanol đều bốc cháy khi tiếp xúc với chất nào sau đây?
Đáp án A
Một số chất vô cơ và hữu cơ như cacbon, photpho, lưu huỳnh, etanol đều bốc cháy khi tiếp xúc với CrO3 (crom trioxit). Ví dụ:
3C + 4CrO3 → 3CO2 + 2Cr2O3.
C2H5OH + 4CrO3 → 2CO2 + 3H2O + 2Cr2O3.
Một mẫu nước tự nhiên có chứa các loại ion: Ca2+, Mg2+, . Dung dịch nào sau đây có khả năng làm mất hoàn toàn tính cứng của mẫu nước trên?
Đáp án D
Mẫu nước chứa Ca2+; Mg2+; HCO3– và Cl– là mẫu nước cứng toàn phần.
→ để làm mềm hoàn toàn, cần dùng Na2CO3 bởi vì
Ca2+ + CO32– → CaCO3↓
Mg2+ + CO32– → MgCO3↓.
⇒ Na2CO3 loại bỏ hết các cation Ca2+ và Mg2+ → nước mất tính cứng.
Hòa tan hết m gam bột nhôm kim loại bằng dung dịch HNO3 thu được dung dịch A không chứa muối amoni và 1,12 lít khí N2 duy nhất ở đktc. Giá trị của m là
Đáp án A
Phân tích: Để tính nhanh, ta sử dụng phương trình ion biểu diễn quá trình nhường-nhận e
\({n_{{N_2}}} = \frac{{1,12}}{{22,4}} = 0,05\,mol\)
\(Al \to \,A{l^{3 + }} + 3e\)
\(\begin{array}{l}
2{N^{ + 5}} + 10e \to {N_2}\\
\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,0,5 \leftarrow 0,05
\end{array}\)
Bảo toàn e, ta có: \({n_{Al}} = \frac{{0,5}}{3} \to {m_{Al}} = 4,5\left( {gam} \right)\)
Cho 8,4 gam sắt tác dụng với 6,4 gam lưu huỳnh trong bình chân không sau phản ứng thu được m gam chất rắn. Giá trị của m là
Đáp án C
Phản ứng: Fe + S → FeS.
Giả thiết: nFe = 0,15 mol; nS = 0,2 mol ⇒ Fe hết, S còn dư.
Tuy nhiên, thật chú ý dù chất nào đủ hay dư thì cuối cùng đều trong m gam chất rắn.
Theo đó, m = 8,4 + 6,4 = 14,8 gam.
Trung hoà 10,62 gam một amin đơn chức X với dung dịch HNO3 vừa đủ, thu được 25,488 gam muối. Công thức phân tử của X là
Đáp án D
Giải: Đặt CT của amin đơn chức có dạng R–NH2
TA có phản ứng: R–NH2 + HNO3 → R–NH3NO3.
+ Bảo toàn khối lượng ⇒ mHNO3 pứ = 25,488 – 10,62 = 14,868 gam
⇒ nHCl==NO3 pứ = 0,236 mol = nAmin đơn chức
⇒ MAmin = MRNH2 = \(\frac{{10,62}}{{0,236}}\) = 45 ⇔ R = C2H5–
⇒ X có CTPT là C2H7N ⇒ Chọn D
Lên men m gam glucozơ thành ancol etylic với hiệu suất 50%, thu được 9,2 gam ancol etylic. Giá trị của m là
Đáp án B
Giải: m = 9,2 ÷ 46 ÷ 2 ÷ 0,5 × 180 = 36 gam ⇒ chọn B.
Quá trình nào sau đây xảy ra phản ứng khâu mạch polime?
Đáp án A
phản ứng lưu hóa cao su thiên nhiên tạo ra các cầu nối –S–S–
giữa các phân tử polime thành mạng lưới không gian (khâu mạch polime);
xảy ra ở nhiệt độ khoảng 150oC, cấu trúc tại mắt xích có cầu nối như sau:
.png)
Phát biểu nào sau đây là sai?
Đáp án B
Xem xét - phân tích các phát biểu:
A. đúng, các amino axit có tính chất lưỡng tính.
B. sai vì cả alanin (H2NCH(CH3)COOH) và anilin (C6H5NH2) đều không làm quỳ tím đổi màu.
C. đúng.
D. đúng.
Đưa một muôi đồng đựng dây Mg đang cháy vào bình đựng đầy khí CO2 thì có hiện tượng gì xảy ra ?
Đáp án C
Dây Mg cháy sáng mãnh liệt do:
2Mg + CO2 → 2MgO + C.
→ Thật chú ý: không dùng CO2 để dập tắt đám cháy kim loại.
Metyl acrylat không tác dụng được với chất nào sau đây?
Đáp án A
Vì CH2=CH–COOCH3 không chứa H linh động như ancol và axit cacboxylic
⇒ Metyl acrylat không thể tác dụng với kim loại Na
Cho hình vẽ mô tả thí nghiệm điều chế và thu khí T bằng phương pháp dời nước:
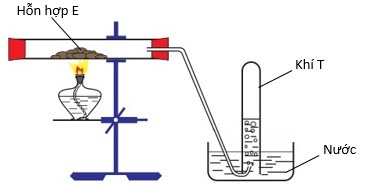
Hỗn hợp nào sau đây không phù hợp với E?
Đáp án C
T thu được bằng phương pháp dời nước
→ Yêu cầu: khí T không tan hoặc tan rất ít trong nước.
Tiến hành các thí nghiệm ở 4 đáp án thì:
Thí nghiệm A, B điều chế khí O2 → thỏa mãn.
Thí nghiệm D điều chế CH4 bằng phản ứng vôi tôi xút cũng thỏa mãn:
CH3COONa + NaOH CH4↑ + Na2CO3.
Thí nghiệm C điều chế NH3:
Ca(OH)2 + NH4Cl → CaCl2 + 2NH3↑ + H2O.
Thí nghiệm hóa học nào sau đây không sinh ra chất rắn (hoặc kết tủa)?
Đáp án D
Các phản ứng hóa học xảy ra khi tiến hành các thí nghiệm hóa học:
A. 2NaOH + Ca(HCO3)2 → CaCO3↓ + Na2CO3 + 2H2O.
B. 2Na + 2H2O → 2NaOH + H2↑
sau đó: CuCl2 + 2NaOH → Cu(OH)2↓ + 2NaCl.
C. Cu + 2AgNO3 → Cu(NO3)2 + 2Ag↓.
D. Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4.
Phương trình hóa học nào sau đây được viết sai?
Đáp án C
HCl không phản ứng được với SiO2.
Nếu thay HCl bằng HF thì mới có phản ứng xảy ra:
SiO2 + 4HF → SiF4 + 2H2O. (phản ứng khắc thủy tinh)
Hợp chất CF2Cl2 thuộc nhóm freon được sử dụng là chất làm lạnh trong các máy lạnh, tủ lạnh. Tuy nhiên, đối với môi trường, freon là tác nhân chính gây
Đáp án A
Các hợp chất dạng CFC dưới tác dụng của tia cực tím UV
→ phân rã quang liên kết C-Cl: CCl2F2 → Cl• + CClF2
clo nguyên tử Cl•, hoạt động rất khác với clo phân tử (Cl2).
gốc Cl• tồn tại lâu dài ở tầng thượng khí quyển,
nơi nó xúc tác việc chuyển đổi ozon thành O2.
→ mỗi gốc Cl• phá hủy hàng ngìn, chục ngìn O3 → gây thủng tầng ozon.
Cho các phát biểu sau:
(a) Trong công nghiệp, một lượng lớn chất béo dùng để sản xuất xà phòng.
(b) Este có nhiệt độ sôi thấp hơn so với ancol có cùng phân tử khối.
(c) Phân tử peptit mạch hở luôn có số nguyên tử N bằng số liên kết peptit.
(d) Nhựa novolac và thủy tinh plexiglas đều thuộc loại chất dẻo.
(e) Trùng hợp buta-1,3-đien và isopren đều thu được polime có tính đàn hồi.
Số phát biểu đúng là
Đáp án D
Xem xét - phân tích các phát biểu:
(a) đúng. Thủy phân chất béo trong môi trường kiềm dùng để sản xuất xà phòng và glixerol.
(b) đúng. Ancol có thể tạo được liên kết hiđro liên phân tử, còn este thì không nên ancol có nhiệt độ sôi cao hơn so với este tương đương.
(c) sai. ví dụ Lys-Val thì chỉ có 1 liên kết peptit nhưng số nguyên tử N lại là 3.
(d) đúng. nhựa dẻo, thủy tinh hữu cơ dẻo
(e) đúng. Trùng hợp buta-1,3-đien và isopren thu được cao su có tính đàn hồi.
→ có 4 phát biểu đúng.
Đốt cháy hoàn toàn 1,84 gam hỗn hợp gồm metan, axetilen và butan bằng khí O2. Hấp thụ toàn bộ sản phẩm cháy vào bình đựng dung dịch Ca(OH)2 dư, tạo thành m gam kết tủa, đồng thời khối lượng phần dung dịch giảm 4,76 gam so với ban đầu. Giá trị của m là
Đáp án C
Thuần đốt cháy ⇒ nhìn hỗn hợp hiđrocacbon gồm a mol C + b mol H2.
Đốt cháy 1,84 gam hỗn hợp + O2 a mol CO2 + b mol H2O.
Ca(OH)2 dùng dư ⇒ Δmdung dịch giảm = mCaCO3↓ – ∑(mCO2 + mH2O)
→ rút gọn, thay số và ẩn có 100a – (44a + 18b) = 4,76 ⇥ 56a – 18b = 4,76.
Lại có 12a + 2b = mhỗn hợp = 1,84 ⇒ giải: a = 0,13; b = 0,14.
→ tương ứng m gam kết tủa là 0,13 mol CaCO3 → m = 13,0 gam.
Từ hợp chất X (C9H8O4, chứa vòng benzen) tiến hành các phản ứng sau (hệ số trong phương trình biểu thị đúng tỉ lệ mol phản ứng):
\(\begin{array}{l}
X\,\,\,\,\, + \,\,\,\,\,NaOH\,\,\, \to \,\,\,\,\,Y\,\,\,\,\, + \,\,\,\,\,Y\\
Y\,\,\,\,\, + \,\,\,\,\,{H_2}S{O_4}\,\,\,\, \to \,\,\,T\,\,\,\,\, + \,\,\,\,\,N{a_2}S{O_4}\\
T\,\,\,\,\, + \,\,\,\,\,{C_2}{H_5}OH\,\,\, \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over
{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} \,\,\,\,\,G\left( {{C_9}{H_{10}}{O_3}} \right)\,\,\,\,\, + \,\,\,\,{H_2}O
\end{array}\)
Phát biểu nào sau đây là sai?
Đáp án B
Hệ số trong phương trình biểu thị đúng tỉ lệ mol phản ứng
→ từ phản ứng (c) ⇒ công thức phân tử của T là C7H6O3
Biết T ⇒ từ phản ứng (b) tính ra công thức của Y là C7H4O3Na2 (☑ D đúng).
Biết Y ⇒ từ phản ứng (a) có công thức của Z là C2H3O2Na
→ cấu tạo của Z là CH3COONa (→ vôi tôi xút Z → CH4 nên ☑ C đúng).
→ Để ý hệ số H2O là 2 ⇒ 1H2O sinh ra do este phenol CH3COOC6
⇒ còn 1H2O nữa là do chức axit COOH ⇒ X là CH3COOC6H4COOH.
→ Vậy, phân tử X chứa một nhóm chức este (A đúng) ⇒ chỉ có B sai vì:
Cấu tạo G là HOC6H4COOC2H5 tác dụng NaOH dư theo tỉ lệ 1 : 2.
HOC6H4COOC2H5 + 2NaOH → NaOC6H4COONa + C2H5ONa.
Cho từ từ dung dịch HCl vào dung dịch chứa a mol Ba(AlO2)2 và b mol Ba(OH)2. Kết quả thí nghiệm được biểu diễn trên đồ thị sau:
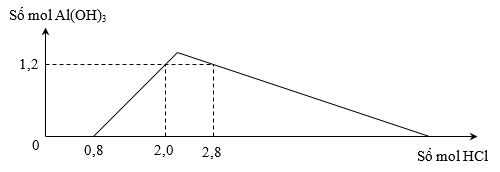
Tỉ lệ a : b là
Đáp án A
Đồ thị biểu diễn số mol kết tủa Al(OH)3 theo số mol HCl:
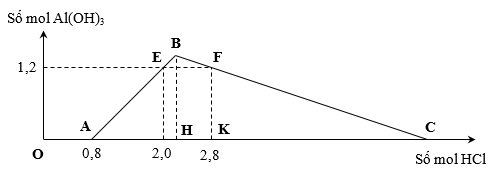
Tại A, phản ứng trung hòa Ba(OH)2 + 2HCl → BaCl2 + 2H2O
xảy ra vừa xong ⇒ b = nBa(OH)2 = ½.nHCl tại A = 0,4 mol.
CK = 3KF = 3,6 ⇒ AC = AK + CK = (2,8 – 0,8) + 3,6 = 5,6
→ BH = AC ÷ 4 = 1,4 ⇒ a = nBa(AlO2) = 1,4 ÷ 2 = 0,7 (bảo toàn Al).
Vậy, yêu cầu a : b = 0,7 ÷ 0,4 = 7 : 4.
Cho E là dung dịch chứa a mol Na2CO3 và T là dung dịch chứa b mol HCl. Nhỏ từ từ đến hết E vào T, thu được 2V lít khí CO2. Nếu nhỏ từ từ đến hết T vào E, thu được V lít khí CO2. Các thể tích khí đo ở cùng điều kiện nhiệt độ, áp suất. Tỉ lệ a : b tương ứng là
Đáp án C
Các thể tích khí đo ở cùng điều kiện nhiệt độ, áp suất → chọn giá trị V tương ứng với 1 mol khí.
Cho từ từ HCl vào dung dịch Na2CO3 xảy ra lần lượt các phản ứng sau:
\(\begin{array}{l}
\begin{array}{*{20}{l}}
{{\rm{N}}{{\rm{a}}_2}{\rm{C}}{{\rm{O}}_3}{\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\rm{ + }}\;\;{\rm{HCl}} \to {\rm{NaHC}}{{\rm{O}}_3}{\rm{ + }}\;{\rm{NaCl}}}\\
{{\mkern 1mu} {\mkern 1mu} {\rm{a b b}}}
\end{array}\\
\begin{array}{*{20}{l}}
{{\rm{NaHC}}{{\rm{O}}_{\rm{3}}}\;{\rm{ + }}\;\;{\rm{HCl}} \to {\rm{NaCl}}\;\;{\rm{ + }}\;{\rm{C}}{{\rm{O}}_2}{\mkern 1mu} {\mkern 1mu} + {\mkern 1mu} {\mkern 1mu} {{\rm{H}}_{\rm{2}}}{\rm{O}}}\\
{{\mkern 1mu} {\mkern 1mu} {\rm{b }}\left( {{\rm{b}} - {\rm{a}}} \right)\,\,\,\,\,\,\left( {{\rm{b}} - {\rm{a}}} \right)}
\end{array}
\end{array}\)
Giả thiết thu được 1 mol CO2 và rõ b – a < b nên b – a = 1.
Cho ngược lại Na2CO3 từ từ vào dung dịch HCl → phản ứng tạo khí luôn:
\(\begin{array}{*{20}{l}}
{{\rm{N}}{{\rm{a}}_2}{\rm{C}}{{\rm{O}}_3}\;{\rm{ + }}\;\;{\rm{2HCl}} \to {\rm{C}}{{\rm{O}}_2}\;{\rm{ + }}\;\;{\rm{2NaCl}}{\mkern 1mu} {\mkern 1mu} {\rm{ + }}{\mkern 1mu} {{\rm{H}}_2}{\rm{O}}.}\\
{{\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\rm{a b }}?}
\end{array}\)
Nếu 2a < b → số mol CO2 tính theo Na2CO3 → a = 2 thay lại có b = 3 không thỏa mãn.
Nếu 2a > b → số mol CO2 tính theo HCl → b = 4. Thay lại có a = 3 → a : b = 3 : 4.
Thực hiện các thí nghiệm sau:
(a) Đun đến sôi nước có tính cứng toàn phần.
(b) Hòa tan phèn chua vào nước rồi thêm dung dịch NH3 dư.
(c) Cho dung dịch NaOH vào dung dịch AlCl3 dư.
(d) Cho mẩu nhỏ Na vào dung dịch gồm CaCl2 và NaHCO3.
(e) Cho nước vôi trong vào dung dịch NaHCO3.
(g) Cho dung dịch H2SO4 dư vào dung dịch Ba(AlO2)2.
Sau khi kết thúc các phản ứng, số thí nghiệm thu được kết tủa là
Đáp án C
Các phản ứng xảy ra ki tiến hành các thí nghiệm:
(a) nước cứng toàn phần có chứa Ca2+ và HCO3 nên khi đun nóng
Ca(HCO3)2 → CaCO3↓ + CO2 + H2O.
(b) phèn chua: K2SO4.Al2(SO4)3.24H2O ⇒ hòa tan thu được Al2(SO4)3.
Al2(SO4)3 + 6NH3 + 6H2O → 2Al(OH)3↓ + 3(NH4)2SO4.
(c) AlCl3 (dùng dư) + 3NaOH → Al(OH)3↓ + 3NaCl.
(d) Na + H2O → NaOH + ½.H2↑
OH– + HCO3– → CO32– + H2O.
sau đó: Ca2+ + CO32– → CaCO3↓.
(e) Ca(OH)2 + NaHCO3 → CaCO3↓ + NaOH + H2O.
(g) 4H2SO4 dư + Ba(AlO2)2 → BaSO4↓ + Al2(SO4)3 + 4H2O.
→ Cả 6 thí nghiệm đều thu được kết tủa.
Thực hiện phản ứng este hóa m gam hỗn hợp X gồm etanol và axit axetic (xúc tác H2SO4 đặc) với hiệu suất phản ứng đạt 80%, thu được 7,04 gam etyl axetat. Mặt khác, cho m gam X tác dụng với NaHCO3 dư, thu được 3,36 lít khí CO2 (đktc). Giá trị của m là
Đáp án A
Phản ứng: CH3COOH + NaHCO3 → CH3COONa + CO2↑ + H2O.
Chỉ có axit axetic trong X phản ứng tạo 0,15 mol CO2 ⇒ số mol axit là 0,15 mol.
Phản ứng este hóa: CH3COOH + C2H5OH ⇄ CH3COOC2H5 + H2O.
Nhận xét: neste = 0,08 mol; naxit tham gia = 0,15 mol
⇥ Hiệu suất phản ứng là 80% tính theo số mol ancol
→ nancol = 0,08 : 0,8 = 0,1 mol.
Vậy, giá trị của m = 0,1 × 46 + 0,15 × 60 = 13,6 gam.
Cho sơ đồ phản ứng sau:
(NH4)2Cr2O7 → X (+ dung dịch HCl, to) → Y ( + Cl2 + dung dịch KOH dư) → Z ( + dung dịch H2SO4 loãng) → T
Trong đó X, Y, Z, T đều là các hợp chất khác nhau của crom. Chất T là
Đáp án D
Các phản ứng xảy ra theo dãy điện hóa:
(NH4)2Cr2O7 → N2 + Cr2O3 (X) + 4H2O.
Cr2O3 + 6HCl → 2CrCl3 (Y) + 3H2O.
CrCl3 + 3Cl2 + 8KOH → K2CrO4 (Z) + 6KCl + 4H2O.
2K2CrO4 + H2SO4 → K2Cr2O7 (T) + K2SO4 + H2O.
Hỗn hợp H gồm 3 peptit X, Y, Z (MX < MY) đều mạch hở; Y và Z là đồng phân của nhau. Cho m gam hỗn hợp H tác dụng vừa đủ với dung dịch chứa 0,98 mol NaOH, cô cạn dung dịch sau phản ứng thu được 112,14 gam muối khan (chỉ chứa muối natri của alanin và valin). Biết trong m gam H có mO : mN = 552 : 343 và tổng số liên kết peptit trong 3 peptit bằng 9. Tổng số nguyên tử có trong peptit Z là
Bảo toàn nguyên tố , Qui đổi.
- Khi đốt hỗn hợp H thì :
nN (trong H) = nValNa + nAlaNa = nNaOH = 0,98
→ nO ( trong H) = (551.14nN) : (16.343) = 1,38
+ Quy đổi hỗn hợp H thành C2H3ON, CH2, H2O
Gọi kX, kY, kZ là số mắt xích của peptit X, Y và Z
Ta có:
K = 2,45
Trong H có chứa đipeptít
+ Mà Y và Z là đồng phân → Y, Z có cùng số mắt xích
Mặt khác kX + kY + kZ = 9 + 3 → ky = kz = 5
→ X là (Ala)2 ; Y và Z là (Val)2(Ala)3
→ Số nguyên tử trong Y hoặc Z là 65.
Chọn A.
Cho dãy các chất: CH3COOH3NCH3, H2NCH2COONa, H2NCH2CONHCH2-COOH, ClH3NCH2COOH, saccarozơ và glyxin. Số chất trong dãy vừa tác dụng với NaOH, vừa tác dụng với dung dịch HCl là
Số chất trong dãy vừa tác dụng với NaOH, vừa tác dụng với dung dịch HCl gồm: CH3COOH3NCH3 , H2NCH2CONHCH2-COOH và glyxin ⇒ Chọn B
Thực hiện các thí nghiệm sau ở điều kiện thường:
(a) Sục khí H2SO4 vào dung dịch NaOH.
(b) Cho NaCl vào dung dịch KNO3.
(c) Cho Na2CO3 vào dung dịch HCl.
(d) Cho dung dịch CuSO4 vào dung dịch Ba(OH)2.
Số thí nghiệm xảy ra phản ứng là:
Đáp án B
Kết quả thí nghiệm của các dung dịch X, Y, Z, T với các thuốc thử được ghi lại trong bảng sau:
Đáp án A
Các chất rắn: tristearin, glucozơ, phenol, axit ađipic được kí hiệu ngẫu nhiên là X, Y, Z, T. Một kết quả thí nghiệm được ghi ở bảng sau.
Đáp án C
Một số hiện tượng dễ nhận ra và suy luận:
chỉ có glucozơ có khả năng phản ứng tráng bạc → Ag↓ ⇒ T là glucozơ.
Chỉ có axit ađipic làm quỳ tím ẩm hóa đỏ ⇒ Y là axit ađipic.
đáp án đúng là C. tương ứng cho biết Z là tristearin và X là phenol.
Phân tích thêm: chất béo không tan trong nước nóng, nhẹ hơn nên nổi lên.
Đổi lại, nếu là phenol thì sẽ tan được trong nước nóng.

