Đề thi thử THPT QG môn Hóa học năm 2018 - Trường THPT Chuyên Lam Sơn - Thanh Hóa
Đề thi thử THPT QG môn Hóa học năm 2018 - Trường THPT Chuyên Lam Sơn - Thanh Hóa
-
Hocon247
-
40 câu hỏi
-
90 phút
-
59 lượt thi
-
Trung bình
Tham gia [ Hs Hocon247.com ] - Cộng Đồng Luyện Thi Trực Tuyến để được học tập những kiến thức bổ ích từ HocOn247.com
Phân tử polime nào sau đây chỉ chứa 3 nguyên tố C, H, N trong phân tử?
- Poli(vinyl clorua) là (-CH2-CHCl-)n chứa C, H, Cl
- Poli(vinyl axetat) là (-CH2-CH(OOCCH3)-)n chứa C, H, O
- Polietilen là (-CH2-CH2-)n chứa C, H
- Poliacrilonitrin là (-CH2-CHCN-)n chứa C, H, N
Trong hóa học vô cơ, phản ứng nào sau đây thuộc loại phản ứng oxi hóa - khử?
Trong hóa học vô cơ, phản ứng thuộc loại phản ứng oxi hóa - khử là
4NO2 + O2 + 2H2O → 4HNO3
Công thức nào sau đây có thể là công thức của chất béo
Chất béo là trieste của glixerol và các axit béo ( từ 12 Cacbon trở lên)
Polime nào sau đây được điều chế bằng phản ứng trùng ngưng?
Poli(etylen terephtalat) được điều chế phản ứng trùng ngưng etylenglicol và axit terephtalic.
PTHH: \(nHOC{H_2}C{H_2}OH + nHOOC{C_6}{H_4}COOH\xrightarrow{{{t^o}}}{( - OC{H_2}C{H_2}O - OOC{C_6}{H_4}COO - )_n} + 2n{H_2}O\)
Đáp án A
Để tác dụng hết a mol triolein cần dùng tối đa 0,6 mol Br2 trong dung dịch. Giá trị của a bằng.
Ta có: mỗi gốc oleat có 1 nối đôi C=C trong gốc hidrocacbon nên triolein có 3 nối đôi C=C
→ 1 mol (C17H33COO)3C3H5 phản ứng vừa đủ với 3 mol Br2 nên ntriolein= 0,2
Dần V lít khí CO (đktc) qua ống sứ đựng lượng dư CuO nung nóng. Sau khi phản ứng hoàn toàn, khối lượng chất rắn giảm 4,0 gam so với ban đầu. Giá trị của V là
Khối lượng rắn giảm = khối lượng oxi trong CuO phản ứng
nO = 4: 16 = 0,25 (mol)
→ nCO = nO = 0,25( mol) → VCO = 0,25.22,4 = 5,6 (lít)
Dung dịch HNO3 0,1M có pH bằng
[H+] = 0,1M → pH = - log[H+] = - log[0,1] = 1
Hòa tan hết m gam chất rắn X gồm CaCO3 và KHCO3 vào dung dịch HCl dư thu được 4,48 lít khí CO2 ở đktc. Giá trị của m bằng
nCO2 = 4,48 : 22,4 = 0,2 (mol)
→ nX = nCO2 = 0,2 (mol) → m = 0,2.100 = 20 (gam)
Đốt cháy hết 4,5 gam đimetylamin thu được sản phẩm gồm N2, H2O và a mol khí CO2. Giá trị của a bằng:
n(CH3)2NH = 4,5 : 45 = 0,1 (mol)
→ nCO2 = 2 n(CH3)2NH = 2. 0,1 = 0,2 (mol)
Trong phân tử Gly-Ala-Val-Phe, amino axit đầu N là
Đọc từ trái sang thì amino axit đầu tiên là đầu N và cuối cùng là đầu C
→ amino axit đầu N là Gly ⇒ chọn D
Cho dung dịch FeCl3 vào dung dịch chất X, thu được kết tủa Fe(OH)3. Chất X là:
3KOH + FeCl3 → 3KCl + Fe(OH)3↓
Thực hiện phản ứng để hiđrat hóa ancol etylic thu được anken X. Tên gọi của X là:
C2H5OH → C2H4 + H2O
Fomalin (còn gọi là fomon) được dùng đẻ ngâm xác động, thực vật, thuộc da, tẩy uế, diệt trùng... Fomalin là dung dịch của chất hữu cơ nào sau đây?
Fomalin là dung dịch HCHO có nồng độ 37-40%
Đáp án A
Số đồng phân cấu tạo của anken C4H8 là:
Đồng phân cấu tạo anken : CH2=CH-CH2-CH3 ; CH3-CH=CH-CH3 ; CH2=C(CH3)2
Phát biểu nào sau đây là sai?
Đường saccarozo còn gọi là đường nho → Sai
Đáp án B
Hấp thụ hết 5,6 lít khí CO2 ở đktc vào dung dịch gồm 0,15 mol BaCl2; 0,08 mol Ba(OH)2 và 0,29 mol KOH sau phản ứng hoàn toàn thu đuợc dung dịch A và m gam kết tủa. Giá trị của m bằng
\(\begin{gathered}
C{O_2}:0,25mol + \left\{ \begin{gathered}
B{a^{2 + }}:0,23mol \hfill \\
O{H^ - }:0,45mol \hfill \\
\end{gathered} \right. \hfill \\
*\, = \frac{{{n_{O{H^ - }}}}}{{{n_{C{O_2}}}}} = 1,8 \Rightarrow {n_{C{O_3}^{2 - }}} = {n_{O{H^ - }}} - {n_{C{O_2}}} = 0,2mol \hfill \\
B{a^{2 + }} + C{O_3}^{2 - } \to BaC{O_3} \hfill \\
\Rightarrow m = 39,40g \hfill \\
\end{gathered} \)
Phân kali clorua đuợc sản xuất từ quặng sinvinit có chứa 47% K2O về khối lượng. Phần trăm khối lượng KCl có trong phân bón đó bằng
Xét 100 gam phân kali, khối lượng K2O là 47 gam
2KCl → K2O
149 94
y 47
Suy ra
y = (47.2.74,5) : 94 = 74,5
Vậy hàm lượng KCl có trong phân là 74,5%
Phát biểu nào sau đây là đúng?
Thủy phân hoàn toàn chất béo luôn thu được glixerol.
→ Đáp án D
Thủy phân este X (C4H6O2) mạch hở trong môi trường axit thu được hai chất hữu cơ Y và Z. Tỉ khối của Z so với khí H2 là 16. Phát biểu đúng là
Chất Y có khả năng làm mất màu dung dịch Br2.
Đáp án C
Cho 30,45 gam tripeptit mạch hở Gly-Ala-Gly vào dung dịch NaOH dư sau phản ứng hoàn toàn thấy có m gam NaOH. Giá trị của m là
n gly-ala-gly = 30,45 : 203 = 0,15 (mol)
n NaOH = 3 n gly-ala-gly = 3.0,15 = 0,45 (mol)
→ mNaOH = 0,45.40 = 18 (gam)
Hòa tan hỗn hợp gồm K2O, BaO, AI2O3 và MgO vào nước dư sau phản ứng hoàn toàn thu được dung dịch X và chất rắn Y. Sục khí CO2 tới dư vào dung dịch X sau phản ứng thu được kết tủa là:
\(\left\{ \begin{gathered}
{K_2}O \hfill \\
A{l_2}{O_3} \hfill \\
MgO \hfill \\
\end{gathered} \right.\xrightarrow{{ + {H_2}O}}\left\{ \begin{gathered}
KOH \hfill \\
KAl{O_2} \hfill \\
\end{gathered} \right. \to Al{(OH)_3}\)
sục khí CO2 tới dư thu được:
\(C{O_2} + {H_2}O + KAl{O_2} \to KHC{O_3} + Al{(OH)_3} \downarrow \)
Cho sơ đồ sau:
\(MC{O_3} → MO + C{O_2}\)
\(MO + {H_2}O \to M{\left( {OH} \right)_2}\)
\(M{\left( {OH} \right)_{2{\rm{ d}}}} + Ba{\left( {HC{O_3}} \right)_2} \to MC{O_3} + BaC{O_3} + {H_2}O\)
Vậy MCO3 là:
MO tan trong H2O → loại A và B (vì FeO và MgO không tan trong H2O).
Do M(OH)2 + Ba(HCO3)2 → 2 muối cacbonat
→ loại D vì chỉ có BaCO3
⇒ chọn C.
Cho dãy gồm các chất: CH3COOH; C2H5OH; H2NCH2COOH và CH3NH3Cl. số chất trong dãy có khả năng tác dụng với dung dịch NaOH là
Số chất trong dãy có khả năng tác dụng với dung dịch NaOH là:
CH3COOH; H2NCH2COOH và CH3NH3Cl
Có các chất sau: protein; sợi bông; amoni axetat; nhựa novolac; keo dán ure- fomanđehit;tơ capron; tơ lapsan; tơ nilon-6,6. Trong các chất trên có bao nhiêu chất mà trong phân tử của chúng có chứa nhóm -NH-CO-?
Các chất: protein, tơ capron, tơ nilon - 6,6, keo dán ure - fomandehit
X là một hợp chất hữu cơ có dạng: (H2N)xCnHm(COOH)y. Biết rằng 0,2 mol hỗn hợp X tác dụng tối đa với 400 ml dung dịch HCl 1M thu được 38,2 gam muối, số đồng phân cấu tạo của X là
nHCl = 0,4 mol → x = 2
m muối = 38,2 → M muối = 191
→ X: (H2N)2C3H5(COOH)
→ 9CTCT
Hòa tan hết m gam P2O5 vào 400 gam dung dịch KOH 10% dư sau phản ứng hoàn toàn cô cạn dung dịch thu được 3,5m gam chất rắn. Giá trị nào sau đây gần nhất với giá trị m ?
nKOH = (400.10%)/(100%.56) = 5/7 (mol)
Gọi nP2O5 = x (mol) → nH3PO4 = 2x (mol)
KOH dư nên muối thu được là K3PO4 : 2x (mol)
Gọi nKOH dư là y (mol)
Ta có:
142x = m; 212.2x + 65y = 3,5m và 6x + y = 5/7
→ x = 0,09779 → mP2O5 = 142. 0,9779 = 13,88 (gam) ≈ 14(gam)
Cho 36,1 gam hợp chất hữu cơ X (có công thức hóa học C6H9O4Cl) tác dụng với dung dịch NaOH dư khi đun nóng nhẹ sau phản ứng hoàn toàn thu được các sản phẩm gồm: 0,4 mol muối Y; 0,2 mol C2H5OH và x mol NaCl. số nhóm -CH2- trong một phân tử X bằng
\({n_X} = 0,2\) mol ⇒ 1 phân tử X sinh ra 2 phân tử Y và 1 phân tử C2H5OH.
=> X là Cl-CH2-COO-CH2-COOCH2-CH3 ⇒ X chứa 3 nhóm –CH2–.
Hợp chất hữu cơ X có dạng CnHmO. Đốt cháy hết 0,04 mol X bằng 0,34 mol khí O2 thu đuọc 0,44 mol hỗn hợp gồm các khí và hơi. Mặt khác 0,05 mol X tác dụng với luợng dư dung dịch AgNO3 trong NH3 sau phản ứng hoàn toàn thu được khối lượng kết tủa vuợt quá 10,8 gam. số đồng phân cấu tạo của X là:
nCO2 = 0,04n và nH2O = 0,02m → nO2 dư = 0,44 – 0,04n – 0,02m
Bảo toàn O: 0,04 + 0,34.2 = 0,04n.2 + 0,02m + 2(0,44 – 0,04n – 0,02m)
→ m = 8 → X là CnH8O
nO2 dư = 0,44 – 0,04n – 0,02m ≥ 0 → n ≤ 7
Khi nX = 0,05 thì m rắn > 10,8 nên X không thể là andehit no, đơn chức.
Vậy X là andehit có nối 3 đầu mạch.
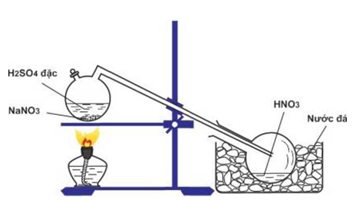
Cho hình vẽ mô tả thí nghiệm điều chế HNO3 trong phòng thí nghiệm như sau:
Hình. Điều chế HNO3 trong phòng thí nghiệm
Phát biểu không đúng về quá trình điều chế là
A sai vì HCl cũng là axit dễ bay hơi giống HNO3 nên không thể dùng để điều chế HNO3 thay cho H2SO4 được.
Cho hỗn hợp khí X gồm HCHO, C2H2 và H2 đi qua ống sứ đựng bột Ni nung nóng. Sau một thời gian thu đuợc hỗn hợp Y (gồm khí và hơi). Đốt cháy hoàn toàn Y cần dùng vừa đủ 0,25 mol O2, sinh ra 0,15 mol CO2 và 4,50 gam H2O. Phần trăm khối luợng của C2H2 trong X là
Đốt X cũng như đốt Y. Đặt \({n_{HCHO}} = x;{n_{{C_2}{H_2}}} = y;{n_{{H_2}}} = z\).
\({n_{{O_2}}} = 0,25 = x + 2,5y + 0,5z;{n_{C{O_2}}} = 0,15 = x + 2y;{n_{{H_2}O}} = 0,25 = x + y + z\).
Giải hệ có: \(x = y = 0,05;z = 0,15\). Bảo toàn khối lượng: \({m_X} = 3,1\) (g).
\( \Rightarrow \% {m_{{C_2}{H_2}}} = 0,05 \times 26 \div 3,1 \times 100\% = 41,94\% \)
Cho các phát biểu sau:
(a) Anbunin là protein hình cầu, không tan trong nuớc.
(b) Animoaxit là hợp chất hữu cơ tạp chức.
(c) Saccarozo thuộc loại đisaccarit.
(d) Công thức tổng quát của amin no, mạch hở đơn chức là CnH2n+3N.
(e) Tất cả các peptit đều có phản ứng với Cu(OH)2 tạo hợp chất màu tím.
(f) Trong phân tử tetrapeptit mạch hở có 3 liên kết peptit.
(g) Lực bazơ của metylamin mạnh hơn đimetylamin.
Số phát biểu đúng là
(a) Sai vì anbumin tan trong nước tạo thành dung dịch keo.
(b) Đúng.
(c) Đúng.
(d) Đúng.
(e) Sai vì peptit chứa từ 3 mắt xích trở lên mới có phản ứng màu biure với Cu(OH)2 /OH- .
(f) Đúng.
(g) Sai vì với amin béo (amin no) thì bậc 2 > bậc 1 > bậc 3.
⇒ có 4 ý đúng
⇒ chọn C.
Hỗn hợp X gồm M2CO3, MHCO3 và MCl (M là kim loại kiềm). Cho 32,65 gam X tác dụng vừa đủ với dung dịch HC1 thu đuợc dung dịch Y và có 17,6 gam CO2 thoát ra. Dung dịch Y tác dụng với dung dịch AgNO3 dư đuợc 100,45 gam kết tủa. Phần trăm khối luợng muối MCl trong X gần nhất với giá trị nào sau đây?
Đặt \({n_{{M_2}C{O_3}}} = x;{n_{MHC{O_3}}} = y;{n_{MCl}} = z \Rightarrow {n_{HCl{\rm{ phan ung}}}} = 2x + y$\)
Bảo toàn nguyên tố Clo: \({n_{AgCl}} = 0,7 = 2x + y + z;{n_{C{O_2}}} = 0,4 = x + y\)
\({m_X} = 32,65 = \left( {2M + 60} \right).x + \left( {M + 61} \right).y + \left( {M + 35,5} \right).z\)
\(\Rightarrow 32,65 = M.\left( {2x + y + z} \right) + 60.\left( {x + y} \right) + y + 35,5z\)
\( \Rightarrow 0,7M + y + 35,5z = 8,65 \Rightarrow 0,7M < 8,65 \Rightarrow M < 12,36\)
=> M là Liti => M = 7 giải hệ có: x = y = 0,2 mol; z = 0,1 mol.
\( \Rightarrow \% {m_{MCl}} = 0,1 \times 42,5 \div 32,65 \times 100\% = 13,02\% \).
Cho các thí nghiệm sau:
(1) Sục khí axetilen vào dung dịch AgNO3 trong NH3.
(2) Cho dung dịch KHSO4 dư vào dung dịch Mg(HCO3)2
(3) Oxi hóa metanal bằng dung dịch AgNO3 trong NH3.
(4) Nhỏ vài giọt HNO3 đặc vào lòng trắng trứng (anbumin).
(5) Cho dung dịch KOH dư vào dung dịch FeCl2.
(6) Nhỏ dung dịch Br2 vào ống nghiệm đựng anilin.
Sau phản ứng hoàn toàn, số thí nghiệm thu đuợc kết tủa là
Thí nghiệm thu được kết tủa là: (1), (3),(4),(5),(6)
Hỗn hợp X gồm 2 este đơn chức. Cho 0,6 mol hỗn hợp X tác dụng vừa đủ với dung dịch NaOH sau phản ứng hoàn toàn thu được dung dịch Y. Cô cạn dung dịch Y thu được hỗn hợp Z gồm hai muối khan. Đốt cháy hoàn toàn Z thu được 110 gam CO2, 53 gam Na2CO3 và m gam H2O. Giá trị của m là
Bảo toàn nguyên tố Natri: \({n_{NaOH}} = 2{n_{N{a_2}C{O_3}}} = 1 \Rightarrow {n_{NaOH}}:{n_X} = 1,67\)
 X chứa este của phenol. Đặt \({n_{este}}\) của ancol = x; \({n_{este}}\) của phenol \(= y \Rightarrow {n_X} = x + y = 0,6\) mol.
X chứa este của phenol. Đặt \({n_{este}}\) của ancol = x; \({n_{este}}\) của phenol \(= y \Rightarrow {n_X} = x + y = 0,6\) mol.
\({n_{NaOH}} = x + 2y = 1\) mol. Giải hệ có: x = 0,2 mol; y = 0,4 mol.
Do Z chỉ chứa 2 muối ⇒ Z gồm muối của axit cacboxylic và muối của phenol.
Đặt số C của muối của axit và phenol lần lượt là a và b (a ≥ 1; b ≥ 6).
\(\Rightarrow 0,6a + 0,4b = 2,5 + 0,5\). Giải phương trình nghiệm nguyên có a = 1, b = 6.
=> Z gồm 0,6 mol HCOONa và 0,4 mol C6H5ONa
\(m = \left( {0,6 + 0,4 \times 5} \right) \div 2 \times 18 = 23,4\) (g).
Có các tập chất khí và dung dịch sau:
\((1){\rm{ }}{K^ + },C{a^{2 + }},HCO_3^ - ,O{H^ - }\)
(2) \(F{e^{2 + }},{H^ + },NO_3^ - ,SO_4^{2 - }\)
(3) \(C{u^{2 + }},N{a^ + },NO_3^ - ,SO_4^{2 - }\)
(4) \(B{a^{2 + }},N{a^ + },NO_3^ - ,C{l^ - }\)
(5) \({N_2},C{l_2},N{H_3},{O_2}\)
(6) \(N{H_3},{N_2},HCl,S{O_2}\)
(7) \({K^ + },A{g^ + },NO_3^ - ,PO_4^{3 - }\)
(8) \(C{u^{2 + }},N{a^ + },C{l^ - },O{H^ - }\)
Số tập hợp cùng tồn tại ở nhiệt độ thường là
Số tập hợp tồn tại điều kiện thường là: (3),(4)
Hỗn hợp M chứa ba peptit mạch hở Ala-Gly-Lys, Ala-Gly và Lys-Lys-Ala-Gly-Lys. Trong hỗn hợp M nguyên tố oxi chiếm 21,302% về khối lượng. Cho 0,12 mol M tác dụng với dung dịch HCl dư sau phản ứng hoàn toàn thu được m gam hỗn hợp gồm ba muối. Giá trị của m gần nhất với giá trị nào sau đây?
Đặt CT trung bình của M là GlyAla(Lys)x ⇒ M(M) = 128x + 146; số O = x + 3.
⇒ %mO = 16 × (x + 3) ÷ (128x + 146) × 100% = 21,302% ⇒ x = 1,5.
GlyAla(Lys)1,5 + 5HCl + 2,5H2O → muối ⇒ nHCl = 0,6 mol; nH2O = 0,3 mol.
Bảo toàn khối lượng: m = 0,12 × 338 + 0,6 × 36,5 + 0,3 × 18 = 67,86(g).
Thực hiện phản ứng crackinh X mol butan thu được hỗn hợp X gồm 5 chất đều là hiđrocacbon với hiệu suất phản ứng là 75%. Cho X đi qua bình đựng dung dịch Br2 dư sau phản ứng hoàn toàn thu được hỗn hợp khí Y. Đốt cháy hết Y bằng O2 thu được CO2 và 3,05x mol H2O. Phần trăm khối lượng CH4 trong Y bằng.
Giả sử x = 1. ⇒ nC4H10 dư = 0,25 mol.
⇒ nCH4 + nC2H6 = nC4H10 pứ = 0,75 mol. Y gồm CH4 và C3H6 và C4H10 dư.
nH2O = 3,05 = 2nCH4 + 3nC3H6 + 5 × 0,25. Giải hệ có: nCH4 = 0,45 mol; nC2H6 = 0,3 mol.
⇒ %mCH4/Y = 0,45 × 16 ÷ (0,45 × 16 + 0,3 × 30 + 0,25 × 58) × 100% = 23,45%.
Hỗn hợp X gồm Mg, Fe, Fe3O4 và CuO, trong đó oxi chiếm 20% khối lượng. Cho a gam hỗn hợp X tan hết vào dung dịch Y gồm H2SO4 1,32M và NaNO3 0,8M, thu được dung dịch Z chứa b gam các chất tan đều là muối trung hòa và 1,792 lít khí NO (ở đktc). Dung dịch Z phản ứng với dung dịch KOH dư thấy có 68,32 gam muối trung hòa và 1,792 lít khí NO (ở đktc). Biết các phản ứng đều xảy ra hoàn toàn và 183a = 50b. Giá trị của b gần nhất với giá trị nào sau đây?
\(m\left( {Mg,Fe,Cu} \right) = 0,8a\left( g \right);{m_O} = 0,2a\left( g \right)\). Đặt \({n_{{H_2}S{O_4}}} = 1,32x \Rightarrow {n_{NaN{O_3}}} = 0,8x\).
\(\left\{ {\left( {Mg,Fe,Cu} \right);O} \right\} + \left\{ {{H_2}S{O_4}:1,32x;NaN{O_3}:0,8x} \right\} \to NO:0,08 + {H_2}O\left\{ {\left( {M{g^{2 + }},F{e^{? + }},C{u^{2 + }}} \right);N{a^ + }:0,8x;NH_4^ + ;SO_4^{2 - }:1,32x;NO_3^ - } \right\}\)
\(\left\{ {\left( {M{g^{2 + }},F{e^{? + }},C{u^{2 + }}} \right);N{a^ + }:0,8x;NH_4^ + ;SO_4^{2 - }:1,32x;NO_3^ - } \right\} + KOH:1,22 \to \left\{ {{K^ + }:1,22;N{a^ + }:0,8x;SO_4^{2 - }:1,32x;NO_3^ - } \right\}\)
\({n_{{H^ + }}} = 2{n_O} + 10{n_{NH_4^ + }} + 4{n_{NO}} \Rightarrow {n_{NH_4^ + }} = \left( {0,264x - 0,0025a - 0,032} \right){\rm{ mol}}\).
Bảo toàn nguyên tố nitơ: \({n_{NO_3^ - /Y}} = {n_{NO}} + {n_{NH_4^ + }} + {n_{NO_3^ - /Z}} \Rightarrow {n_{NO_3^ - /Z}} = 0,536x + 0,0025a - 0,048\)
Bảo toàn điện tích: \({n_{{K^ + }}} + {n_{N{a^ + }}} = 2{n_{SO_4^{2 - }}} + {n_{NO_3^ - }} \Rightarrow 1,22 + 0,8x = 3,176x + 0,0025a - 0,048\)
\(b = m\left( {Mg,Fe,Cu} \right) + {m_{N{a^ + }}} + {m_{NH_4^ + }} + {m_{SO_4^{2 - }}} + {m_{NO_3^ - }} = 183,104x + 0,91a - 3,552\)
\(\Rightarrow 183a = 50 \times \left( {183,104x + 0,91a - 3,552} \right)\)
Giải hệ có: \(x = 0,5{\rm{ mol;a = 32}}\left( g \right) \Rightarrow b = 117,12\left( g \right)\).
Hỗn hợp E gồm một tripeptit X (có dạng M-M-Gly, được tạo từ các α-amino axit thuộc dãy đồng đẳng), amin Y và este no, hai chức Z (X, Y, Z đều mạch hở, X và Z cùng số nguyên tử cacbon trong phân tử). Đun nóng m gam E với dung dịch KOH vừa đủ, cô cạn dung dịch thu được chất rắn A gồm 3 muối và 0,08 mol hỗn hợp hơi T (gồm 3 chất hữu cơ) có tỉ khối so với H2 bằng 24,75. Đốt cháy toàn bộ A cân dùng vừa đủ 21,92 gam khí O2 thu được N2, 15,18 gam K2CO3 và 30,4 gam hỗn hợp gồm CO2 và H2O. Khối lượng chất Y có trong m gam hỗn hợp E gần nhất với giá trị nào sau đây?
T chứa 3 chất hữu cơ trong đó chắc chắn có Y ⇒ T phải chứa 2 ancol
⇒ Z là este tạo bởi axit 2 chức. Quy A về C₂H₄NO₂K, (COOK)₂, CH₂.
Đặt nC₂H₄NO₂K = x; n(COOK)₂ = y; nCH₂ = z ⇒ nO2 = 2,25x + 0,5y + 1,5z = 0,685 mol.
nK₂CO₃ = 0,11 mol. Bảo toàn nguyên tố Kali: x + 2y = 0,11 × 2
Đốt A cho CO₂: 1,5x + y + z; H₂O: 2x + z ⇒ 30,4 = 44.(1,5x + y + z) + 18.(2x + z)
Giải hệ có: x = z = 0,18 mol; y = 0,02 mol ⇒ nX = 0,06 mol.
Đặt số gốc CH₂ ghép vào peptit và axit là 2a và b (a ≥ 2; b ≥ 1).
⇒ 0,06.2a + 0,02b = 0,18. Giải phương trình nghiệm nguyên: a = 1; b = 3.
⇒ X là Ala-Ala-Gly và muối của axit là C₅H₆O₄K₂. Do có cùng số C nên Z chứa 8C.
⇒ Z tạo bởi 2 ancol là CH₃OH và C₂H₅OH ⇒ nCH₃OH = nC₂H₅OH = 0,02 mol.
⇒ mY = 0,08 × 24,75 × 2 – 0,02 × 32 – 0,02 × 46 = 2,4(g).
Thực hiện phản ứng nhiệt nhôm hỗn hợp Al và Fe3O4 (trong điều kiện không có không khí thu được 234,75 gam chất rắn X. Chia X thành hai phần:
Cho 1 phần tác dụng với dung dịch NaOH dư thu được 1,68 lít khí H2 ở đktc và m gam chất rắn. Hòa tan hết m gam chất rắn vào dung dịch H2SO4 đặc nóng thu được dung dịch chứa 82,8 gam muối và 0,6 mol SO2 là sản phẩm khử duy nhất.
Hòa tan hết phần 2 trong 12,97 lít dung dịch HNO3 1M, thu được hỗn hợp khí Y (gồm 1,25 mol NO và 1,51 mol NO2) và dung dịch A chứa các chất tan đều là muối, trong đó có a mol Fe(NO3)3.
Biết các phản ứng hoàn toàn. Giá trị của a gần nhất với giá trị nào sau đây?
Xét phần 1: do sinh ra H2 ⇒ Al dư. nH2 = 0,075 mol ⇒ nAl dư = 0,05 mol.
Rắn không tan là Fe. Ta có: 2H2SO4 + 2e → SO2 + SO42– + 2H2O.
⇒ nSO42– = nSO2 = 0,6 mol ⇒ nFe = (82,8 – 0,6 × 96) ÷ 56 = 0,45 mol.
8Al + 3Fe3O4 → 4Al2O3 + 9Fe ⇒ nAl2O3 = 0,45 × 4 ÷ 9 = 0,2 mol.
⇒ mphần 1 = 0,05 × 27 + 0,2 × 102 + 0,45 × 56 = 46,95(g) ⇒ m phần 2 = 187,8(g).
⇒ phần 2 gấp 4 lần phần 1 ⇒ phần 2 chứa 0,2 mol Al; 0,8 mol Al2O3; 1,8 mol Fe.
Ta có: nH+ = 4nNO + 2nNO2 + 2nO + 10nNH4+ ⇒ nNH4+ = 0,015 mol.
Đặt nFe(NO3)2 = b ⇒ a + b = nFe = 1,8 mol; Bảo toàn electron:
0,2 × 3 + 3a + 2b = 1,25 × 3 + 1,51 + 0,015 × 8.
Giải hệ có: a = 1,18.