Đề thi thử THPT QG năm 2021 môn Hóa học - Trường THPT Bùi Thị Xuân
Đề thi thử THPT QG năm 2021 môn Hóa học - Trường THPT Bùi Thị Xuân
-
Hocon247
-
40 câu hỏi
-
90 phút
-
64 lượt thi
-
Trung bình
Tham gia [ Hs Hocon247.com ] - Cộng Đồng Luyện Thi Trực Tuyến để được học tập những kiến thức bổ ích từ HocOn247.com
Số đồng phân este ứng với công thức phân tử C3H6O2 là
Số đồng phân este ứng với công thức phân tử C3H6O2 là 2
Chọn phát biểu sai.
Phát biểu sai là Khi làm lạnh, hơi của photpho trắng chuyển thành photpho đỏ.
Phản ứng nào sau đây không phải là phản ứng trao đổi ion:
Phản ứng không phải là phản ứng trao đổi ion:
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
Cho các chất sau: CH2=CH-CH2-CH2-CH=CH2, CH2=CH-CH=CH-CH2-CH3, CH3-C(CH3)=CH-CH3, CH2=CH-CH2-CH=CH2. Số chất có đồng phân hình học là
Số chất có đồng phân hình học là 1: CH3-C(CH3)=CH-CH3
Cấu hình electron của ion X2+ là 1s22s22p63s23p63d6. Trong bảng tuần hoàn các nguyên tố hoá học, nguyên tố X thuộc
Trong bảng tuần hoàn các nguyên tố hoá học, nguyên tố X thuộc chu kì 4, nhóm VIIIB
Để phân biệt CO2 và SO2 chỉ cần dùng thuốc thử là
Để phân biệt CO2 và SO2 chỉ cần dùng thuốc thử là nước brom
Tỉ lệ số người chết về bệnh phổi do hút thuốc lá gấp hàng chục lần số người không hút thuốc là. Chất gây nghiện và gây ung thư có trong thuốc lá là
Tỉ lệ số người chết về bệnh phổi do hút thuốc lá gấp hàng chục lần số người không hút thuốc là. Chất gây nghiện và gây ung thư có trong thuốc lá là nicotin.
Trong các loại quặng sắt, quặng có hàm lượng sắt cao nhất là
Trong các loại quặng sắt, quặng có hàm lượng sắt cao nhất là manhetit.
Khi thủy phân chất nào sau đây thu được glixerol ?
Khi thủy phân trioleịn thu được glixerol
Sự phá huỷ kim loại do kim loại phản ứng với hơi nước hoặc chất khí ở nhiệt độ cao, gọi là
Sự phá huỷ kim loại do kim loại phản ứng với hơi nước hoặc chất khí ở nhiệt độ cao, gọi là sự ăn mòn hoá học
Kim loại nào sau đây có tính dẫn điện tốt nhất trong tất cả các kim loại?
Bạc có tính dẫn điện tốt nhất trong tất cả các kim loại
Polime có cấu trúc mạng không gian (mạng lưới) là
Polime có cấu trúc mạng không gian (mạng lưới) là nhựa bakelit
Trong phân tử hợp chất hữu cơ nào sau đây có liên kết peptit?
Trong phân tử protein có liên kết peptit
Cho các hợp chất hữu cơ: Glucozơ, fructozơ, saccarozơ, tinh bột, xenlulozơ. Số chất không tham gia phản ứng tráng bạc là
Số chất không tham gia phản ứng tráng bạc là 3
Để xác định glucozơ có trong nước tiểu người bệnh đái đường người ta dùng chất nào sau đây?
Để xác định glucozơ có trong nước tiểu người bệnh đái đường người ta dùng Cu(OH)2/ dd NaOH
Kim loại nào sau đây có độ cứng lớn nhất trong tất cả các kim loại?
Crom có độ cứng lớn nhất trong tất cả các kim loại
Các nguyên tử thuộc nhóm IIA có cấu hình electron lớp ngoài cùng là
Các nguyên tử thuộc nhóm IIA có cấu hình electron lớp ngoài cùng là ns2
Dãy gồm các kim loại đều phản ứng với nước ở nhiệt độ thường tạo ra dung dịch có môi trường kiềm là:
Dãy gồm các kim loại đều phản ứng với nước ở nhiệt độ thường tạo ra dung dịch có môi trường kiềm là: Na, Ba, K.
Cho phản ứng: aAl + bHNO3 → cAl(NO3)3 + dNO + eH2O. Hệ số a, b, c, d, e là các số nguyên, tối giản. Tổng (a + b) bằng
Al + 4HNO3 → Al(NO3)3 + NO + 2H2O
Công thức chung của oxit kim loại thuộc nhóm IA là
Công thức chung của oxit kim loại thuộc nhóm IA là R2O
Cho các chất: stiren, ancol benzylic, anilin, toluen, phenol. Số chất trong dãy có khả năng làm mất màu nước brom là
Số chất trong dãy có khả năng làm mất màu nước brom là 3
Các chất trong dãy nào sau đây đều tạo kết tủa khi cho tác dụng với dung dịch AgNO3 trong NH3 dư, đun nóng?
Các chất đều tạo kết tủa khi cho tác dụng với dung dịch AgNO3 trong NH3 dư, đun nóng: vinylaxetilen, glucozơ, anđehit axetic.
Khi làm thí nghiệm với H2SO4 đặc, nóng thường sinh ra khí SO2. Để hạn chế tốt nhất khí SO2 thoát ra gây ô nhiễm môi trường, người ta nút ống nghiệm bằng bông tẩm dung dịch nào sau đây?
Đáp án D
Cho 17,6 gam etyl axetat tác dụng hoàn toàn với 300ml dung dịch NaOH 1M, cô cạn thu được m gam chất rắn. Giá trị của m là
CH3COOC2H5 + NaOH -> CH3COONa + C2H5OH
0,2 mol -> 0,2 -> 0,2
Chất rắn gồm : 0,2 mol CH3COONa và 0,1 mol NaOH dư
=> mrắn = 20,4g
Đáp án A
Khi bị ốm, mất sức, nhiều người bệnh thường được truyền dịch đường để bổ sung nhanh năng lượng. Chất trong dịch truyền có tác dụng trên là
Khi bị ốm, mất sức, nhiều người bệnh thường được truyền dịch đường để bổ sung nhanh năng lượng. Chất trong dịch truyền có tác dụng trên là glucozơ
Cho 200 ml dung dịch Ba(OH)2 0,6M vào 100 ml dung dịch chứa NaHCO3 2M và BaCl2 1M, thu được a gam kết tủa. Giá trị của a là
nOH- = 0,24 mol; nHCO3- = 0,2 mol; nBa2+ = 0,22 mol
OH- + HCO3- → CO32- + H2O
0,2 0,2 0,2
Ba2+ + CO32- → BaCO3 + H2O
0,2 0,2 mol
mkết tủa = 39,4 gam
Cho các dữ kiện thí nghiệm:
(1) Cho dung dịch NaOH dư vào dung dịch Ca(HCO3)2.
(2) Cho Ba vào dung dịch Ba(HCO3)2.
(3) Cho Ba vào dung dịch H2SO4 loãng.
(4) Cho H2S vào dung dịch CuS.
(5) Sục dư NH3 vào dung dịch AlCl3.
(6) Cho dung dịch NaAlO2 dư vào dung dịch HCl.
Số trường hợp xuất hiện kết tủa khi kết thúc thí nghiệm là
Số trường hợp xuất hiện kết tủa khi kết thúc thí nghiệm là 6
Đá vôi là nguyên liệu có sẵn trong tự nhiên, được dùng làm vật liệu xây dựng, sản xuất vôi… Nung 100kg đá vôi ( chứa 80% CaCO3 về khối lượng, còn lại là tạp chất trơ) đến khối lượng không đổi, thu được m kg chất rắn. Gía trị của m là
nCO2 = 100.0,8/100 = 0,8 kmol
Bảo toàn khối lượng: m = 100 - 0,8.44 = 64,8 kg
Cho V ml dung dịch NaOH 2M vào 200 ml dung dịch AlCl3 1M, sau khi các phản ứng xảy ra hoàn toàn thu được 3,9 gam kết tủa. Giá trị lớn nhất của V là
Đáp án C
Điền số điện tích
Cho từ từ dung dịch HCl đến dư vào dung dịch NaAlO2. Kết quả thí nghiệm được biểu diễn ở đồ thị dưới đây.
Giá trị của a, b tương ứng là
Giá trị của a, b tương ứng là 0,2 và 0,2
Điện phân 100 ml dung dịch Cu(NO3)2 0,1M và NaCl 0,2M với điện cực trơ, màng ngăn xốp tới khi cả hai điện cực cùng có khí thoát ra thì kết thúc điện phân. Dung dịch sau phản ứng có pH là
2nCu2+ = nCl- = 0,02 mol , khi ở hai điện cực sinh ra khí thì Cu2+ và Cl- đồng thười điện phân hết
Dung dịch sau phản ứng chỉ chứa Na+, NO3-, H2O, pH = 7
Đáp án C
Hòa tan hết 32 gam hỗn hợp X gồm Fe, FeO và Fe2O3 vào 1 lít dung dịch HNO3 1,7M thu được V lít khí NO( sản phẩm khử duy nhất của N+5 , ở đktc) và dd Y. Biết Y hòa tan tối đa 12,8 gam Cu và không có khí thoát ra. Gía trị của V là
![]()
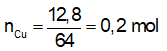
Quy hỗn hợp X về Fe và O
Sơ đồ phản ứng:
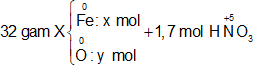

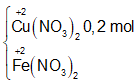
Quá trình cho nhận e:
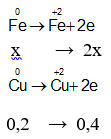
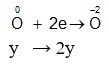
1,7 - 2y
![]()
2y → y
=> 56x + 16y = 32 (1)
Bảo toàn electron
![]()
=> 2x - 0,5y = 0,875 (2)
Từ (1) và (2) => x = 0,5; y = 0,25
![]()
= 0,3 mol
=> = 0,3.22,4 = 6,72 lit
=> Dung dịch Y chứa chất tan là FeCl2 và HCl
Cho hỗn hợp gồm Na và Al có tỉ lệ số mol tương ứng là 1 : 2 vào nước (dư). Sau khi các phản ứng xảy ra hoàn toàn, thu được 8,96 lít khí H2 (ở đktc) và m gam chất rắn không tan. Giá trị của m là
Gọi số mol của Na và Al lần lượt là x và 2x (mol)
Na + H2O → NaOH + 0,5H2
x x 0,5x
Al + NaOH + H2O → NaAlO2 + 1,5H2
x ← x → x → 1,5x
nH2 = 0,4 => 0,5x + 1,5x = 0,4 => x = 0,2
Chất rắn không tan là Al dư: nAl dư = 2x – x = x = 0,2 mol
=> m = mAl dư = 27.0,2 = 5,4 gam
Nung nóng m gam hỗn hợp Al và Fe2O3 (trong môi trường không có không khí) đến khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp rắn Y. Chia Y thành hai phần bằng nhau:
Phần 1 tác dụng với dung dịch H2SO4 loãng (dư), sinh ra 3,08 lít khí H2 (ở đktc);
Phần 2 tác dụng với dung dịch NaOH (dư), sinh ra 0,84 lít khí H2 (ở đktc).
Giá trị của m là
Chất rắn Y tác dụng với NaOH sinh ra H2 => Al dư => Chất rắn Y gồm: Al dư, Al2O3, Fe
nAl dư = nH2(P2)/1,5 = 0,0375/1,5 = 0,025 mol
nH2(P1) = nFe + 1,5nAl => nFe = 0,1375 – 1,5.0,025 = 0,1 mol
m(1 phần) = mAl ban đầu + mFe2O3 = 27(0,1+0,025) + 160.0,05 = 11,375 gam
=> m = 22,75 gam
Cho 0,3 mol hỗn hợp X gồm hai este đơn chức tác dụng vừa đử với 250 ml dung dịch KOH 2M, thu được chất hữu cơ Y( no, đơn chức, mạch hở, có tham gia phản ứng tráng bạc) và 53 gam hỗn hợp muối. Đốt cháy toàn bộ Y cần vừa đử 5,6 lít khí O2 (đktc). Khối lượng của 0,3 mol X là
0,3 mol X + vừa đủ 0,5 mol KOH
=> Chứng tỏ X có chứa este của phenol.
=> neste của phenol =0,5-0,3=0,2 mol; neste không của phenol = 0,3 - 0,2 =0,1 mol
Y có tham gia phản ứng tráng bạc => Y là andehit có dạng CnH2nO (0,1 mol)
CnH2nO +3n-12 O2 →tonCO2 +nH2O
nO2 = (3n – 1)/2.0,1 = 5,6/22,4 → n = 2
X + KOH → muối + CH3CHO + H2O
BTKL: mX = 53 = 44.0,1 + 18.0,2 – 56.0,5 = 33 gam
Hợp chất X mạch thẳng có CTPT là C4H9NO2. Cho 10,3 gam X phản ứng vừa đử với dung dịch NaOH sinh ra một chất khí Y và dung dịch Z. Khí Y nặng hơn không khí, làm giấy quì tím ẩm chuyển màu xanh. Dung dịch Z có khả năng làm mất màu nước brom. Cô cạn dung dịch Z thu được m gam muối khan. Gía trị m là
nX = = 0,1 mol
X tác dụng NaOH tạo khí Y nên X : R1COOH3NR2
Dung dịch Z làm mất màu nước Brom nên R có liên kết đôi C=C, suy ra R ≥ 27 (1)
Khí Y làm giấy quì tím ẩm hóa xanh nên Y : R2NH2 và MY > 29 ⇒ R2 + 16 > 29
⇒ R2 >13 (2)
Ta có : MX = R1 + R2 + 67 = 103 suy ra R1 + R2 = 42 (3)
Từ (1), (2)& (3) ⇒ R1= 27 : CH2=CH- và R2 = 15 : CH3-
CH2=CH-COOH3NCH3 + NaOH → CH2=CH-COONa + CH3NH2↑ + H2O
0,1mol 0,1 mol
Giá trị m = 0,1.94 = 9,4 gam
Đốt cháy hoàn toàn m gam một amin đơn chức X bằng lượng không khí vừa đủ thu được 1,76 gam CO2, 1,26 gam H2O và V lít N2 (đktc). Công thức phân tử của X và giá trị của V lần lượt là
X là C2H5NH2; V = 6,944 lít
Tiến hành thí nghiệm với các dung dịch X, Y, Z, và T. Kết quả được ghi lại ở bảng sau:
Axit glutamic, etyl fomat, glucozo, axitfomic
Đề thi liên quan
-
Đề thi thử THPT QG năm 2021 môn Hóa học - Trường THPT Bùi Thị Xuân
-
40 câu hỏi
-
90 phút
-