Đề thi thử THPT QG năm 2021 môn Hóa học - Trường THPT Trần Cao Vân
Đề thi thử THPT QG năm 2021 môn Hóa học - Trường THPT Trần Cao Vân
-
Hocon247
-
40 câu hỏi
-
90 phút
-
32 lượt thi
-
Trung bình
Tham gia [ Hs Hocon247.com ] - Cộng Đồng Luyện Thi Trực Tuyến để được học tập những kiến thức bổ ích từ HocOn247.com
Hỗn hợp X gồm đipeptit C5H10N2O3, este đa chức C4H6O4, este C5H11O2N. Cho X tác dụng vừa đủ với 800 ml dung dịch NaOH 0,1M, cô cạn dung dịch sau phản ứng thu được m gam rắn khan và 1,25 gam hỗn hợp hơi Z (chứa các hợp chất hữu cơ). Cho toàn bộ lượng Z thu được tác dụng với Na dư thấy thoát ra 0,448 lít khí H2 (đktc). Còn nếu đốt cháy hoàn toàn Z thì thu được 1,76 gam CO2. Giá trị của m là
Chọn A.
Xử lí hỗn hợp Z, nhận thấy: \({n_C} = {n_{C{O_2}}} = {n_{O{H^ - }}} = 2{n_{{H_2}}}\)Þ Các chất trong Z có số nguyên tử C bằng với số nhóm OH.
Từ 2 este ban đầu Þ Z gồm \(\left\{ \begin{gathered} C{H_3}OH:x\;mol \hfill \\ {C_2}{H_4}{\left( {OH} \right)_2}:y\;mol \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered} x + 2y = {n_{C{O_2}}} = 0,04 \hfill \\ 32x + 62y = 1,25 \hfill \\ \end{gathered} \right. \Rightarrow \left\{ \begin{gathered} x = 0,01 \hfill \\ y = 0,015 \hfill \\ \end{gathered} \right.\)
Khi cho X tác dụng với NaOH thì: \({n_{KOH}} = 2{n_{Gly - Ala}} + 2.{n_{{C_4}{H_6}{O_4}}} + {n_{{C_5}{H_{11}}{O_2}N}} \Rightarrow {n_{Gly - Ala}} = 0,02\,mol\)
\(X\left\{ \begin{gathered} Gly - Ala:0,02\;mol \hfill \\ {(HC{\text{OO)}}_{\text{2}}}{{\text{C}}_{\text{2}}}{{\text{H}}_{\text{4}}}:0,015\;mol \hfill \\ {{\text{H}}_{\text{2}}}{\text{N}}{{\text{C}}_3}{{\text{H}}_6}{\text{COOC}}{{\text{H}}_{\text{3}}}:0,01\;mol \hfill \\ \end{gathered} \right. \to \) hỗn hợp rắn \(\left\{ \begin{gathered} AlaNa + GlyNa \hfill \\ HC{\text{OONa}} \hfill \\ {{\text{H}}_{\text{2}}}{\text{N}}{{\text{C}}_3}{{\text{H}}_6}{\text{COO}}Na \hfill \\ \end{gathered} \right.\)Þ m = 7,45 gam
Có 4 dung dịch :natri clorua, ancol etylic, axit axetic, kali sunfat đều có nồng độ 0,1 mol/l. Khả năng dẫn điện của các dd đó tăng dần theo thứ tự nào trong các thứ tự sau:
Khả năng dẫn điện của các dd đó tăng dần theo thứ tự nào trong các thứ tự sau: C2H5OH < CH3COOH < NaCl < K2SO4.
Cho các ion kim loại. Zn2+, Sn2+, Ni2+, Fe2+, Pb2+. Thứ tự tính oxi hoá giảm dần là
Thứ tự tính oxi hoá giảm dần là Pb2+ > Sn2+ > Ni2+ > Fe2+ > Zn2+.
Cho kim loại Ba dư vào dung dịch Al2(SO4)3, thu được sản phẩm có:
Cho kim loại Ba dư vào dung dịch Al2(SO4)3, thu được sản phẩm có một chất khí và một chất kết tủa.
Hợp chất nào sau đây không có tính lưỡng tính?
Hợp chất AlCl3 không có tính lưỡng tính
Hòa tan nhôm vào dung dịch NaOH, chất bị khử trong phản ứng là gì?
Hòa tan nhôm vào dung dịch NaOH, chất bị khử trong phản ứng là H2O
Tiến hành bốn thí nghiệm sau:
- Thí nghiệm (1): Nhúng thanh Fe vào dung dịch FeCl3;
- Thí nghiệm (2): Nhúng thanh Fe vào dung dịch CuSO4;
- Thí nghiệm (3): Nhúng thanh Cu trong dung dịch Fe2(SO4)3 có nhỏ vài giọt dung dịch H2SO4 loãng;
- Thí nghiệm (4): Cho thanh Fe tiếp xúc với thanh Cu rồi nhúng vào dung dịch HCl.
Các thí nghiệm xuất hiện ăn mòn điện hoá là:
Các thí nghiệm xuất hiện ăn mòn điện hoá là: (2), (4).
Cacbon không tác dụng với chất nào sau đây?
Cacbon không tác dụng với NaOH
Trong các chất: Mg(OH)2, Al, NaHSO3 và KNO3, số chất thuộc loại chất lưỡng tính là
NaHSO3 là chất lưỡng tính
Dãy nào sau đây chỉ gồm các chất vừa tác dụng được với dung dịch HCl, vừa tác dụng được với dung dịch AgNO3 ?
Dãy chỉ gồm các chất vừa tác dụng được với dung dịch HCl, vừa tác dụng được với dung dịch AgNO3 là Fe, Ni, Sn.
Cho dãy các chất: Ag, Fe3O4, Na2CO3 và Fe(OH)3. Số chất trong dãy tác dụng được với dung dịch H2SO4 loãng là
Số chất trong dãy tác dụng được với dung dịch H2SO4 loãng là 3
Khi thủy phân hợp chất hữu cơ X (không có phản ứng tráng bạc) trong môi trường axit rồi trung hòa axit thì dung dịch thu được có phản ứng tráng bạc. X là gì?
X là Saccarozơ
Chất béo là thức ăn quan trọng của con người, là nguồn cung cấp dinh dưỡng và năng lượng đáng kể cho cơ thể hoạt động. Ngoài ra, một lượng lớn chất béo được dùng trong công nghiệp để sản xuất
Chất béo là thức ăn quan trọng của con người, là nguồn cung cấp dinh dưỡng và năng lượng đáng kể cho cơ thể hoạt động. Ngoài ra, một lượng lớn chất béo được dùng trong công nghiệp để sản xuất xà phòng và glixerol.
Một este E mạch hở có công thức phân tử C4H6O2. Thủy phân E trong môi trường axit thu được sản phẩm có phản ứng tráng bạc. Có bao nhiêu công thức cấu tạo của E thỏa mãn tính chất trên?
Có 4 công thức cấu tạo của E thỏa mãn tính chất trên
Cho dãy các dung dịch sau:C6H5NH2, NH2CH2COOH, HOOC[CH2]2CH(NH2)COOH C2H5NH2, NH2[CH2]2CH(NH2)COOH. Số dung dịch trong dãy làm đổi màu quỳ tím ?
Số dung dịch trong dãy làm đổi màu quỳ tím là 3
Cacbohidrat nào sau đây được dùng làm nguyên liệu sản xuất tơ visco ?
Xenlulozơ được dùng làm nguyên liệu sản xuất tơ visco
Thủy phân hoàn toàn tinh bột, thu được monosaccarit X. Hiđro hóa X, thu được chất hữu cơ Y. Hai chất X, Y lần lượt là
Thủy phân hoàn toàn tinh bột, thu được monosaccarit X. Hiđro hóa X, thu được chất hữu cơ Y. Hai chất X, Y lần lượt là glucozơ, sobitol.
Chất nào sau đây trùng hợp tạo PVC?
CH2=CHCl trùng hợp tạo PVC
Cho X, Y, Z, T là các chất khác nhau trong các chất: ![]() (phenol),
(phenol), ![]() và các tính chất được ghi trong bảng sau:
và các tính chất được ghi trong bảng sau:
Z là CH3NH2.
Phát biểu nào sau đây đúng ?
Cao su buna có phản ứng cộng.
Ô nhiễm không khí có thể tạo ra mưa axit gây tác hại rất lớn đối với thiên nhiên, con người, động vật, công trình xây dựng… Các chất khí gây nên hiện tượng trên, đó là
Ô nhiễm không khí có thể tạo ra mưa axit gây tác hại rất lớn đối với thiên nhiên, con người, động vật, công trình xây dựng… Các chất khí gây nên hiện tượng trên, đó là SO2, NO2.
Đốt cháy hoàn toàn một thê tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thê tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thê tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là (Cho H = 1; C = 12; O = 16)
Đáp án A
nCO2=7,84/22,4=0,35(mol) ; nH2O =9,9/18=0,55(mol)
Bảo toàn nguyên tố O:
2nO2=2nCO2+nH2O ⇒nO2=0,625(mol) ⇒VO2=0,625 . 22,4 = 14 l
Vì oxi chiếm 1/5 Vkk => Vkk = 5.14 = 70 (lít)
Cho các thí nghiệm sau:
(1) Cho hỗn hợp Na và Al (tỉ lệ mol 2 : 1) vào nước dư.
(2) Cho CrO3 vào nước dư.
(3) Vôi sống (CaO) và sođa (Na2CO3) (tỉ lệ mol 1 : 1) vào nước dư.
(4) Cho a mol hỗn hợp Fe2O3 và Cu (tỉ lệ mol 1 : 1) vào dung dịch chứa 3a mol HCl.
(5) Cho a mol khí CO2 vào dung dịch chứa 2a mol NaOH.
(6) Cho a mol Na vào dung dịch chứa a mol CuSO4.
Số thí nghiệm sau khi các phản ứng xảy ra hoàn toàn, phần dung dịch thu được chứa hai chất tan là
Số thí nghiệm sau khi các phản ứng xảy ra hoàn toàn, phần dung dịch thu được chứa hai chất tan là 6
Cho các cặp chất sau:
(1). Khí Br2 và khí O2. (5) Si và dung dịch NaOH loãng
(2). Khí H2S và dung dịch FeCl3. (6). Dung dịch KMnO4 và khí SO2.
(3). Khí H2S và dung dịch Pb(NO3)2. (7). Hg và S.
(4). CuS và dung dịch HCl. (8). Khí Cl2 và dung dịch NaOH.
Số cặp chất xảy ra phản ứng hóa học ở nhiệt độ thường là
Số cặp chất xảy ra phản ứng hóa học ở nhiệt độ thường là 6
Cho m gam Mg vào dung dịch chứa 0,1 mol AgNO3 và 0,25 mol Cu(NO3)2, sau một thời gian thu được 19,44 gam kết tủa và dung dịch X chứa 2 muối. Tách lấy kết tủa, thêm tiếp 8,4 gam bột sắt vào dung dịch X, sau khi các phản ứng hoàn toàn thu được 9,36 gam kết tủa. Giá trị của m là
Đáp án C
Dung dịch X chứa Mg(NO3)2 (a mol) và Cu(NO3)2 dư (b mol)
Bảo toàn N => 2a + 2b = 0,1 + 0,25.2
X với Fe: ![]() m = 64b - 56b = 9,36 - 8,4
m = 64b - 56b = 9,36 - 8,4
Giải hệ được a = 0,18 và b = 0,12
Trong 19,44 gam kết tủa chứa Ag (0,1), Cu
(0,25 - 0,12 = 0,13) => mMg dư = 0,32
- m = 0,18.24 + 0,32 = 4,64
Hoà tan hết a gam Al vào 450 ml dung dịch NaOH 1M thu được 13,44 lít H2 (đktc) và dung dịch X. Hoà tan hết b gam Al vào 400 ml dung dịch HCl 1M thu được 3,36 lít H2 (đktc) và dung dịch Y. Trộn dung dịch X với dung dịch Y đến phản ứng hoàn toàn thì thu được m gam kết tủa. Giá trị m là?
\(X\left\{ \begin{gathered} NaAl{O_2}:{0,4^{mol}} \hfill \\ NaOH:{0,05^{mol}} \hfill \\ \end{gathered} \right.\)
\(Y\left\{ \begin{gathered} AlC{l_3}:{0,1^{mol}} \hfill \\ HCl:{0,1^{mol}} \hfill \\ \end{gathered} \right.\)
\(m = 78.(0,05 + 0,1.4) = 35,1{\text{ gam}}\)
Cho m gam hỗn X gồm Fe và Al tan hoàn toàn trong 1,2 lít dung dịch HCl 1M (dư), thu được dung dịch Y và thoát ra 10,752 lít H2 (đktc). Mặt khác cho m gam hỗn hợp X vào dung dịch H2SO4 đặc nóng, dư, khi phản ứng xảy ra hoàn toàn, thu được 14,112 lít SO2 (đktc, sản phẩm khử duy nhất của S+6). Thêm 0,1 mol NaNO3 vào dung dịch Y, khi phản ứng xảy ra hoàn toàn thu được dung dịch Z và thoát ra V lít khí NO (đktc, sản phẩm khử duy nhất của N+5). Khối lượng muối có trong Z là?
\(Y\left\{ \begin{gathered} A{l^{3 + }}:{0,12^{mol}} \hfill \\ F{e^{2 + }}:{0,3^{mol}} \hfill \\ C{l^ - }:{1,2^{mol}} \hfill \\ {H^ + }:{0,24^{mol}} \hfill \\ \end{gathered} \right.\xrightarrow{{NaN{O_3}:{{0,1}^{mol}}}}NO:{0,06^{mol}} + Z\left\{ \begin{gathered} A{l^{3 + }}:{0,12^{mol}} \hfill \\ F{e^{3 + }}:{0,3^{mol}} \hfill \\ C{l^ - }:{1,2^{mol}} \hfill \\ N{a^ + }:{0,1^{mol}} \hfill \\ NO_3^ - :{0,04^{mol}} \hfill \\ \end{gathered} \right. \to m = 67,42{\text{ gam}}\)
Điện phân dung dịch X chứa Cu(NO3)2 và NaCl với điện cực trơ thấy thể tích khí thoát ra ở cả 2 điện cực (V lít) và thời gian điện phân (t giây) phụ thuộc nhau như trên đồ thị.
Nếu điện phân dung dịch trong thời gian 2,5a giây rồ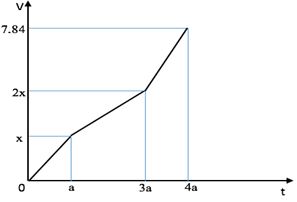
Chọn B.
Tại t = a (s) : có khí Cl2 thoát ra tại anot Þ \({V_{C{l_2}}} = x \Rightarrow {n_{e\;(1)}} = 2{n_{C{l_2}}} = \frac{{2x}}{{22,4}}\)
Tại t = 3a (s) : có khí Cl2, O2 thoát ra tại anot mà \({V_{C{l_2}}} + {V_{{O_2}}} = 2x \Rightarrow {V_{{O_2}}} = x \Rightarrow {n_{{O_2}}} = \frac{x}{{22,4}}\)
\(\xrightarrow{{BT:\;e}}{n_{Cu}} = \frac{{3{n_{e\;(1)}}}}{2} = \frac{{3x}}{{22,4}}\)
Tại t = 4a (s) : có khí Cl2, O2 thoát ra tại anot và khí H2 thoát ra tại catot.
\(V = {V_{C{l_2}}} + {V_{{O_2}}} + {V_{{H_2}}} = 7,84 \Rightarrow {n_{{O_2}}} + {n_{{H_2}}} = 0,35 - \frac{x}{{22,4}}\) (1)
\(\xrightarrow{{BT:\;e}}\left\{ \begin{gathered} {n_{{H_2}}} = \frac{1}{2}(4{n_{e\;(1)}} - 2{n_{Cu}}) = \frac{1}{2}(\frac{{8x}}{{22,4}} - \frac{{6x}}{{22,4}}) = \frac{x}{{22,4}} \hfill \\ {n_{{O_2}}} = \frac{1}{4}(4{n_{e\;(1)}} - 2{n_{C{l_2}}}) = \frac{1}{4}(\frac{{8x}}{{22,4}} - \frac{{2x}}{{22,4}}) = \frac{{1,5x}}{{22,4}} \hfill \\ \end{gathered} \right.\) (2)
Thay (2) thay vào (1): x = 2,24.
Tại t = 2,5a (s) : có khí Cl2 (0,1 mol), O2 thoát ra tại anot và tại có Cu
Có \({n_e} = 2,5{n_{e\;(1)}} = 0,5\;mol \Rightarrow \left\{ \begin{gathered} {n_{{O_2}}} = 0,075\;mol \Rightarrow {n_{HN{O_3}}} = 4{n_{{O_2}}} = 0,3\,mol \hfill \\ {n_{Cu}} = 0,25\;mol \Rightarrow {n_{C{u^{2 + }}\,({\text{dd}})}} = 0,3 - 0,25 = 0,05\;mol \hfill \\ \end{gathered} \right.\)
Khi cho Fe tác dụng với dung dịch sau điện phân thì: \({m_{Fe}} = 56.\left( {\frac{3}{8}{n_{HN{O_3}}} + {n_{C{u^{2 + }}}}} \right) = 9,1\;(g)\)
Cho m gam hỗn hợp E gồm este hai chức Y mạch hở và este đơn chức X tác dụng vừa đủ với dung dịch NaOH, thu được hỗn hợp Z chứa hai muối và một ancol T duy nhất. Đốt cháy hoàn toàn Z cần vừa đủ 1,08 mol O2, thu được 14,84 gam Na2CO3; tổng số mol CO2 và H2O bằng 1,36 mol. Cho ancol T tác dụng với Na (dư), thoát ra 1,792 lit khí (đktc); biết để đốt cháy hết m gam E cần vừa đủ 1,4 mol O2. Phần trăm khối lượng của Y có giá trị gần nhất với
\({n_{OH(ancol)}} = 0,08.2 = {0,16^{mol}}\) → X là este của phenol
\({n_X} = \frac{{0,28 - 0,16}}{2} = {0,06^{mol}} \to {n_Y} = {0,08^{mol}}\)
\(\left\{ \begin{gathered} C{O_2}:{x^{mol}} \hfill \\ {H_2}O:{y^{mol}} \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered} x + y = 1,36 \hfill \\ \xrightarrow{{BT{\text{ O}}}}2x + y + 0,14.3 = 0,22.2 + 0,06 + 1,08.2 \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered} x = 0,88 \hfill \\ y = 0,48 \hfill \\ \end{gathered} \right.\)
\(Z\left\{ \begin{gathered} RCOONa:{0,22^{mol}} \hfill \\ R'ONa:{0,06^{mol}} \hfill \\ \end{gathered} \right.\xrightarrow{{Lam{\text{ troi}}}}\left\{ \begin{gathered} C{H_2} = CH - COONa \hfill \\ {C_6}{H_5}ONa \hfill \\ \end{gathered} \right.\)
\({n_{{O_2}/(T)}} = 1,4 - 1,08 = {0,32^{mol}} \to T:{C_3}{H_8}{O_2} \to Y:{(C{H_2} = CHCOO)_2}{C_3}{H_6}\)
\( \to \% {m_Y} = 62,37\% \)
X là axit no, đơn chức, Y là axit không no, có một liên kết đôi C=C, có đồng phân hình học và Z là este hai chức tạo X, Y và một ancol no (tất cả các chất đều thuần chức, mạch hở). Đốt cháy hoàn toàn 9,52 gam E chứa X, Y và Z thu được 5,76 gam H2O. Mặt khác, 9,52 gam E có thể phản ứng tối đa với dung dịch chứa 0,12 mol NaOH sản phẩm sau phản ứng có chứa 12,52 hỗn hợp các chất hữu cơ. Cho các phát biểu liên quan tới bài toán gồm:
(1) Phần trăm khối lượng của X trong E là 72,76% (2) Số mol của Y trong E là 0,08 mol.
(3) Khối lượng của Z trong E là 1,72 gam. (4) Tổng số nguyên tử (C, H, O) trong Y là 12
(5) X không tham gia phản ứng tráng bạc
Số phát biểu đúng là ?
Đáp án B
X: CH2xO2 (a mol)
Y: OH2y-2O2 (b mol)
Z: CH2z-4O4 (c mol)
nH2O =ax + b(y - 1) + c(z - 2) = 0,32
mE = a(14x + 32) + b(14y + 30) + c(14z +60) = 9,52
nNaOH =a + b + 2c = 0,12
Bảo toàn khối lượng cho phản ứng với
NaOH → nH2O =a + b= 0,1,02; b = 0,08; c = 0,01;
ax + by + cz→ 2x+8y+z= 42
Do\(x \geqslant 1,\,y \geqslant 4,z \geqslant 7 \to\)x = 1;y =4 ;z = 8 là nghiệm duy nhất.
X là HCOOH: 0,02
Y là CH3-CH=CH-COOH: 0,08
Z là CH3-CH=CH-COO-C3H6-OOC-H: 0,01
%X = 9,669 —> a sai.
nY = 0,08 —> b sai
mZ = 1,72 —> c sai
Z là C8H12O4 —> Tổng 24 nguyên tử —>d đúng
Đốt cháy hoàn toàn m gam hỗn hợp M (có tổng số mol 0,07 mol) gồm đipeptit X, tripeptit Y, tetrapeptit Z và pentapeptit T đều mạch hở cần dùng 15,288 lít khí O2. Nếu cho m gam hỗn hợp M tác dụng với dung dịch KOH vừa đủ rồi cô cạn cẩn thận thu được rắn E gồm hỗn hợp muối của glyxin và alanin. Đốt cháy E trong bình chứa 3,5 mol không khí. Toàn bộ khí sau phản ứng cháy sau khi được ngưng tụ hơi nước thì còn lại 75,656 lít hỗn hợp khí. Các phản ứng xảy ra hoàn toàn, các thể tích khí đo ở điều kiện tiêu chuẩn. Trong không khí O2 chiếm 20% thể tích, còn lại là N2. Giá trị gần nhất của m là?
\(M\left\{ \begin{gathered} {C_2}{H_3}NO:{x^{mol}} \hfill \\ C{H_2}:{y^{mol}} \hfill \\ {H_2}O:{0,07^{mol}} \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered} 2,25x + 1,5y = 0,6825 \hfill \\ \underbrace {0,7 - 0,6825}_{{O_2}} + \underbrace {1,5x + y}_{C{O_2}} + \underbrace {0,5x + 2,8}_{{N_2}} = 3,3775 \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered} x = 0,21 \hfill \\ y = 0,14 \hfill \\ \end{gathered} \right.\)
\( \to m = 15,19{\text{ gam}}\)
Hỗn hợp T gồm các chất mạch hở: anđehit X, axit cacboxylic Y và ancol Z (50 < MX< MY; X và Z có số mol bằng nhau). Đốt cháy hoàn toàn m gam T, thu được H2O và 17,92 lít khí CO2(đktc). Cho m gam T phản ứng với dung dịch NaHCO3 dư, thu được 6,72 lít khí CO2 (đktc). Nếu cho m gam T tác dụng với lượng dư Na thu được 0,6 gam khí H2. Mặt khác, m gam T phản ứng hoàn toàn với lượng dư dung dịch AgNO3/NH3, thu được 43,2 gam Ag. Giá trị của m là
\(\begin{gathered} T + NaHC{O_3} \to {n_{COOH}} = {n_{C{O_2}}} = 0,3 \hfill \\ T + Na \to {n_{COOH}} + {n_{CHOH}} = 2{n_{{H_2}}} = 0,6 \to {n_{CHOH}} = 0,3 \hfill \\ \end{gathered}\)
\(T + \frac{{AgN{O_3}}}{{N{H_3}}} \to {n_{CHO}} = \frac{{{n_{Ag}}}}{2} = 0,2\)
Dễ thấy \({n_{C{O_2}}} = {n_{COOH}} + {n_{CHOH}} + {n_{CHO}} = 0,8\) nên X, Y, Z chỉ tạo bởi các nhóm này, không còn C nào khác.
\(50 < MX < MY \to X:{\left( {CHO} \right)_2}\,\left( {0,1\,mol} \right);\,Y:{\left( {COOH} \right)_2}\,\left( {0,15\,mol} \right)\)
\(nZ = nX = 0,1 \to Z\) có 0,3/0,1 =3 nhóm OH
Z là \({C_3}{H_5}{\left( {OH} \right)_3}\,\left( {0,1\,mol} \right)\)
\( \Rightarrow {m_T} = 28,5\,gam\)
Chất nào sau đây không phải chất điện li trong nước?
C6H12O6 không phải chất điện li trong nước
Hợp chất hữu cơ luôn có nguyên tố nào?
Hợp chất hữu cơ luôn có nguyên tố cacbon
Số nhóm chức este có trong mỗi phân tử chất béo là bao nhiêu?
Số nhóm chức este có trong mỗi phân tử chất béo là 3
Phát biểu nào sau đây sai?
Phát biểu sai: Trong nước, brom khử glucozơ thành axit gluconic.
Tính chất hóa học đặc trưng của kim loại là gì?
Tính chất hóa học đặc trưng của kim loại là tính khử
Trong các kim loại sau: Na, Fe, Hg, W. Kim loại nào có nhiệt độ nóng chảy thấp nhất?
Hg có nhiệt độ nóng chảy thấp nhất
Trong công nghiệp, kim loại nào chỉ được điều chế bằng phương pháp điện phân nóng chảy?
Trong công nghiệp, kim loại natri chỉ được điều chế bằng phương pháp điện phân nóng chảy

