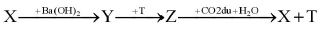Đề thi thử THPT QG năm 2021 môn Hóa học - Trường THPT Trần Hưng Đạo
Đề thi thử THPT QG năm 2021 môn Hóa học - Trường THPT Trần Hưng Đạo
-
Hocon247
-
40 câu hỏi
-
90 phút
-
30 lượt thi
-
Dễ
Tham gia [ Hs Hocon247.com ] - Cộng Đồng Luyện Thi Trực Tuyến để được học tập những kiến thức bổ ích từ HocOn247.com
Phát biểu nào sau đây đúng ?
Trong công thức của este RCOOR’, R có thể là nguyên tử H hoặc gốc hidrocacbon.
Nhúng một lá sắt (dư) vào dung dịch chứa một trong các chất sau: FeCl3, AlCl3, CuSO4, Pb(NO3)2, H2SO4 đặc nóng. Sau phản ứng lấy lá sắt ra, có bao nhiêu trường hơp tạo muối sắt (II) ?
Sau phản ứng lấy lá sắt ra, có 4 trường hơp tạo muối sắt (II)
: Tiến hành các thí nghiệm sau:
(a) Cho Mg vào dung dịch Fe2 (SO4)3 dư
(b) Sục khí Cl2vào dung dịch FeCl2
(c) Dẫn khí H2 dư qua bột CuO nung nóng
(d) Cho Na vào dung dịch CuSO4 dư
(e) Nhiệt phân AgNO3
(g) Đốt FeS2 trong không khí
(h) Điện phân dung dịch CuSO4 với điện cực trơ.
Sau khi kết thúc các phản ứng. Số thí nghiệm thu được kim loại là
Sau khi kết thúc các phản ứng. Số thí nghiệm thu được kim loại là 3
Đốt cháy hoàn toàn một hiđrocacbon X cho CO2 và hơi H2O theo tỉ lệ 1,75:1 về thể tích. Cho bay hơi hoàn toàn 5,06g X thu được một thể tích đúng bằng thể tích của 1,76g oxi trong cùng điều kiện. Ở nhiệt độ phòng, X không làm mất màu nước brom nhưng làm mất màu dung dịch KMnO4 khi đun nóng. X là hiđrocacbon nào dưới đây ?
nO2 0,055 mol → MX = 92. (1)
Gọi CTPT X là CxHy. Vì VCO2 :VH2O = 1,75 :1 → x :y = 1,75 : 2 = 7 :8 (2)
Từ (1)(2) → CTPT của X là C7H8. → Đáp án B
Hỗn hợp X gồm 2 aminoaxit no( chỉ có nhóm chức –COOH và –NH2 trong phân tử), trong đó tỉ lệ mO : mN= 80 :21.Để tác dụng vừa đủ với 3,83 gam hỗn hợp X cần 30 ml dung dịch HCl 1M.Mặt khác ,đốt cháy hoàn toàn 3,83 gam hỗn hợp X cần 3,192 lít O2 (đktc).Dẫn toàn bộ sản phẩm cháy (CO2,H2O,N2) vào nước vôi trong dư thì thu được m gam kết tủa.Giá trị của m là
-NH2 + HCl → -NH3Cl → nN = nHCl = 0,03 mol
- mN = 0,42 gam → mO = 1,6 gam → nO = 0,1 mol
Đặt nC = x, nH = y → nCO2 = x, nH2O = 0,5y.
mX = mC + mH + mN + mO → 12x + y = 1,81 (1)
Bảo toàn nguyên tố oxi : nO/X + 2nO2 = nCO2 + nH2O
- 0,1 + 2.0,1425 = 2x + 0,5y (2)
Từ (1)(2)→ x = 0,13 mol ; y = 0,25 mol
- mkết tủa = 13 gam → Đáp án B.
Cho m gam glucozơ lên men thành ancol etylic với H= 75%. Toàn bộ khí CO2 sinh ra được hấp thụ hết vào dung dịch Ca(OH)2 lấy dư tạo ra 350 gam kết tủa. Giá trị của m
nCaCO3 = nCO2 = 3,5 mol
- nGlucozo = 3,5/2.0,75 = 7/3 mol.
- mGlucozo = 180.7/3 = 420 gam → Đáp án B.
Hỗn hợp X gồm 2 este đơn chức A và B (B hơn A một nhóm -CH2-). Cho 3,35 gam hỗn hợp X tác dụng vừa đủ với 50ml dung dịch NaOH 1M thu được 3,75 gam hỗn hợp 2 muối. Công thức cấu tạo của A và B?
nNaOH = 0,05 mol → Mtb của hh este = 67 → MA < 67 MB
- A là H-COOCH3 → B là H-COOC2H5 hoặc CH3-COOCH3 (1)
Từ mhh este = 3,35 gam và nhh = 0,05 mol → nA = nB = 0,025 mol
Từ mhh muối = 3,75 gam → B là CH3-COOCH3 → Đáp án D.
Hoặc từ (1) suy luận vì tạo hỗn hợp 2 muối nên B không thể là H-COOC2H5 (Chỉ tạo 1 muối H-COONa) à B là CH3-COOCH3.
Cho m gam bột Zn vào 400 ml dung dịch Fe2(SO4)3 0,15M. Sau khi các phản ứng xảy ra hoàn toàn, khối lượng dung dịch tăng thêm 4,8 gam so với khối lượng dung dịch ban đầu. Giá trị của m là
Zn + 2Fe3+ → Zn2+ + 2Fe2+ (1)
0,06 0,12
Zn + Fe2+ → Zn2+ + Fe (2)
nFe3+ = 0,06 mol
mdd tăng = mZn(1) + mZn(2) – nFe(2) = 4,8 → 65.0,06 + 9.nZn(2) = 4,8 → nZn(2) = 0,1 mol
M = 0,16.65 = 10,4 gam
Đáp án A.
Cho 6,048 gam Mg phản ứng hết với 189 gam dung dịch HNO3 40% thu được dung dịch X (không chứa muối amoni) và hỗn hợp khí là oxit của nitơ. Thêm 392 gam dung dịch KOH 20% vào dung dịch X, rồi cô cạn và nung sản phẩm đến khối lượng không đổi thì thu được 118,06 gam hỗn hợp chất rắn. Nồng độ phần trăm của Mg(NO3)2 và HNO3 trong dung dịch X là
nHNO3= 1,2 mol nMg=0,252 nKOH đã lấy= 1,4 mol
Vì nKOH >nHNO3 nên KOH dư
118,06 gam chất rắn gồm 0,252 mol MgO, x mol KOH và y mol KNO2
x+y = 1,4
40*0,252 + 56x + 85y = 118,06 x=0,38 y=1,02
Þ nNO3 trong dung dịch sau phản ứng = nKNO2= 1,02
Þ nN+5 nhận electron = 1,2-1,02 =0,18.
Gọi số mol electron mà N+5 nhận trung bình là n ta có 0,18*n=0,252*2 Þ n=2,8
coi như oxit thoát ra là 0,09 mol N2O2,2Þ mkhi=0,09*(28+16*2,2)= 5,688
mdung dịch X=6,048 +189-5,688=189,36 gam
X chứa 0,252 mol Mg(NO3)2; 0,516 mol HNO3 dư
C%Mg(NO3)2=19,696% C%HNO3= 17,167%
Nung m gam hỗn hợp X gồm bột Al và Fe3O4 sau một thời gian thu được chất rắn Y. Để hoà tan hết Y cần V lít dung dịch H2SO4 0,7M (loãng). Sau phản ứng thu được dung dịch Z và 0,6 mol khí. Cho dung dịch NaOH vào dung dịch Z đến dư, thu được kết tủa M. Nung M trong chân không đến khối lượng không đổi thu được 44 gam chất rắn T. Cho 50 gam hỗn hợp A gồm CO và CO2 qua ống sứ được chất rắn T nung nóng. Sau khi T phản ứng hết thu được hỗn hợp khí B có khối lượng gấp 1,208 lần khối lượng của A. Giá trị của (m - V) gần với giá trị nào sau đây nhất ?
Khi cho nung T với hỗn hợp khí A thì \({n_{O(trong\,T)}} = \frac{{{m_B} - {m_A}}}{{16}} = \frac{{1,208{m_A} - {m_A}}}{{16}} = 0,65\)
- Xét hỗn hợp rắn T ta có :
\(\left\{ \begin{gathered} 160{n_{F{e_2}{O_3}}} + 72{n_{FeO}} = {m_T} = 44 \hfill \\ 3{n_{F{e_2}{O_3}}} + {n_{FeO}} = {n_{O(trong\,T)}} = 0,65 \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered} {n_{F{e_2}{O_3}}} = 0,05 \hfill \\ {n_{FeO}} = 0,5 \hfill \\ \end{gathered} \right. \Rightarrow {n_{F{e_3}{O_4}(X)}} = \frac{{2{n_{F{e_2}{O_3}}} + {n_{FeO}}}}{3} = 0,2\,mol\)
- Khi cho m gam X tác dụng với H2SO4 thì : \({n_{{H_2}S{O_4}}} = 4{n_{F{e_3}{O_4}}} + {n_{{H_2}}} = 1,4\,mol \Rightarrow {V_{{H_2}S{O_4}}} = \frac{{1,4}}{{0,7}} = 2\,(l)\)
- Dung dịch Z gồm Al3+, SO42- (1,4 mol), Fe2+ và Fe3+ (với \({n_{F{e^{3 + }}}} = 2{n_{F{e_2}{O_3}}};{{\text{n}}_{F{e^{2 + }}}} = {n_{FeO}}\) )
\(\xrightarrow{{BTDT(Z)}}{n_{A{l^{3 + }}}} = \frac{{{n_{S{O_4}^{2 - }}} - 2{n_{F{e^{2 + }}}} - 3{n_{F{e^{3 + }}}}}}{3} = 0,5\,mol \Rightarrow \left\{ \begin{gathered} {m_X} = 27{n_{Al}} + 232{n_{F{e_3}{O_4}}} = 59,9\,(g) \hfill \\ \to {m_X} - V = \boxed{57,9\,(g)} \hfill \\ \end{gathered} \right.\)
Đốt cháy hoàn toàn 14,24 gam hỗn hợp X chứa 2 este đều no, đơn chức, mạch hở thu được CO2 và H2O có tổng khối lượng là 34,72 gam. Mặt khác đun nóng 14,24 gam X với dung dịch NaOH vừa đủ, thu được hỗn hợp Y chứa 2 ancol kế tiếp và hỗn hợp Z chứa 2 muối của 2 axit cacboxylic kế tiếp, trong đó có a gam muối A và b gam muối B (MA < MB). Tỉ lệ gần nhất của a : b là
- Khi đốt X chứa 2 este no, đơn chức, mạch hở thì ta luôn có: \({n_{C{O_2}}} = {n_{{H_2}O}} = 0,56\;mol\)
\(\xrightarrow{{BTKL}}{n_{{O_2}}} = \frac{{{m_{C{O_2} + {H_2}O}} - {m_X}}}{{32}} = 0,64\;mol\xrightarrow{{BT:\;O}}{n_X} = \frac{{2{n_{C{O_2}}} + {n_{{H_2}O}} - 2{n_{{O_2}}}}}{2} = 0,2\;mol\)
- Ta có: \({C_X} = \frac{{0,56}}{{0,2}} = 2,8\). Vì khi cho X tác dụng với NaOH thu được 2 ancol kế tiếp và 2 muối của 2 axit cacboxylic kế tiếp nên 2 este trong X lần lượt là:
\(\left\{ \begin{gathered} HCOOC{H_3}:x\;mol \hfill \\ C{H_3}COO{C_2}{H_5}:y\;mol \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered} x + y = 0,2 \hfill \\ 2x + 4y = 0,56 \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered} x = 0,12 \hfill \\ y = 0,08 \hfill \\ \end{gathered} \right.\)
- Hỗn hợp muối Z gồm HCOONa (A): 0,12 mol và CH3COONa (B): 0,08 mol Þ a : b = 1,243
Kim loại nào sau đây tan được trong dung dịch kiềm dư?
Kim loại Al tan được trong dung dịch kiềm dư:
2A1 + 2NaOH + 2H2O → 2NaAlO2 + 3H2
Đáp án A
Chất nào sau đây được gọi là xút ăn da?
NaOH được gọi là xút ăn da.
Đáp án D
Chất X là chất rắn dạng sợi, màu trắng, là nguyên liệu sản xuất tơ nhân tạo, thuốc súng không khói và chế tạo phim ảnh. Chất X là:
Chất X là chất rắn dạng sợi, màu trắng, là nguyên liệu sản xuất tơ nhân tạo, thuốc súng không khói và chế tạo phim ảnh X là xenlulozơ
Đáp án D
Kim loại nào sau đây được điều chế bằng phương pháp thủy luyện ?
Phương pháp thủy luyện thường dùng để điều chế các kim loại sau Mg (thường là kim loại yếu). Vậy kim loại Cu được điều chế bằng phương pháp thủy luyện.
Đáp án C
Polietilen là chất dẻo mềm, được dùng nhiều để làm
Polietilen là chất dẻo mềm, được dùng nhiều để làm màng mỏng, vật liệu cách điện, bình chứa.
Đáp án A
Thạch cao nung được dùng để nặn tượng, bó bột. Công thức của thạch cao nung là:
Công thức của thạch cao nung là CaSO4.H2O
Đáp án B
Khử hết m gam CuO bằng dư, thu được chất rắn X. Cho X tan hết trong dung dịch dư thu được 2,24 lít khí NO (sản phẩm khử duy nhất của N+5). Giá trị của m là:
Các phương trình hóa học xảy ra:
CuO + H2 → Cu + H2O (1)
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O (2)
Theo (2)= nCu = 3/2. nNO = 3/2.0,1 = 0,15 mol
Theo (1)= nCuo= nCu = 0,15 mol
=> mCuO = 0,15.80 = 12 (g)
Đáp án D
Cho 2,3 gam Na vào 100 ml dung dịch AlCl3 0,3M, sau khi các phản ứng xảy ra hoàn toàn thu được m gam kết tủa. Giá trị của m là:
Ta có: nNaOH = nNa = 0,1 mol; nAlCl3 = 0,03 mol
Tính tỉ lệ k= nOH-/nAl3+ = 3,33
Ta có 3 < k < 4 nên kết tủa tan 1 phần → n↓ = 4.nAl3+ - nOH- = 4. 0,03 - 0,1 = 0,02 mol
→ mAl(OH)3 = 0,02.78 = 1,56 (gam)
Đáp án C
Cách pha loãng dung dịch H2SO4 đặc (theo hình vẽ bên) đúng kĩ thuật là:
H2SO4 tan vô hạn trong nước và tỏa rất nhiều nhiệt. Nếu ta rót nước vào H2SO4 đặc, nước sôi đột ngột và kéo theo những giọt axit bắn ra xung quanh gây nguy hiểm. Vì vậy muốn pha loãng axit H2SO4 đặc nguội, người ta phải rót từ từ H2SO4 đặc vào H2O và khuấy đều.
Đáp án C
Kim loại nào sau đây dẫn điện tốt nhất?
Kim loại Ag dẫn điện tốt nhất.
Đáp án D
CO2 tác dụng với lượng dư dung dịch nào sau đây tạo kết tủa?
Khi cho CO2 vào lượng dư dung dịch Ca(OH)2 ta thu được kết tủa CaCO3:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Đáp án D
Quá trình nào sau đây không gây ô nhiễm môi trường không khí?
Quá trình quang hợp của cây xanh không gây ô nhiễm môi trường không khí vì quá trình đó hấp thụ khí CO2 và tạo ra khí oxi.
Đáp án C
Este nào sau đây thuộc loại este no, đơn chức, mạch hở?
Công thức tổng quát của este no, đơn chức, mạch hở là CnH2nO2 (n ≥2).
Vậy este CH3COOCH3 thuộc loại este no, đơn chức, mạch hở.
Đáp án C
Kim loại sắt không phản ứng được với dung dịch nào sau đây?
Phản ứng Fe + ZnCl2 không xảy ra vì tính khử của Fe yếu hơn tính khử của Zn.
Đáp án D
Khi cho dung dịch anbumin tác dụng với Cu(OH)2 thì thu được dung dịch có màu:
Bản chất của anbumin là protein nên khi cho dung dịch anbumin tác dụng với Cu(OH)2 thì thu được dung dịch có màu tím.
Đáp án A
Dung dịch chứa chất nào sau đây không làm đổi màu quỳ tím?
- Glyxin có công thức NH2-CH2-COOH có số nhóm NH2 = số nhóm COOH nên không làm đổi màu quỳ tím.
- Metylamin làm quỳ tím hóa xanh
- Axit glutamic làm quỳ tím hóa đỏ (do có 2 nhóm COOH, 1 nhóm NH2)
- Lysin làm quỳ tím hóa xanh (do có 1 nhóm COOH, 2 nhóm NH2)
Đáp án A
Cho 0,5 mol hơi nước qua cacbon nung đỏ thu được 0,9 mol hỗn hợp X gồm CO, . Cho X hấp thụ vào 100 ml dung dịch NaOH 1,5M, thu được dung dịch Z. Cho từ từ dung dịch Z vào 120 ml dung dịch HCl 1M, thu được V lít . Biết các phản ứng xảy ra hoàn toàn. Giá trị của V là:
Hướng dẫn giải:
Ta có: nC phản ứng = nX - nH2O = 0,4 mol
Bảo toàn electron ta có:
4. nC phản ứng = 2nCO+2.nH2 → nCO + nH2 = 0,8 mol → nCO2 = 0,9 - 0,8 = 0,1 mol
Ta có: nNaOH = 0,15 mol
→ Tỉ lệ 1< nNaOH/nCO2< 2 nên Z chứa 2 muối Na2CO3(0,05 mol) và NaHCO3 (0,05 mol)
Khi cho từ từ Z vào dung dịch HCl xảy ra các phương trình sau:
Na2CO3 + 2HCl → 2NaCl + CO2 + H2O
NaHCO3 + HCl → NaCl + CO2 + H2O
Đặt nNa2CO3 phản ứng = nNaHCO3 phản ứng = z mol
→ nHCl = 2z + z= 0,12 mol → z = 0,04 mol → nCO2 = z + z = 0,08 mol → V=1,792 (lít)
Đáp án B
Thủy phân hoàn toàn cacbohiđrat A thu được hai monosaccarit X và Y, Hiđro hóa X hoặc Y đều thu được chất hữu cơ Z. Hai chất A và Z lần lượt là:
C12H22O11(saccarozo)+ H2O →C6H12O6(glucozơ) + C6H12O6 (fructozơ)
CH2OH[CHOH]4CH=O + H2 →CH2OH[CHOH]4CH2OH (sobitol)
CH2OH(CHOH]3COCH2OH + H2 →CH2OH(CHOH]4CH2OH (sobitol)
Vậy A và Z là saccarozơ và sobitol.
Đáp án D
Thí nghiệm nào sau đây xảy ra ăn mòn điện hóa học?
- A không có ăn mòn điện hóa do không có môi trường dd điện li
- B không có ăn mòn điện hóa do không có 2 điện cực
- C có ăn mòn điện hóa do: 2A1 + 3CuSO4 → Al2(SO4)3 + 3Cu
Thí nghiệm sinh ra Cu bám vào lá Al tạo thành 2 điện cực Al-Cu cùng tiếp xúc với dung dịch chất điện li (muối).
- D không có ăn mòn điện hóa do không có 2 điện cực
Đáp án C
Số hợp chất hữu cơ đơn chức, mạch hở có công thức phân tử C2H4O2 là:
Hợp chất hữu cơ đơn chức, mạch hở có công thức phân tử C2H4O2 là: CH3COOH và HCOOCH3
Vậy có tất cả 2 hợp chất hữu cơ đơn chức, mạch hở.
Đáp án B
Từ chất X (C3H8O4) mạch hở, không phản ứng tráng bạc và có các phản ứng sau:
X + 2NaOH → \(Y + Z{\text{ }} + {H_2}O;\)
Z + HCl →T + NaCl;
\(T\xrightarrow{{{H_2}S{O_4}dac}}Q + {H_2}O\)
Biết Q làm mất màu dung dịch brom. Kết luận nào sau đây đúng ?
X không tráng bạc nên không có HCOO
Vì X tác dụng với NaOH tạo H2O nên X có nhóm COOH
Do đó X là CH3COO-CH2-CH2-COOH
Khi đó ta có các phương trình phản ứng sau:
CH3COO-CH2-CH2-COOH (X) + 2NaOH → CH3COONa (Y) + HO-CH2-CH2-COONa (Z) + H2O;
HO-CH2-CH2-COONa (Z) + HC1 → HO-CH2-CH2-COOH (T) + NaCl;
HO-CH2-CH2-COOH (T) CH2-CH-COOH (Q) + H20
Vậy: Y là CH3COONa, Z là HO-CH2-CH2-COONa, T là HO-CH2-CH2-COOH; Q là CH2=CH-COOH Phát biểu A đúng vì Y là CH3COONa (natri axetat)
Phát biểu B sai vì T là HO-CH2-CH2-COONa, đây là hợp chất hữu cơ tạp chức.
Phát biểu C sai vì X là CH3COO-CH2-CH2-COOH là hợp chất hữu cơ tạp chức
Phát biểu D sai vì Q là axit acrylic
Đáp án A
Dãy chuyển hóa theo sơ đồ
Các chất X, Y, Z, T thỏa mãn sơ đồ trên tương ứng là
Ta có: NaHCO3 + Ba(OH)2 → NaOH + BaCO3 + H2O
NaOH + Al(OH)3 → NaAlO2 + 2H2O
NaAlO2 + CO2dư + H2O → NaHCO3 + Al(OH)3
Vậy các chất các chất X, Y, Z, T thỏa mãn sơ đồ trên tương ứng là NaHCO3, NaOH, NaAlO2, Al(OH)3.
Đáp án B
Cho 5,6 lít hỗn hợp X gồm propin và H2 qua Ni đun nóng, thu được hỗn hợp khí Y (chỉ gồm các hiđrocacbon) có tỉ khối so với H2 bằng 21,5. Hỗn hợp Y phản ứng tối đa với a mol Br2 trong dung dịch. Giá trị của a là:
Ta có nX = 0,25 mol gồm CH4 (x mol) và H2 (y mol)
Suy ra x+y=0,25 (1)
C3H4 + H2 → C3H6
C3H4 + 2H2 → C3H8
Vì hỗn hợp Y chỉ gồm các hiđrocacbon nên ny =x mol
Bảo toàn khối lượng ta có mx = my
→ 40x + 2y = 21,5.2x (2)
Giải hệ (1) và (2) ta được x = 0,1 và y = 0,15
Bảo toàn số mol liên kết pi ta có: 2x =y+ nBr2 → nBr2 = 0,05 mol
Vậy giá trị của a là 0,05.
Đáp án A
Cho các chất: HCl, NaHCO3, Al, Fe(OH)3. Số chất tác dụng được với dung dịch NaOH là
Các chất: HCl, NaHCO3, Al tác dụng được với dung dịch NaOH (có 3 chất).
Đáp án B
Thủy phân 68,4 gam saccarozơ trong môi trường axit với hiệu suất 92%, sau phản ứng thu được dung dịch chứa m gam glucozơ. Giá trị của m là:
C12H22O11 (saccarozơ)+ H2O →C6H12O6 (glucozơ) + C6H12O6 (fructozơ)
Ta có: nglucozo = nsaccarozo = 0,2 mol
Suy ra mglucozo (PT) = 0,2.180 = 36 (gam)
Do hiệu suất phản ứng đạt 92% nên msản phẩm (thực tế) = 36.92% = 33,12 (gam).
Đáp án A
Đốt cháy hoàn toàn hỗn hợp M gồm hai amin no, đơn chức, mạch hở X và Y (có số mol bằng nhau, MX < MY) cần lượng vừa đủ 13,44 lít O2, thu được H2O, N2 và 6,72 lít CO2. Chất Y là:
Ta có: nO2 = 0,6 mol; nCO2 = 0,3 mol
Bảo toàn nguyên tố O ta có 2nO2 = 2nCO2 + nH2O → nH2O = 0,6 mol
Đặt công thức chung của 2 amin no, đơn chức, mạch hở X và Y là CnH2n+3N
CnH2n+3N + (3n/2+3/4) O2 → nCO2 + (2n+3)/2 H2O
Suy ra nM = (nH2O + nCO2)/1,5 = 0,2 mol
Suy ra số nguyên tử C = nCO2/nM=0,3: 0,2 = 1,5
Do hai chất có cùng số mol nên X là CH3N và Y là C2H7N (etylamin).
Đáp án A
Cho các chất: NaHCO3, Mg(OH)2, CH3COOH, HCl. Số chất điện li mạnh là:
Các chất điện li mạnh gồm NaHCO3, HCl (có 2 chất).
Đáp án C
Cho các polime sau: polietilen, tinh bột, tơ tằm, xenlulozơ triaxetat, polibutađien. Số polime thiên nhiên là:
Polime thiên nhiên là các polime có sẵn trong tự nhiên.
Các polime thiên nhiên gồm tinh bột, tơ tằm (2 polime).
Đáp án C
Thủy phân hoàn toàn a mol triglixerit X trong dung dịch NaOH vừa đủ, thu được glixerol và m gam hỗn hợp muối. Đốt cháy hoàn toàn a mol X cần vừa đủ 7,75 mol O2 và thu được 5,5 mol CO2. Mặt khác a mol X tác dụng tối đa với 0,2 mol Br2 trong dung dịch. Giá trị của m là:
Độ bất bão hòa của X là k = 0,2/a + 3
* Khi đốt cháy X:
Bảo toàn nguyên tố O ta có: 6.nx + 2.no2 = 2nCO2 + nH2O
Suy ra nH2O = 6a + 2.7,75 - 2.5,5 = 6a +4,5 (1)
Mặt khác: nX.(k - 1) = nCO2 + nH2O+ a.(0,2/a + 3 – 1) = 5,5 - (6a +4,5)
Giải phương trình trên ta được a = 0,1
Thay vào (1) ta được nH2O= 5,1 (mol)
Bảo toàn khối lượng cho phản ứng đốt cháy ta có: mX + mO2 = mCO2 + mH2O
→ mx = 85,8 gam
*Khi thủy phân triglixerit X trong NaOH vừa đủ:
Gọi công thức của X là (RCOO)3C3H5.
(RCOO)3C3H5 + 3NaOH → 3RCOONa + C3H5(OH)3
0,1 0,3 0,1 mol
Bảo toàn khối lượng cho phản ứng thủy phân ta có:
m = mmuối = mX + mNaOH - mglixerol = 85,8 +0,3.40 - 0,1.92 = 88,6 (gam)
Đáp án C